名校
解题方法
1 . 工业上利用废铁屑(含少量氧化铝和氧化铁等)生产高铁酸钾(K2FeO4)的工艺流程如图:
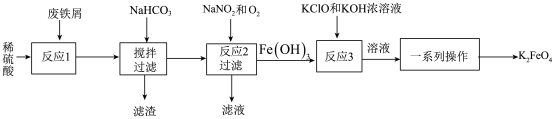
已知:流程中Fe2+被氧化的过程中NO可做催化剂。
回答下列问题:
(1)反应1中发生的氧化还原反应的离子方程式为______ ,______ 。
(2)根据题意推测流程中加入NaHCO3的目的是______ 。
(3)反应2中Fe2+被氧化的过程中,控制起始时Fe2+的浓度、溶液体积和通入O2的速率不变,改变其他条件时,Fe2+被氧化的转化率(Fe2+被氧化的量与反应前Fe2+总量之比)随时间的变化如图所示。
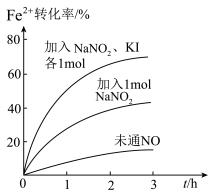
①加入NaNO2发生反应:2H++3NO =NO
=NO +2NO↑+H2O,该反应中若有6mol电子转移,得到的还原产物为
+2NO↑+H2O,该反应中若有6mol电子转移,得到的还原产物为______ mol。
②加入NaNO2、KI发生反应:4H++2NO +2I-=2NO↑+I2+2H2O,解释图中该条件下能进一步提高单位时间内Fe2+转化率的原因:
+2I-=2NO↑+I2+2H2O,解释图中该条件下能进一步提高单位时间内Fe2+转化率的原因:_____ 。
(4)写出反应3的离子方程式:______ 。
(5)K2FeO4可作为新型多功能水处理剂,其具有杀菌消毒功能的原因是_____ 。

已知:流程中Fe2+被氧化的过程中NO可做催化剂。
回答下列问题:
(1)反应1中发生的氧化还原反应的离子方程式为
(2)根据题意推测流程中加入NaHCO3的目的是
(3)反应2中Fe2+被氧化的过程中,控制起始时Fe2+的浓度、溶液体积和通入O2的速率不变,改变其他条件时,Fe2+被氧化的转化率(Fe2+被氧化的量与反应前Fe2+总量之比)随时间的变化如图所示。

①加入NaNO2发生反应:2H++3NO
 =NO
=NO +2NO↑+H2O,该反应中若有6mol电子转移,得到的还原产物为
+2NO↑+H2O,该反应中若有6mol电子转移,得到的还原产物为②加入NaNO2、KI发生反应:4H++2NO
 +2I-=2NO↑+I2+2H2O,解释图中该条件下能进一步提高单位时间内Fe2+转化率的原因:
+2I-=2NO↑+I2+2H2O,解释图中该条件下能进一步提高单位时间内Fe2+转化率的原因:(4)写出反应3的离子方程式:
(5)K2FeO4可作为新型多功能水处理剂,其具有杀菌消毒功能的原因是
您最近一年使用:0次
2023-03-29更新
|
346次组卷
|
2卷引用:四川省德阳中学2022-2023学年高一下学期3月月考化学试题
2 . 侯德榜先生为我国的制碱工业做出了突出贡献,其制碱原理为NH3+NaCl+CO2+H2O=NaHCO3↓+NH4Cl。实验室模拟原理流程如下:

下列说法错误的是

下列说法错误的是
| A.先通入NH3的目的是造成碱性环境利于CO2的吸收 |
| B.操作①为过滤、操作②为灼烧 |
| C.该模拟流程应用了溶解性和热稳定性:Na2CO3>NaHCO3 |
| D.蒸发母液可得到纯净的NH4Cl |
您最近一年使用:0次
解题方法
3 . 下列叙述正确的是( )
| A.除去MgCl2溶液中混有的FeCl2溶液工业上一般先将Fe2+氧化为Fe3+再以Fe(OH)3除去,因为Fe(OH)2为白色絮状沉淀不易过滤。 |
| B.向饱和的FeCl3溶液中加入适量的NaOH溶液并加热至溶液呈红褐色,可以制得Fe(OH)3胶体 |
C.向饱和的NaHCO3溶液中滴加酚酞,溶液呈浅红色是因为 电离产生了H+ 电离产生了H+ |
| D.铝箔用砂纸仔细打磨,除去表面的保护膜,在酒精灯上加热会观察到铝受热融化并滴落 |
您最近一年使用:0次



