2023高二上·全国·专题练习
1 . 沉淀转化的应用
(1)锅炉除水垢(含有CaSO4):CaSO4(s) CaCO3(s)
CaCO3(s) Ca2+(aq),反应为:
Ca2+(aq),反应为:_______ 。
(2)自然界中矿物的转化:原生铜的硫化物 CuSO4溶液
CuSO4溶液 铜蓝(CuS),反应为:
铜蓝(CuS),反应为:_______ 。
(3)工业废水处理:工业废水处理过程中,重金属离子可利用沉淀转化原理用FeS等难溶物转化为HgS、Ag2S、PbS等沉淀。用FeS除去Hg2+的离子方程式:_______ 。
(1)锅炉除水垢(含有CaSO4):CaSO4(s)
 CaCO3(s)
CaCO3(s) Ca2+(aq),反应为:
Ca2+(aq),反应为:(2)自然界中矿物的转化:原生铜的硫化物
 CuSO4溶液
CuSO4溶液 铜蓝(CuS),反应为:
铜蓝(CuS),反应为:(3)工业废水处理:工业废水处理过程中,重金属离子可利用沉淀转化原理用FeS等难溶物转化为HgS、Ag2S、PbS等沉淀。用FeS除去Hg2+的离子方程式:
您最近一年使用:0次
2023高二上·全国·专题练习
解题方法
2 . 难溶电解质沉淀溶解平衡的影响因素
已知沉淀溶解平衡:Mg(OH)2(s)=Mg2+(aq)+2OH-(aq)
Q:离子积对于AmBn(s)=mAn+(aq)+nBm-(aq)任意时刻Q=cm(An+)·cn(Bm-)。
(1)Q>Ksp,溶液过饱和,有_______ 析出,直至溶液_______ ,达到新的平衡。
(2)Q=Ksp,溶液饱和,沉淀与溶解处于_______ 。
(3)Q<Ksp,溶液未饱和,无_______ 析出,若加入过量难溶电解质,难溶电解质_______ 直至溶液_______ 。
已知沉淀溶解平衡:Mg(OH)2(s)=Mg2+(aq)+2OH-(aq)
| 条件改变 | 移动方向 | c(Mg2+) | c(OH-) |
| 加少量水 | |||
| 升温 | |||
| 加MgCl2(s) | |||
| 加盐酸 | |||
| 加NaOH(s) |
(1)Q>Ksp,溶液过饱和,有
(2)Q=Ksp,溶液饱和,沉淀与溶解处于
(3)Q<Ksp,溶液未饱和,无
您最近一年使用:0次
2023高二上·全国·专题练习
3 . 沉淀的溶解
(1)沉淀溶解的原理
根据平衡移动原理,对于在水中难溶的_______ ,如果能设法不断地移去平衡体系中的_______ ,使平衡向_______ 的方向移动,就可以使沉淀_______ 。
(2)实验探究:Mg(OH)2沉淀溶解
(3)沉淀溶解的方法
①酸溶解法:用强酸溶解的难溶电解质有_______ 等。
如CaCO3难溶于水,却易溶于盐酸,原因是:CaCO3在水中存在沉淀溶解平衡为CaCO3(s)=Ca2+(aq)+CO (aq),当加入盐酸后发生反应
(aq),当加入盐酸后发生反应_______ ,c(CO )
)_______ ,溶液中CO 与Ca2+的离子积Q(CaCO3)<Ksp(CaCO3),沉淀溶解平衡向
与Ca2+的离子积Q(CaCO3)<Ksp(CaCO3),沉淀溶解平衡向_______ 方向移动。
②盐溶液溶解法:Mg(OH)2难溶于_______ ,能溶于盐酸、NH4Cl溶液中。溶于NH4Cl溶液反应的离子方程式为_______ 。
(1)沉淀溶解的原理
根据平衡移动原理,对于在水中难溶的
(2)实验探究:Mg(OH)2沉淀溶解
| 操作 |  |
| 现象 | ①浑浊;②澄清 |
| 理论分析 |  |
①酸溶解法:用强酸溶解的难溶电解质有
如CaCO3难溶于水,却易溶于盐酸,原因是:CaCO3在水中存在沉淀溶解平衡为CaCO3(s)=Ca2+(aq)+CO
 (aq),当加入盐酸后发生反应
(aq),当加入盐酸后发生反应 )
) 与Ca2+的离子积Q(CaCO3)<Ksp(CaCO3),沉淀溶解平衡向
与Ca2+的离子积Q(CaCO3)<Ksp(CaCO3),沉淀溶解平衡向②盐溶液溶解法:Mg(OH)2难溶于
您最近一年使用:0次
名校
4 . 下列反应的发生与“盐类水解平衡”或“难溶电解质的溶解平衡”无关 的是
| A.镁条与NH4Cl溶液反应生成H2 |
| B.NaHSO4溶液与NaOH溶液反应生成Na2SO4 |
| C.盐酸与CaCO3反应生成CO2 |
| D.Fe2(SO4)3溶液和Na2CO3溶液反应生成CO2 |
您最近一年使用:0次
2022-11-20更新
|
399次组卷
|
5卷引用:【知识图鉴】单元讲练测选择性必修1第3单元02基础练
5 . 某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):
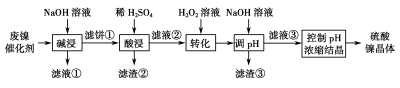
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
利用上述表格数据,计算Ni(OH)2的Ksp=___________ (列出计算式)。如果“转化”后的溶液中Ni2+浓度为1.0 mol·L-1,则“调pH”应控制的pH范围是___________ 。

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时(c=0.01 mol·L-1)的pH | 7.2 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时(c=1.0×10-5 mol·L-1)的pH | 8.7 | 4.7 | 3.2 | 9.0 |
利用上述表格数据,计算Ni(OH)2的Ksp=
您最近一年使用:0次
6 . 已知: 时,
时, 的溶度积分别为
的溶度积分别为 .下列说法正确的是
.下列说法正确的是
 时,
时, 的溶度积分别为
的溶度积分别为 .下列说法正确的是
.下列说法正确的是| A.可溶性硫化物可作为处理上述金属离子的沉淀剂 |
B.上述三种物质溶解度最小的是 |
C.在硫化铜悬浊液中滴加几滴 溶液,会生成 溶液,会生成 沉淀 沉淀 |
D.向含 均为 均为 的溶液中通入 的溶液中通入 气体,产生沉淀的顺序依次为 气体,产生沉淀的顺序依次为 |
您最近一年使用:0次
7 . 化学与生产、生活密切相关。下列说法错误的是
| A.加入生石灰减少燃煤时排放的温室气体 |
| B.用Na2S除去工业废水中的Cu2+和Hg2+ |
| C.用纯碱溶液除油污,加热可提高去污能力 |
| D.用硫酸铁除去水中的悬浮物 |
您最近一年使用:0次
8 . 某炼铁废渣中含有大量CuS及少量铁的化合物,工业上以该废渣为原料生产CuCl2▪2H2O晶体的工艺流程如图,下列说法错误的是


| A.焙烧后的废气能使酸性高锰酸钾溶液褪色 |
| B.氧化步骤中,用双氧水代替氯气会更好 |
| C.调节pH选用的试剂可以是CuO固体 |
| D.CuCl2▪2H2O晶体直接加热可制得CuCl2固体 |
您最近一年使用:0次
9 . 已知几种难溶电解质的溶度积常数Ksp(25℃)如下:
向100mL含 、
、 和
和 浓度均为0.01mol/L的溶液中逐滴加入0.001mol/L的
浓度均为0.01mol/L的溶液中逐滴加入0.001mol/L的 溶液,下列说法正确的是
溶液,下列说法正确的是
| 难溶电解质 | ZnS | CuS | HgS |
| Ksp |  |  | 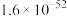 |
 、
、 和
和 浓度均为0.01mol/L的溶液中逐滴加入0.001mol/L的
浓度均为0.01mol/L的溶液中逐滴加入0.001mol/L的 溶液,下列说法正确的是
溶液,下列说法正确的是A. 先沉淀 先沉淀 | B. 先沉淀 先沉淀 | C. 先沉淀 先沉淀 | D.同时沉淀 |
您最近一年使用:0次
10 . 孔雀石主要含碱式碳酸铜[Cu2(OH)2CO3],还含少量Fe、Si的化合物。
实验室以孔雀石为原料制备CuSO4及CaCO3,首先将其溶于稀硫酸中,得到的溶液中含有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:
A.KMnO4 B.(NH4)2S C.H2O2 D.KSCN
(1)检验溶液中Fe3+的最佳试剂为______ (填代号)。
(2)为使Fe2+、Fe3+一起沉淀,需先加____ (填代号),此时发生反应的离子方程式为________ 。
(3)然后再加_______ (填化学式)调整溶液的pH只生成Fe(OH)3沉淀。
实验室以孔雀石为原料制备CuSO4及CaCO3,首先将其溶于稀硫酸中,得到的溶液中含有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:
A.KMnO4 B.(NH4)2S C.H2O2 D.KSCN
(1)检验溶液中Fe3+的最佳试剂为
(2)为使Fe2+、Fe3+一起沉淀,需先加
(3)然后再加
您最近一年使用:0次



