1 . 已知25 ℃时,AgI饱和溶液中c(Ag+)为1.23×10-8mol·L-1,AgCl的饱和溶液中c(Ag+)为1.25×10-5mol·L-1。若在5 mL含有KCl和KI各为0.01 mol·L-1的溶液中,加入8 mL 0.01 mol·L-1AgNO3溶液,下列叙述正确的是( )
| A.混合溶液中c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-) |
| B.混合溶液中c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-) |
| C.加入AgNO3溶液时首先生成AgCl沉淀 |
D.混合溶液中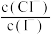 约为1.02×10-3 约为1.02×10-3 |
您最近一年使用:0次
2020-02-16更新
|
234次组卷
|
2卷引用:贵州省荔波高级中学2019-2020学年高二上学期期末考试化学试题
解题方法
2 . 下表中实验操作、现象以及所得出的结论都正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 向盛有  溶液的试管中,先滴加几滴 溶液的试管中,先滴加几滴 KCl溶液,再滴加 KCl溶液,再滴加 KI溶液 KI溶液 | 先出现白色沉淀,后出现黄色沉淀 |  |
| B | 将适量 和 和 分别通入装有 分别通入装有 溶液的两支试管中 溶液的两支试管中 | 一支试管出现白色沉淀,另一支试管无明显现象 | 出现的白色沉淀是 |
| C | 取少量 晶体溶于适量的蒸馏水,再加入硝酸酸化的 晶体溶于适量的蒸馏水,再加入硝酸酸化的 溶液 溶液 | 产生白色沉淀 |  中含 中含 |
| D | 湿润的KI淀粉试纸靠近气体Y | 试纸变蓝 | Y可能是 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-02-06更新
|
515次组卷
|
3卷引用:夯基提能2020届高三化学选择题对题专练——氧化还原反应的实际应用(提升练)
夯基提能2020届高三化学选择题对题专练——氧化还原反应的实际应用(提升练)夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——溶度积常数及相关计算(已下线)第12练 原子结构与元素周期表-2022年【寒假分层作业】高一化学(人教版2019)
名校
解题方法
3 . 下列解释实验现象的反应方程式正确的是
| A.切开的金属Na暴露在空气中,光亮表面逐渐变暗:2Na+O2=Na2O2 |
| B.向AgC1悬浊液中滴加Na2S溶液,白色沉淀变成黑色:2AgCl+S2- =Ag2S↓+2Cl- |
| C.Na2O2在潮湿的空气中放置一段时间,变成白色粘稠物:2Na2O2+CO2=2Na2CO3+O2 |
| D.FeCl2溶液中滴加NaClO溶液生成红褐色沉淀:2Fe2+ + ClO- + 5H2O= 2Fe(OH)3↓+Cl-+ 4H+ |
您最近一年使用:0次
4 . 以软锰矿、石灰石和含SO2的工业尾气为原料可制备K2SO4、Mn3O4,如图是该生产的工艺流程:

下列判断正确的是

下列判断正确的是
| A.反应Ⅰ是CaCO3转化为CaSO3 |
| B.反应Ⅱ是NH3提供碱性环境,微溶物转化为难溶物 |
| C.反应Ⅲ加入的试剂a是氨水 |
| D.反应Ⅳ利用了SO2的氧化性和酸性 |
您最近一年使用:0次
5 . 下列实验方案中,不能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 除去CO2气体中的SO2气体 | 将混合气体通入饱和碳酸氢钠溶液,洗气 |
| B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
| C | 验证Br2的氧化性强于I2 | 向少量溴水加入KI溶液中,再加入CCl4,振荡,静置,可观察到下层液体呈紫色 |
| D | 验证Fe(OH)3的溶解度小于Mg(OH)2 | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2016-12-09更新
|
198次组卷
|
2卷引用:2017届山西省康杰中学高三上学期10月月考化学试卷
13-14高三·全国·课时练习
6 . 下列说法不正确的是
| A.活性炭、SO2、Na2O2都能使品红溶液褪色,但原理不同 |
| B.同温同压下,两份相同质量的铁粉,分别与足量的稀硫酸和稀硝酸反应,产生气体的体积不相等 |
| C.将SO2气体通入BaCl2溶液中至饱和,未见沉淀生成,继续通入NO2则有沉淀生成 |
| D.将足量Cl2通入NaBr、NaI的混合溶液中,反应后将溶液蒸干并充分灼烧,剩余的固体物质成分为NaCl |
您最近一年使用:0次



