解题方法
1 . 深埋在潮湿土壤中的铁管道,在硫酸盐还原菌作用下,能被硫酸根离子腐蚀,其电化学腐蚀原理如下图所示。下列转述正确的是
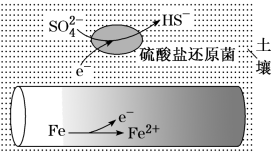

| A.此铁管道发生的是吸氧腐蚀 |
| B.输送暖气的管道也易发生此类腐蚀 |
| C.在这种情况下,土壤的c(OH-)增大 |
| D.若管道上刷富铜油漆可以延缓管道的腐蚀 |
您最近一年使用:0次
2021-12-14更新
|
300次组卷
|
2卷引用:福建省漳州市正兴学校2021-2022学年高二上学期期中考试化学试题
2 . 完成下列各小题
(1)已知在25℃、101kPa时,4g H2完全燃烧生成液态水,放出571.6kJ的热量,写出表示H2摩尔燃烧焓的热化学方程式:______________________ 。
(2)金属腐蚀一般可分为化学腐蚀和电化学腐蚀。炒过菜的铁锅未及时清洗容易发生___________ 腐蚀而生锈。请写出铁锅生锈过程的正极反应式:_______________________ 。
(3)图中甲池的总反应式为N2H4+O2=N2+2H2O。
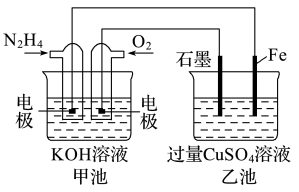
①甲池中负极上发生的是____________________ (填“氧化反应”或“还原反应”),乙池中SO 向
向_________ 移动(填“左”或“右”)。
②乙池中电解反应的离子方程为_________________________ 。
③要使乙池恢复到电解前的状态,应向溶液中加入_____________ (填化学式)。
(1)已知在25℃、101kPa时,4g H2完全燃烧生成液态水,放出571.6kJ的热量,写出表示H2摩尔燃烧焓的热化学方程式:
(2)金属腐蚀一般可分为化学腐蚀和电化学腐蚀。炒过菜的铁锅未及时清洗容易发生
(3)图中甲池的总反应式为N2H4+O2=N2+2H2O。

①甲池中负极上发生的是
 向
向②乙池中电解反应的离子方程为
③要使乙池恢复到电解前的状态,应向溶液中加入
您最近一年使用:0次
3 . 电化学保护法是常用的金属防腐的手段,在题图所示的情境中,下列有关说法正确的是


A.图1正极的电极反应式为 |
| B.图1中钢铁的活动性比金属M的活动性强 |
| C.图2高硅铸铁的作用是作为损耗阳极材料和传递电流 |
| D.图2防止金属腐蚀的方法叫做外加电流的阴极电保护法 |
您最近一年使用:0次
2021-12-06更新
|
496次组卷
|
4卷引用:福建省宁德市同心顺联盟校2021—2022学年高二上学期期中联考化学试题
福建省宁德市同心顺联盟校2021—2022学年高二上学期期中联考化学试题福建省福清西山学校2021-2022学年高二上学期12月月考化学试题第三节 金属的腐蚀与防护(已下线)第28讲 金属的腐蚀与防护(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
4 . 研究金属腐蚀和防腐的原理很有现实意义。

(1)甲图为人教版教材中探究钢铁的吸氧腐蚀的装置。某兴趣小组按该装置实验,导管中液柱的上升缓慢,下列措施可以更快更清晰观察到水柱上升现象的有___________(填序号)。
(2)该小组将甲图装置改进成乙图装置并进行实验,导管中红墨水液柱高度随时间的变化如下表,根据数据判断腐蚀的速率随时间逐渐___________ (填“加快”、“不变”、“减慢”), 你认为影响因素为___________ 。
(3)为探究铁钉腐蚀实验 a、b 两点所发生的反应,进行以下实验,请完成表格空白:
根据以上实验探究,试判断___________ (填“a”或“b”)为负极,该点腐蚀更严重。
(4)金属阳极钝化是一种电化学防腐方法。将 Fe 作阳极置于 H2SO4溶液中,一定条件下Fe 钝化形成致密 Fe3O4氧化膜,试写出该阳极电极反应式___________ 。

(1)甲图为人教版教材中探究钢铁的吸氧腐蚀的装置。某兴趣小组按该装置实验,导管中液柱的上升缓慢,下列措施可以更快更清晰观察到水柱上升现象的有___________(填序号)。
| A.用纯氧气代替试管内空气 |
| B.用酒精灯加热试管提高温度 |
| C.将铁钉换成铁粉和炭粉混合粉末 |
| D.换成更细的导管,水中滴加红墨水 |
| 时间/min | 1 | 3 | 5 | 7 | 9 |
| 液柱高度/cm | 0.8 | 2.1 | 3.0 | 3.7 | 4.2 |
| 实验操作 | 实验现象 | 实验结论 |
| 向 NaCl溶液中滴加 2~3 滴酚酞指示剂 | a 点附近溶液出现红色 | a 点电极反应为① |
| 然后再滴加 2~3 滴② | b 点周围出现蓝色沉淀 | b 点电极反应为③ |
(4)金属阳极钝化是一种电化学防腐方法。将 Fe 作阳极置于 H2SO4溶液中,一定条件下Fe 钝化形成致密 Fe3O4氧化膜,试写出该阳极电极反应式
您最近一年使用:0次
2021-11-26更新
|
514次组卷
|
4卷引用:福建省厦门市厦门双十中学2021-2022学年上学期期中考试化学试题
福建省厦门市厦门双十中学2021-2022学年上学期期中考试化学试题(已下线)第四单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)第四章 电化学基础 单元综合检测-2021-2022学年高二化学课后培优练(人教版选修4)河南省南阳市方城县第一高级中学2022-2023学年高二上学期11月期中考试化学试题
名校
解题方法
5 . 如图所示三套实验装置,分别回答下列问题。
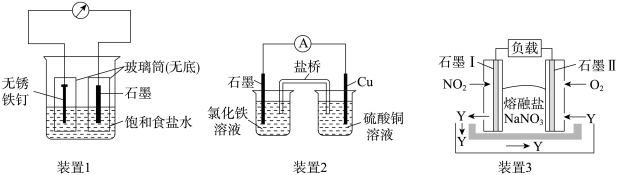
(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入K3[Fe(CN)6]溶液,即可观察到铁钉附近的溶液出现蓝色沉淀,表明铁被___________ (填“氧化”或“还原”);向插入石墨的玻璃筒内滴入酚酞溶液,可观察到石墨附近的溶液变红,该电极反应式为___________ 。
(2)装置2中的石墨作___________ (填“正”或“负”)极,该装置发生的总反应的离子方程式为___________ 。
(3)装置3为由NO2、O2、熔融盐NaNO3组成的燃料电池示意图。在使用过程中石墨I电极反应生成一种氧化物Y,则Y为___________ (填化学式);石墨II极的电极反应式为:___________ ;当石墨I极中有1molNO2参加反应时,石墨II极消耗的O2的体积___________ (标准状况下)。

(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入K3[Fe(CN)6]溶液,即可观察到铁钉附近的溶液出现蓝色沉淀,表明铁被
(2)装置2中的石墨作
(3)装置3为由NO2、O2、熔融盐NaNO3组成的燃料电池示意图。在使用过程中石墨I电极反应生成一种氧化物Y,则Y为
您最近一年使用:0次
6 . 钢铁防护方法有多种,图中的方法描述正确的是
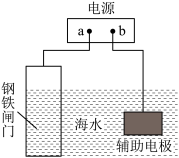

| A.b为电源负极 |
| B.电源改用导线连接进行防护时,辅助电极发生氧化反应 |
| C.电子流向:a→钢铁闸门→辅助电极→b→a |
| D.该方法是牺牲阳极的阴极保护法 |
您最近一年使用:0次
名校
7 . 自嗨锅的发热包主要成分有:硅藻土、铁粉、铝粉、焦炭粉、食盐、生石灰,使用时使发热包里面的物质与水接触即可。下列说法错误的是
| A.铁粉发生析氢腐蚀,缓慢放出热量,延长放热时间 |
| B.硅藻土可增大反应物的接触面积 |
| C.过程中形成微小原电池,正极反应为:O2+2H2O+4e-=4OH- |
| D.使用后的发热包含有熟石灰属于有害垃圾 |
您最近一年使用:0次
2021-11-08更新
|
123次组卷
|
3卷引用:福建省南平市高级中学2021-2022学年高二上学期期中考试化学(选考)试题
名校
解题方法
8 . 化学与人们的生活息息相关,下列说法错误的是
| A.农村推广风力发电、光伏发电有利于“碳达峰、碳中和” |
| B.可将港珠澳大桥钢骨架与外加直流电源的正极相连以保护它不受腐蚀 |
| C.升高温度,可使活化分子的百分数增大,反应速率加快 |
| D.合成氨工业采用700K是因为该温度下速率较快且催化剂活性大 |
您最近一年使用:0次
2021-11-08更新
|
83次组卷
|
2卷引用:福建省南平市高级中学2021-2022学年高二上学期期中考试化学(选考)试题
9 . 将金属M连接在钢铁设施表面构成原电池,可减缓水体中钢铁设施的腐蚀。在如图所示的情境中,下列有关说法正确的是
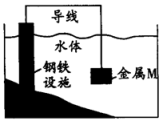

A.钢铁设施上的电极反应式为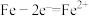 | B.电子流向:金属M→水体→钢铁设施表面 |
| C.M的金属性比Fe的金属性强 | D.钢铁设施在河水中的腐蚀速率比在海水中的快 |
您最近一年使用:0次
2021-10-28更新
|
143次组卷
|
2卷引用:福建泉州现代中学2021-2022学年高二上学期期中考试化学试题
名校
解题方法
10 . 下列有关电化学装置的说法正确的是




| A.甲图中正极的电极反应式为Ag2O+2e-+2H+=2Ag+H2O |
| B.乙图表示钢闸门用牺牲阳极的阴极保护法加以防护 |
| C.丙图中,盐桥中的K+向盛有ZnSO4溶液的烧杯中移动 |
| D.丁图中,X处补充稀NaOH溶液以增强溶液导电性 |
您最近一年使用:0次
2021-10-27更新
|
304次组卷
|
5卷引用:福建省厦门外国语学校石狮分校2021-2022学年高二上学期第一次月考化学试题



