名校
解题方法
1 . 下列有关化学反应原理的说法中,不正确的说法组合是
①有效碰撞一定能导致化学反应的发生
②难溶物的溶解度和 Ksp 的大小都仅仅只受温度的影响
③某反应正方向能自发进行,则逆方向一定难以自发进行
④某溶液的 pH 不受温度的影响,那么该溶液一定显强酸性
⑤用盐酸滴定氨水,若选择酚酞做指示剂,则测定的结果会偏小
⑥中和热的测定实验,若量取 NaOH 溶液的量筒仰视读数,则所测的△H 偏大
⑦金属的吸氧腐蚀比析氢腐蚀更普遍,但吸氧腐蚀的速率不如金属的析氢腐蚀
①有效碰撞一定能导致化学反应的发生
②难溶物的溶解度和 Ksp 的大小都仅仅只受温度的影响
③某反应正方向能自发进行,则逆方向一定难以自发进行
④某溶液的 pH 不受温度的影响,那么该溶液一定显强酸性
⑤用盐酸滴定氨水,若选择酚酞做指示剂,则测定的结果会偏小
⑥中和热的测定实验,若量取 NaOH 溶液的量筒仰视读数,则所测的△H 偏大
⑦金属的吸氧腐蚀比析氢腐蚀更普遍,但吸氧腐蚀的速率不如金属的析氢腐蚀
| A.②③ | B.①③⑥ | C.①③④ | D.②③⑥ |
您最近一年使用:0次
2 . 含可钝化金属的工业管道或反应器,由于会被内部溶液腐蚀,通过外接电源而钝化,称之为阳极保护法。下图是某金属外接电势与电流密度的变化关系,有关说法正确的是
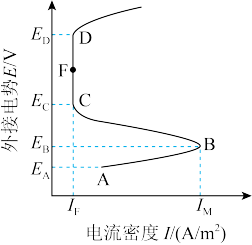

| A.阳极保护法中受保护的金属外接电源的负极 |
| B.电流密度越大,金属受保护程度越好 |
| C.CFD区,金属受到保护 |
| D.外接电势越高,对金属保护性越有效 |
您最近一年使用:0次
2022-06-14更新
|
912次组卷
|
4卷引用:江西省抚州市2022届高三下学期4月教学质量监测理综化学试题
江西省抚州市2022届高三下学期4月教学质量监测理综化学试题(已下线)专题11 金属的腐蚀与防护-备战2023年高考化学母题题源解密(广东卷)(已下线)第19讲 电解池 金属的电化学腐蚀与防护(练)-2023年高考化学一轮复习讲练测(全国通用)黑龙江省大庆实验中学实验三部2023-2024学年高三上学期阶段考试(二)化学试题
3 . 下列关于电化学的说法不正确的是
| A.铝制品可利用阳极氧化法处理表面,使之形成致密的氧化膜而起到防护作用 |
| B.水库的钢闸门接直流电源的正极,可以减缓闸门的腐蚀 |
| C.轮船在船壳水线以下常装有一些锌块,这是利用了牺牲阳极的阴极保护法 |
| D.氯碱工业选用阳离子交换膜隔离两个电极区 |
您最近一年使用:0次
2022-11-06更新
|
421次组卷
|
4卷引用:浙江省温州十校联合体2022-2023学年高二上学期期中联考化学试题
浙江省温州十校联合体2022-2023学年高二上学期期中联考化学试题湖南省雅礼中学2022-2023学年高二上学期第三次月考化学试题(已下线)【2022】【高二上】【期中考】【温州十校】【高中化学】【李鼎收集】浙江省温州市2022-2023学年高二上学期11月期中考试化学试题
名校
4 . 《我在故宫修文物》这部纪录片里关于古代青铜器的修复引起了某研学小组的兴趣。“修旧如旧”是文物保护的主旨。
(1)查阅高中教材得知铜锈为Cu2(OH)2CO3,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值。参与形成铜绿的物质有Cu和_______ 。
(2)继续查阅中国知网,了解到铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。考古学家将铜锈分为无害锈和有害锈,结构如图所示:
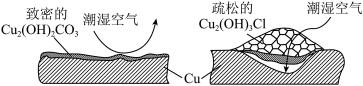
Cu2(OH)2CO3和Cu2(OH)3Cl分别属于无害锈和有害锈,请解释原因_____________ 。
(3)文献显示有害锈的形成过程中会产生CuCl(白色不溶于水的固体),请结合下图回答:
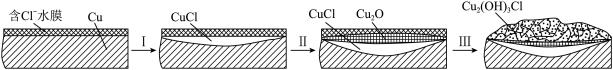
① 过程Ⅰ的正极反应物是___________ 。
② 过程Ⅰ负极的电极反应式是_____________ 。
(4)青铜器的修复有以下三种方法:
ⅰ.柠檬酸浸法:将腐蚀文物直接放在2%-3%的柠檬酸溶液中浸泡除锈;
ⅱ.碳酸钠法:将腐蚀文物置于含Na2CO3的缓冲溶液中浸泡,使CuCl转化为难溶的Cu2(OH)2CO3;
ⅲ.BTA保护法:
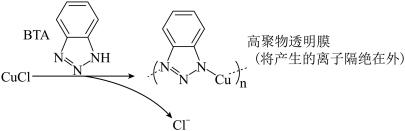
请回答下列问题:
①写出碳酸钠法的离子方程式___________________ 。
②三种方法中,BTA保护法应用最为普遍,分析其可能的优点有___________ 。
A.在青铜器表面形成一层致密的透明保护膜
B.替换出锈层中的Cl-,能够高效的除去有害锈
C.和酸浸法相比,不破坏无害锈,可以保护青铜器的艺术价值,做到“修旧如旧”
(1)查阅高中教材得知铜锈为Cu2(OH)2CO3,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值。参与形成铜绿的物质有Cu和
(2)继续查阅中国知网,了解到铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。考古学家将铜锈分为无害锈和有害锈,结构如图所示:

Cu2(OH)2CO3和Cu2(OH)3Cl分别属于无害锈和有害锈,请解释原因
(3)文献显示有害锈的形成过程中会产生CuCl(白色不溶于水的固体),请结合下图回答:

① 过程Ⅰ的正极反应物是
② 过程Ⅰ负极的电极反应式是
(4)青铜器的修复有以下三种方法:
ⅰ.柠檬酸浸法:将腐蚀文物直接放在2%-3%的柠檬酸溶液中浸泡除锈;
ⅱ.碳酸钠法:将腐蚀文物置于含Na2CO3的缓冲溶液中浸泡,使CuCl转化为难溶的Cu2(OH)2CO3;
ⅲ.BTA保护法:

请回答下列问题:
①写出碳酸钠法的离子方程式
②三种方法中,BTA保护法应用最为普遍,分析其可能的优点有
A.在青铜器表面形成一层致密的透明保护膜
B.替换出锈层中的Cl-,能够高效的除去有害锈
C.和酸浸法相比,不破坏无害锈,可以保护青铜器的艺术价值,做到“修旧如旧”
您最近一年使用:0次
2019-06-11更新
|
1882次组卷
|
7卷引用:福建省泉州市第六中学2022-2023学年高二上学期期中考化学试题
5 . 铁的腐蚀与防护与生产生活密切相关。
Ⅰ.研究铁的腐蚀
实验步骤如下:
步骤1:将铁粉放置于0.002
 溶液中浸泡,过滤后用水洗涤。
溶液中浸泡,过滤后用水洗涤。
步骤2:向15.00 mL 1 NaCl溶液(用盐酸调pH=1.78)中加入浸泡过的Fe粉。
NaCl溶液(用盐酸调pH=1.78)中加入浸泡过的Fe粉。
步骤3:采集溶液pH随时间变化的数据。
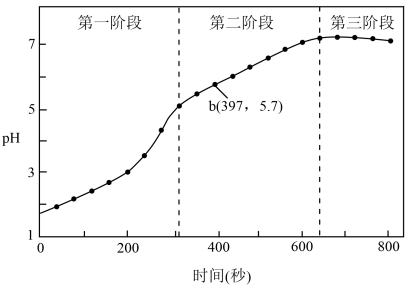
(1)第一阶段,主要发生析氢腐蚀,Cu上发生的电极反应为___________ 。
(2)第二、三阶段主要发生吸氧腐蚀。
①选取b点进行分析,经检验溶液中含有 ,写出Fe被腐蚀的总反应
,写出Fe被腐蚀的总反应___________ 。
②取b点溶液向其中滴加KSCN无明显现象,加入稀盐酸后立即变红。写出b点 被氧化的离子方程式
被氧化的离子方程式___________ 。
③依据b点发生的反应,分析第二阶段pH上升的原因是___________ 。
Ⅱ.研究铁的防护
(3)在铁表面镀锌可有效防止铁被腐蚀
已知: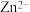 放电的速率缓慢且平稳,有利于得到致密、细腻的镀层。
放电的速率缓慢且平稳,有利于得到致密、细腻的镀层。
①镀件Fe应与电源的___________ 相连。
②向 电解液中加入NaCN溶液,将
电解液中加入NaCN溶液,将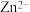 转化为
转化为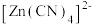 ,电解得到的镀层更加致密、细腻,原因是
,电解得到的镀层更加致密、细腻,原因是___________ 。
(4)电镀后的废水中含有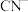 ,一种测定其含量的方法是:取废水50 mL,再加KI溶液1 mL,用c
,一种测定其含量的方法是:取废水50 mL,再加KI溶液1 mL,用c 
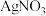 溶液滴定,消耗
溶液滴定,消耗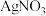 溶液V mL。已知:
溶液V mL。已知: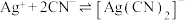 (无色)
(无色) 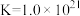 ,
,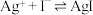
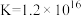 。
。
①滴定终点的现象是___________ 。
②废水中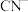 的含量是
的含量是___________  (填计算式)。
(填计算式)。
Ⅰ.研究铁的腐蚀
实验步骤如下:
步骤1:将铁粉放置于0.002

 溶液中浸泡,过滤后用水洗涤。
溶液中浸泡,过滤后用水洗涤。步骤2:向15.00 mL 1
 NaCl溶液(用盐酸调pH=1.78)中加入浸泡过的Fe粉。
NaCl溶液(用盐酸调pH=1.78)中加入浸泡过的Fe粉。步骤3:采集溶液pH随时间变化的数据。

(1)第一阶段,主要发生析氢腐蚀,Cu上发生的电极反应为
(2)第二、三阶段主要发生吸氧腐蚀。
①选取b点进行分析,经检验溶液中含有
 ,写出Fe被腐蚀的总反应
,写出Fe被腐蚀的总反应②取b点溶液向其中滴加KSCN无明显现象,加入稀盐酸后立即变红。写出b点
 被氧化的离子方程式
被氧化的离子方程式③依据b点发生的反应,分析第二阶段pH上升的原因是
Ⅱ.研究铁的防护
(3)在铁表面镀锌可有效防止铁被腐蚀
已知:
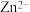 放电的速率缓慢且平稳,有利于得到致密、细腻的镀层。
放电的速率缓慢且平稳,有利于得到致密、细腻的镀层。①镀件Fe应与电源的
②向
 电解液中加入NaCN溶液,将
电解液中加入NaCN溶液,将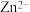 转化为
转化为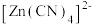 ,电解得到的镀层更加致密、细腻,原因是
,电解得到的镀层更加致密、细腻,原因是(4)电镀后的废水中含有
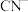 ,一种测定其含量的方法是:取废水50 mL,再加KI溶液1 mL,用c
,一种测定其含量的方法是:取废水50 mL,再加KI溶液1 mL,用c 
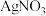 溶液滴定,消耗
溶液滴定,消耗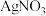 溶液V mL。已知:
溶液V mL。已知: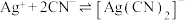 (无色)
(无色) 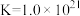 ,
,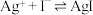
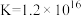 。
。①滴定终点的现象是
②废水中
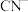 的含量是
的含量是 (填计算式)。
(填计算式)。
您最近一年使用:0次
2022-03-25更新
|
730次组卷
|
5卷引用:北京市丰台区2022届高三一模化学试题
6 . 下列说法正确的是
| A.反应物用量增加后,有效碰撞次数增多,反应速率一定增大 |
| B.等物质的量的硫蒸气和固体硫分别完全燃烧,后者放出热量多 |
| C.△H<0、△S>0的反应在任何温度下都能自发进行 |
| D.铜铁交接处,在潮湿的空气中直接发生反应:Fe-3e-=Fe3+,继而形成铁锈 |
您最近一年使用:0次
2022-02-19更新
|
358次组卷
|
2卷引用:湖北省荆州市八县市2021-2022学年高二上学期期末质量检测化学试题
解题方法
7 . 下列说法不正确 的是
| A.燃料电池、铅蓄电池都利用了原电池原理 |
| B.镀锌的铁表面有划痕时,仍比不镀锌的铁更难被腐蚀 |
C.在使用的燃煤中加入适量 ,可减少 ,可减少 及温室气体的排放 及温室气体的排放 |
| D.选用不同种类的催化剂,甲醛与苯酚可反应制得线型或体型的酚醛树脂 |
您最近一年使用:0次
名校
解题方法
8 . 青铜器在潮湿环境中发生电化学腐蚀原理如图所示:多孔催化层中的Cl-扩散到孔口,与电极产物作用生成多孔粉状锈Cu2(OH)3Cl,下列说法正确的是( )
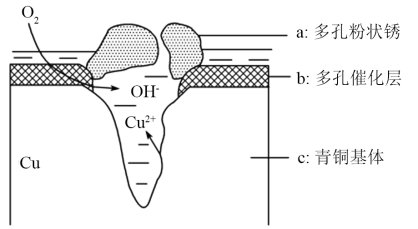

| A.此过程为电化学腐蚀中的析氢腐蚀 |
| B.电极b发生的反应:O2+4e-+2H2O=4OH- |
| C.生成Cu2(OH)3Cl的反应:2Cu2++3H2O+Cl-=Cu2(OH)3Cl↓+3H+ |
| D.若采用牺牲阳极的阴极保护法保护青铜器是利用了电解的原理 |
您最近一年使用:0次
2020-11-19更新
|
1191次组卷
|
4卷引用:黑龙江省友谊县高级中学2022-2023学年高二上学期期末考试(新教材)化学试题
名校
9 . 下列电极反应式与出现的环境相匹配的是
| 电极反应式 | 出现的环境 | |
| A | C2H5OH-12e-+3H2O=CO2↑+12H+ | 碱性环境下乙醇燃料电池的负极反应 |
| B | O2+2H2O-4e-=4OH- | 钢铁吸氧腐蚀的正极反应 |
| C | CO-2e-+CO =2CO2 =2CO2 | 熔融碳酸盐环境下的CO燃料电池负极 |
| D | 2H++2e-=H2↑ | 用惰性电极电解H2SO4溶液的阳极反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 按如图所示装置进行下列不同的操作,其中不正确的是
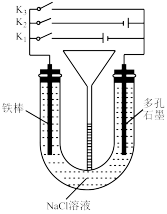

| A.先只接通K1,一段时间后,漏斗液面上升,然后再只接通K2,漏斗液面下降 |
| B.只接通K1,一段时间后,U形管中出现白色沉淀 |
| C.只接通K2,U形管左、右两端液面均下降 |
| D.铁腐蚀的速率由大到小的顺序是:只接通K1>只闭合K3>都断开>只闭合K2 |
您最近一年使用:0次
2021-08-26更新
|
713次组卷
|
6卷引用:黑龙江省哈尔滨市尚志中学2022-2023学年高三上学期期中考试化学试题



