1 . 对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:
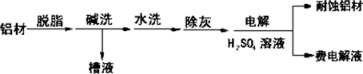
①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是___________ (用离子方程式表示)。为将碱洗后槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的_______________________ 。
A.NH3 B.CO2 C. NaOH D.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极的电极反应式为_________________________________ 。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是__________________ 。
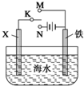
(3)利用图装置,可以模拟铁的电化学防护。若X为碳棒,为减缓铁的腐蚀,开关K应置于__ 处。若X为锌,开关K置于M处,该电化学防护法称为___________ 。
(1)以下为铝材表面处理的一种方法:

①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是
A.NH3 B.CO2 C. NaOH D.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极的电极反应式为
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是
(3)利用图装置,可以模拟铁的电化学防护。若X为碳棒,为减缓铁的腐蚀,开关K应置于

您最近一年使用:0次
2018-11-30更新
|
366次组卷
|
8卷引用:第四章 化学反应与电能(B卷·能力提升练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)
(已下线)第四章 化学反应与电能(B卷·能力提升练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)陕西省渭南市尚德中学2017-2018学年高二第一次教学质量检测化学试题江西省临川实验学校2017-2018学年高二上学期期末质量检测化学试题高二人教版选修4 第四章 第四节 金属的电化学腐蚀与防护安徽省阜阳市第三中学2018-2019学年高二下学期开学考试化学试题福建省莆田第一中学2019-2020学年高二上学期第一次月考化学试题(已下线)4.3.2 金属的防护(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)4.3.2 金属的防护(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)
2 . 化学科技工作者对含有碳杂质的金属铝的腐蚀与溶液酸碱性的关系进行了研究,在25℃时得出溶液pH值对铝的腐蚀影响关系如图所示,下列说法正确的是
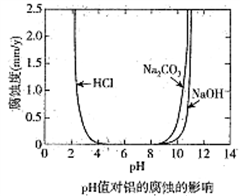

| A.金属铝在浓硫酸中的腐蚀速率大于盐酸中的腐蚀速率 |
| B.金属铝在中性环境中不易被腐蚀 |
| C.金属铝在pH=8.5的Na2CO3 溶液中会发生电化学腐蚀析出氧气 |
| D.不能用电解的方法在金属铝的表面生成致密的氧化物薄膜 |
您最近一年使用:0次
2017-12-24更新
|
461次组卷
|
5卷引用:第36练 金属的腐蚀与防护-2023年高考化学一轮复习小题多维练(全国通用)
(已下线)第36练 金属的腐蚀与防护-2023年高考化学一轮复习小题多维练(全国通用)辽宁省百校联盟2018届高三TOP20十二月联考(Ⅱ卷)理综化学试题(已下线)黄金30题系列 高二化学(选修4) 小题好拿分【提升版】2017-2018学年第一学期期末复习备考之精准复习模拟题高三化学(单科)(C卷)(已下线)课时34 金属的腐蚀与防护-2022年高考化学一轮复习小题多维练(全国通用)
2020高三·全国·专题练习
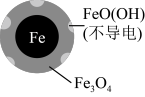
3 . 用零价铁(Fe)去除水体中的硝酸盐( )已成为环境修复研究的热点之一。
)已成为环境修复研究的热点之一。
(1)Fe还原水体中 的反应原理如图所示。
的反应原理如图所示。

①作负极的物质化学式为___________ 。
②正极的电极反应式是_____________ 。
(2)将足量铁粉投入水体中,经24小时测定 的去除率和pH,结果如下:
的去除率和pH,结果如下:
pH=4.5时, 的去除率低。其原因是
的去除率低。其原因是_________________ 。
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高 的去除率。对Fe2+的作用提出两种假设:
的去除率。对Fe2+的作用提出两种假设:
I.Fe2+直接还原 ;
;
II.Fe2+破坏FeO(OH)氧化层。
①做对比实验,结果如图所示,可得到的结论是_________ 。
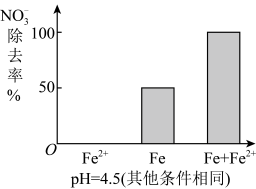
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4,该反应的离子方程式为_________ ,解释加入Fe2+提高 去除率的原因:
去除率的原因:___________ 。
 )已成为环境修复研究的热点之一。
)已成为环境修复研究的热点之一。(1)Fe还原水体中
 的反应原理如图所示。
的反应原理如图所示。
①作负极的物质化学式为
②正极的电极反应式是
(2)将足量铁粉投入水体中,经24小时测定
 的去除率和pH,结果如下:
的去除率和pH,结果如下:初始pH | pH=2.5 | pH=4.5 |
| 接近100% | <50% |
24小时pH | 接近中性 | 接近中性 |
铁的最终物质形态 |
|
|
 的去除率低。其原因是
的去除率低。其原因是(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高
 的去除率。对Fe2+的作用提出两种假设:
的去除率。对Fe2+的作用提出两种假设:I.Fe2+直接还原
 ;
;II.Fe2+破坏FeO(OH)氧化层。
①做对比实验,结果如图所示,可得到的结论是
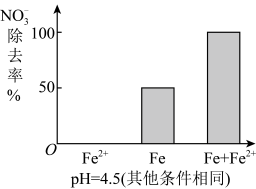
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4,该反应的离子方程式为
 去除率的原因:
去除率的原因:
您最近一年使用:0次
名校
解题方法
4 . 近年来,我国多条高压直流电线路的瓷绝缘子出现铁帽腐蚀现象,在铁帽上加锌环能有效防止铁帽的腐蚀,下列说法正确的是
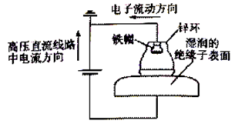

| A.阳极电极反应为Zn—2eˉ=Zn2+ |
| B.阴极电极反应为4OHˉ-4eˉ=O2↑+2H2O |
| C.该装置为牺牲阳极的阴极保护法 |
| D.绝缘子表面产生的OH- 向阴极移动 |
您最近一年使用:0次
2018-12-14更新
|
299次组卷
|
3卷引用:云南省蒙自一中2021-2022学年高二下学期3月份考试化学试题
名校
解题方法
5 . 按如图所示装置进行下列不同的操作,
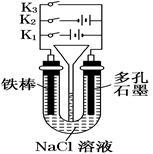
其中不正确的是

其中不正确的是
| A.铁腐蚀的速度由大到小的顺序是:只接通K1>只闭合K3>都断开>只闭合K2 |
| B.只接通K1,一段时间后,U形管中出现白色沉淀 |
| C.只接通K2,U形管左、右两端液面均下降 |
| D.先只接通K1,一段时间后,漏斗液面上升,然后再只接通K2,漏斗液面下降 |
您最近一年使用:0次
2016-12-09更新
|
595次组卷
|
5卷引用:山西省太原师范学院附属中学2022-2023学年高二上学期12月月考化学试题
名校
6 . 宝鸡被誉为“青铜器之乡”,出土了大盂鼎、毛公鼎、散氏盘等五万余件青铜器。研究青铜器(含Cu、Sn等)在潮湿环境中发生的腐蚀对于文物保护和修复有重要意义。下图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图,下列说法不正确的是
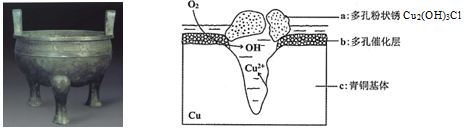

| A.青铜器发生电化学腐蚀,图中c作负极,被氧化 |
| B.正极发生的电极反应为O2+ 4e-+2H2O=4OH- |
| C.环境中的Cl-与正、负两极反应的产物作用生成a的离子方程式为2Cu2++3OH-+Cl-=Cu2 (OH)3Cl↓ |
| D.若生成0.2 mol Cu2(OH)3Cl,则理论上消耗的O2体积为4.48L |
您最近一年使用:0次
2017-01-10更新
|
586次组卷
|
5卷引用:湖南省株洲市第一中学2022-2023学年高三上学期第一次月考化学试题
名校
解题方法
7 . 锡及其化合物在生产、生活中有着重要的用途。已知:Sn的熔点为231℃;Sn2+易水解、易被氧化;SnCl4极易水解、熔点为-33℃、沸点为114℃。
2H++SnO22- Sn(OH)2
Sn(OH)2 Sn2++2OH-
Sn2++2OH-
请按要求回答下列相关问题:
(1)元素锡比同主族碳的周期数大3,锡的原子序数为_______ 。
(2)用于微电子器件生产的锡粉纯度测定:
① 取1.19g试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;
② 加入过量的Fe2(SO4)3;③ 用0.1000 mol/LK2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00 mL。
步骤② 中加入Fe2(SO4)3的作用是_______ ;此锡粉样品中锡的质量分数________ 。
(3)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如图所示:
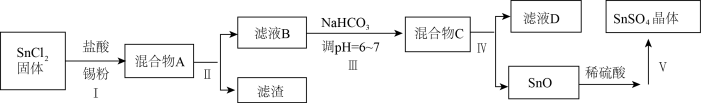
① 步骤I加入Sn粉的作用:___________ 及调节溶液pH。
② 步骤Ⅲ生成SnO的离子方程式:____________________ 。
③ 以锡单质为阳极,铁片为阴极,SnSO4溶液为电解质溶液,在铁片上镀锡,阴极反应式是____________ ,镀锡铁破损后在潮湿的环境中容易发生腐蚀的原因是_________ ,若是在较弱的酸性环境中发生腐蚀,正极反应式是____________ 。
(4)SnCl4蒸气遇水汽呈浓烟状,因而叮制作烟幕弹, 其反应的化学方程式为___________ 。
(5)锡的+2价化合物应具有较强的还原性,已知Sn2+的还原性比 Fe2+的还原性强,PbO2的氧化性比Cl2的氧化性强。试写出下列反应的化学方程式:
① 将SnCl4溶液蒸干灼烧得到的固体物质是________ ;
② 若用SnCl2溶液与过量的碱溶液反应制Sn(OH)2,该碱溶液可选用________ 。
2H++SnO22-
 Sn(OH)2
Sn(OH)2 Sn2++2OH-
Sn2++2OH-请按要求回答下列相关问题:
(1)元素锡比同主族碳的周期数大3,锡的原子序数为
(2)用于微电子器件生产的锡粉纯度测定:
① 取1.19g试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;
② 加入过量的Fe2(SO4)3;③ 用0.1000 mol/LK2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00 mL。
步骤② 中加入Fe2(SO4)3的作用是
(3)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如图所示:

① 步骤I加入Sn粉的作用:
② 步骤Ⅲ生成SnO的离子方程式:
③ 以锡单质为阳极,铁片为阴极,SnSO4溶液为电解质溶液,在铁片上镀锡,阴极反应式是
(4)SnCl4蒸气遇水汽呈浓烟状,因而叮制作烟幕弹, 其反应的化学方程式为
(5)锡的+2价化合物应具有较强的还原性,已知Sn2+的还原性比 Fe2+的还原性强,PbO2的氧化性比Cl2的氧化性强。试写出下列反应的化学方程式:
① 将SnCl4溶液蒸干灼烧得到的固体物质是
② 若用SnCl2溶液与过量的碱溶液反应制Sn(OH)2,该碱溶液可选用
您最近一年使用:0次
2017-05-15更新
|
706次组卷
|
2卷引用:山西省阳泉市第一中学校2022-2023学年高三上学期11月期中考试化学试题