名校
解题方法
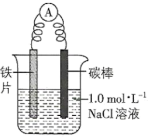
1 . 某小组同学利用原电池装置探究物质的性质。资料显示:原电池装置中,负极反应物的还原性越强,或正极反应物的氧化性越强,原电池的电压越大。
(1)同学们利用表中装置进行实验并记录。
①同学们认为实验Ⅰ中铁主要发生了析氢腐蚀,其负极反应式是___ 。
②针对实验Ⅱ现象:甲同学认为不可能发生析氢腐蚀,其判断依据是___ ;乙同学认为实验Ⅱ中应发生吸氧腐蚀,其正极的电极反应式是___ 。
(2)同学们仍用上述装置并用Cu和石墨为电极继续实验,探究实验Ⅱ指针偏转原因及影响O2氧化性因素。
①丙同学比较实验Ⅱ、Ⅲ、Ⅳ的电压表读数为:c>a>b,请解释原因是___ 。
②丁同学对Ⅳ、Ⅴ进行比较,其目的是探究___ 对O2氧化性的影响;实验Ⅳ中加入Na2SO4溶液的目的是___ 。
(1)同学们利用表中装置进行实验并记录。
| 装置 | 编号 | 电极A | 溶液B | 操作及现象 |
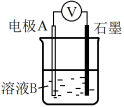 | Ⅰ | Fe | pH=2 H2SO4 | 连接装置后,石墨表面产生无色气泡;电压表指针偏转 |
| Ⅱ | Cu | pH=2 H2SO4 | 连接装置后,石墨表面无明显现象;电压表指针偏转,记录读数为a |
②针对实验Ⅱ现象:甲同学认为不可能发生析氢腐蚀,其判断依据是
(2)同学们仍用上述装置并用Cu和石墨为电极继续实验,探究实验Ⅱ指针偏转原因及影响O2氧化性因素。
| 编号 | 溶液B | 操作及现象 |
| Ⅲ | 经煮沸的pH=2的H2SO4 | 溶液表面用煤油覆盖,连接装置后,电压表指针微微偏转,记录读数为b |
| Ⅳ | pH=2的H2SO4 | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为c;取出电极,向溶液中加入数滴浓Na2SO4溶液混合后,插入电极,保持O2通入,电压表读数仍为c |
| Ⅴ | pH=12的NaOH | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为d |
②丁同学对Ⅳ、Ⅴ进行比较,其目的是探究
您最近半年使用:0次
解题方法
2 . 某化学兴趣小组设计了如下实验,探究铁的电化学腐蚀及防护原理。
(1)甲同学利用下图装置,进行铁的电化学腐蚀原理探究。
查阅资料:1.Fe2+遇K3[Fe(CN)6]溶液生成蓝色沉淀。
2.K3[Fe(CN)6]具有氧化性。
①用电极反应式解释实验ⅱ中的现象:_______ 。
②乙同学认为仅通过ⅲ中现象不能证明铁发生了电化学腐蚀,理由是_______ 。
③为验证猜想,乙同学设计了ⅳ、ⅴ、ⅵ三组对比实验,并记录如下:
a.以上实验表明:在Cl−存在条件下,K3[Fe(CN)6]溶液可以与铁片发生反应。
b.为探究Cl−的存在对反应的影响:乙同学将铁片酸洗(用稀硫酸浸泡后洗净)后再进行实验ⅵ,发现铁片表面产生蓝色沉淀。此补充实验表明 Cl−的作用是_______ 。
④结合上述两位同学的实验探究,请你改进甲同学步骤ⅲ的操作:_______ ,以证明铁发生了电化学腐蚀。
(2)丙同学向如图所示装置的容器a、b中分别加入30 mL3.5%的NaCl溶液,闭合K,电流计指针未发生偏转。加热容器a,电流计指针向右偏转。
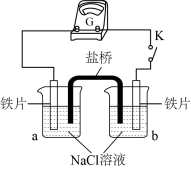
实验检测表明:容器a中的溶液产生了Fe2+,而容器b中的溶液不存在Fe2+。则:容器b中铁片做_______ 极(填:“正”或“负”)。加热后,电流计指针发生偏转的原因可能是_______ 。
(3)金属阳极钝化是一种电化学防护方法。将Fe作阳极置于H2SO4溶液中,一定条件下, Fe钝化形成致密Fe3O4氧化膜,则阳极的电极反应式为_______ 。
(1)甲同学利用下图装置,进行铁的电化学腐蚀原理探究。
| 装置 | 实验步骤及操作 | 现象 |
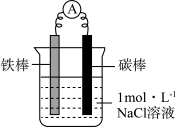 | ⅰ.连好装置,观察 | 电流表指针偏转 |
| ⅱ.一段时间后,向烧杯中滴加酚酞 | 碳棒附近溶液变红 | |
| ⅲ.一段时间后,向烧杯中滴加铁氰化钾 (K3[Fe(CN)6])溶液 | 铁片表面产生蓝色沉淀 |
2.K3[Fe(CN)6]具有氧化性。
①用电极反应式解释实验ⅱ中的现象:
②乙同学认为仅通过ⅲ中现象不能证明铁发生了电化学腐蚀,理由是
③为验证猜想,乙同学设计了ⅳ、ⅴ、ⅵ三组对比实验,并记录如下:
| 实验 | 滴管 | 试管 | 现象 |
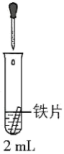
 | 0.5 mol·L−1 K3[Fe(CN)6] 溶液 | ⅳ.蒸馏水 | 无明显变化 |
| ⅴ. 1.0 mol·L−1 NaCl 溶液 | 铁片表面产生大量蓝色沉淀 | ||
| ⅵ.0.5 mol·L−1 Na2SO4溶液 | 无明显变化 |
b.为探究Cl−的存在对反应的影响:乙同学将铁片酸洗(用稀硫酸浸泡后洗净)后再进行实验ⅵ,发现铁片表面产生蓝色沉淀。此补充实验表明 Cl−的作用是
④结合上述两位同学的实验探究,请你改进甲同学步骤ⅲ的操作:
(2)丙同学向如图所示装置的容器a、b中分别加入30 mL3.5%的NaCl溶液,闭合K,电流计指针未发生偏转。加热容器a,电流计指针向右偏转。

实验检测表明:容器a中的溶液产生了Fe2+,而容器b中的溶液不存在Fe2+。则:容器b中铁片做
(3)金属阳极钝化是一种电化学防护方法。将Fe作阳极置于H2SO4溶液中,一定条件下, Fe钝化形成致密Fe3O4氧化膜,则阳极的电极反应式为
您最近半年使用:0次
2022-09-06更新
|
158次组卷
|
2卷引用:福建省宁德市部分达标中学2021-2022学年高二上学期期中联合考试化学试题
解题方法
3 . 已知铁氰化钾K3[Fe(CN)6]溶液呈黄色,可以与Fe2+反应生成带有特征蓝色的Fe3[Fe(CN)6]2(铁氰化亚铁)沉淀,因而在实验室中常用于鉴别溶液中是否存在Fe2+。
I.某化学兴趣小组查阅资料了解到[Fe(CN)6]3-具有氧化性,可被还原生成[Fe(CN)6]4-。设计了如下实验,探究[Fe(CN)6]3-的相关性质。
(1)实验一:向饱和Na2S溶液中滴加几滴0.1mol·L-1的K3[Fe(CN)6]溶液,溶液出现黄色浑浊,发生反应的离子方程式为______ 。
(2)实验二:向滴有淀粉的饱和KI溶液中滴加几滴0.1mol·L-1的K3[Fe(CN)6]溶液,可以观察到的现象为______ 。
II.小组同学提出问题:K3[Fe(CN)6]能否将Fe氧化成Fe2+?设计并实施实验:
(3)指导老师指出实验中需要用煮沸后再冷却至室温的蒸馏水配制的K3[Fe(CN)6]溶液,并且往试管中的溶液上加入少量煤油,其目的为___________ 。
(4)①根据实验现象得出结论:___________ 。
②反思现象:乙同学认为实验三和实验四现象不同的原因是铁屑表面有一层金属氧化膜,阻止了反应进行,加入NaCl的作用为______ 。
③深度探究:为证明不同现象是由Cl-而不是Na+造成的,可向实验三的试管中加入少量___________ (填化学式),观察是否出现蓝色沉淀。
(5)拓展实验:按如图所示装置及试剂组装仪器,观察到电流表指针发生偏转,Fe电极表面的电极方程式为___________ 。请设计实验方案探究该装置是否能有效防止Fe发生腐蚀:___________ 。
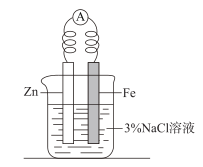
I.某化学兴趣小组查阅资料了解到[Fe(CN)6]3-具有氧化性,可被还原生成[Fe(CN)6]4-。设计了如下实验,探究[Fe(CN)6]3-的相关性质。
(1)实验一:向饱和Na2S溶液中滴加几滴0.1mol·L-1的K3[Fe(CN)6]溶液,溶液出现黄色浑浊,发生反应的离子方程式为
(2)实验二:向滴有淀粉的饱和KI溶液中滴加几滴0.1mol·L-1的K3[Fe(CN)6]溶液,可以观察到的现象为
II.小组同学提出问题:K3[Fe(CN)6]能否将Fe氧化成Fe2+?设计并实施实验:
| 序号 | 实验方案 | 实验现象 |
| 实验三 | 取少量0.1mol·L-1的K3[Fe(CN)6]溶液于试管中,加入适量铁屑 | 无明显现象 |
| 实验四 | 向实验三的试管中加入少量NaCl固体 | 溶液中出现蓝色浑浊 |
(4)①根据实验现象得出结论:
②反思现象:乙同学认为实验三和实验四现象不同的原因是铁屑表面有一层金属氧化膜,阻止了反应进行,加入NaCl的作用为
③深度探究:为证明不同现象是由Cl-而不是Na+造成的,可向实验三的试管中加入少量
(5)拓展实验:按如图所示装置及试剂组装仪器,观察到电流表指针发生偏转,Fe电极表面的电极方程式为

您最近半年使用:0次
2022-01-22更新
|
830次组卷
|
2卷引用:广东省肇庆市2021-2022学年高三第二次模拟考试化学试题
名校
4 . 某小组同学利用原电池装置探究物质的性质。资料显示:原电池装置中,负极反应物的还原性越强,或正极反应物的氧化性越强,原电池的电压越大。
(1)同学们利用下表中装置进行实验并记录。
①同学们认为实验Ⅰ中铁主要发生了析氢腐蚀,其正极反应式是_____________ 。
②针对实验Ⅱ现象:甲同学认为不可能发生析氢腐蚀,其判断依据是_______ ;乙同学认为实验Ⅱ中应发生吸氧腐蚀,其正极的电极反应式是___________ 。
(2)同学们仍用上述装置并用Cu和石墨为电极继续实验,探究实验Ⅱ指针偏转原因及影响O2氧化性因素。
①丙同学比较实验Ⅱ、Ⅲ、Ⅳ的电压表读数为:c>a>b,请解释原因是_____________ 。
②丁同学对Ⅳ、Ⅴ进行比较,其目的是探究_____________________ 对O2氧化性的影响;实验Ⅳ中加入Na2SO4溶液的目的是_____________ 。
(1)同学们利用下表中装置进行实验并记录。
| 装置 | 编号 | 电极A | 溶液B | 操作及现象 |
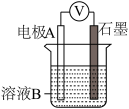 | Ⅰ | Fe | pH=2的H2SO4 | 连接装置后,石墨表面产生无色气泡;电压表指针偏转 |
| Ⅱ | Cu | pH=2的H2SO4 | 连接装置后,石墨表面无明显现象;电压表指针偏转,记录读数为a |
②针对实验Ⅱ现象:甲同学认为不可能发生析氢腐蚀,其判断依据是
(2)同学们仍用上述装置并用Cu和石墨为电极继续实验,探究实验Ⅱ指针偏转原因及影响O2氧化性因素。
| 编号 | 溶液B | 操作及现象 |
| Ⅲ | 经煮沸的pH=2的 H2SO4 | 溶液表面用煤油覆盖,连接装置后,电压表指针微微偏转,记录读数为b |
| Ⅳ | pH=2的H2SO4 | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为c;取出电极,向溶液中加入数滴浓Na2SO4溶液混合后,插入电极,保持O2通入,电压表读数仍为c |
| Ⅴ | pH=12的NaOH | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为d |
②丁同学对Ⅳ、Ⅴ进行比较,其目的是探究
您最近半年使用:0次
2019-11-21更新
|
1238次组卷
|
11卷引用:江苏省苏州市张家港高级中学2019-2020学年高二上学期期中考试化学试题
江苏省苏州市张家港高级中学2019-2020学年高二上学期期中考试化学试题安徽省太和第一中学2019-2020学年高一下学期期末考试化学试题河北省承德市隆化存瑞中学2019-2020学年高一下学期期末测试化学试题福建省厦门第一中学2020-2021学年高二10月月考化学试题(已下线)专题4.4 金属的电化学腐蚀与防护-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)4.4 金属的电化学腐蚀与防护(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)第4章 化学反应与电能(章末检测)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)第4章 电化学基础(选拔卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)(已下线)【教材实验热点】09 化学能与电能河北省石家庄市第四十二中学2022-2023高二上学期10月月考化学试题福建省莆田第六中学2022-2023学年高二上学期第二次月考(B卷)化学试题
名校
解题方法
5 . 下列劳动项目与所述的化学知识没有关联的是
| 选项 | 劳动项目 | 化学知识 |
| A | 用84消毒液对图书馆桌椅消毒 | NaClO具有氧化性 |
| B | 用热的纯碱溶液去除衣物上的油污 |  溶液显碱性 溶液显碱性 |
| C | 用安装锌块的方法减缓船体腐蚀 | Zn的还原性比Fe强 |
| D | 用 除去污水中少量的 除去污水中少量的 |  具有还原性 具有还原性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
6 . 某实验小组金属的电化学腐蚀实验探究
(1)完成下列问题。
①请解释铜丝区域溶液变红的原因是_______ (电极反应式及文字说明)。
②写出生成蓝色沉淀的离子方程式_______ 。
(2)完成下列问题。
根据实验二的现象,推测 可能具有
可能具有_______ “填氧化性或还原性”。
(3)依据实验二的现象,甲同学认为实验一不一定能说明 发生了电化学腐蚀,设计如下实验证明其结论。
发生了电化学腐蚀,设计如下实验证明其结论。
根据实验现象推出实验三的结论是:在 溶液中情况下,
溶液中情况下,_______ 。
(4)结合实验一~实验三,乙同学设计如下装置进行实验四,证明金属可以发生电化学腐蚀,当电极X为 时,实验四的两个实验方案均可以证明
时,实验四的两个实验方案均可以证明 发生电化学腐蚀
发生电化学腐蚀
①补全实验方案2中的空格部分
②思考:若电极X为 时,电流表读数为
时,电流表读数为 ,推测电极X为
,推测电极X为 时电流表读数的范围是
时电流表读数的范围是_____ 。
(1)完成下列问题。
| 实验序号 | 实验装置 | 实验方案 | 实验现象 |
| 实验一 |  | 1.将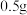 琼脂加入 琼脂加入 烧杯中,再加入 烧杯中,再加入 饱和食盐水和 饱和食盐水和 水。搅拌、加热煮沸,使琼脂溶解,转入培养皿中。滴入5~6滴酚酞溶液和 水。搅拌、加热煮沸,使琼脂溶解,转入培养皿中。滴入5~6滴酚酞溶液和 溶液 溶液 | |
| 2.将一个铁钉用砂纸打磨光滑,一端缠有铜丝,放入培养皿中一段时间。 | 铜丝的区域溶液变红色;铁钉区域出现蓝色沉淀 |
②写出生成蓝色沉淀的离子方程式
(2)完成下列问题。
| 实验序号 | 实验方案 | 实验现象 |
| 实验二 | 取 饱和 饱和 溶液于试管中,滴加几滴淀粉,振荡。继续滴加5~6滴 溶液于试管中,滴加几滴淀粉,振荡。继续滴加5~6滴 溶液,振荡。 溶液,振荡。 | 滴入 溶液后,溶液变蓝色。 溶液后,溶液变蓝色。 |
 可能具有
可能具有(3)依据实验二的现象,甲同学认为实验一不一定能说明
 发生了电化学腐蚀,设计如下实验证明其结论。
发生了电化学腐蚀,设计如下实验证明其结论。| 实验序号 | 实验装置 | 实验方案 | 实验现象 |
| 实验三 | 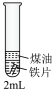 | 1.取 煮沸过的的 煮沸过的的 溶液于试管中,向试管中加入一小段铁片,再加入 溶液于试管中,向试管中加入一小段铁片,再加入 煤油液封。 煤油液封。 | 溶液无明显变化 |
2.继续向试管中加入少许 固体。 固体。 | 一段时间后,铁片表面产生大量的蓝色沉淀 |
 溶液中情况下,
溶液中情况下,(4)结合实验一~实验三,乙同学设计如下装置进行实验四,证明金属可以发生电化学腐蚀,当电极X为
 时,实验四的两个实验方案均可以证明
时,实验四的两个实验方案均可以证明 发生电化学腐蚀
发生电化学腐蚀①补全实验方案2中的空格部分
| 实验序号 | 实验装置 | 实验方案 | 实验现象 |
| 实验四 | 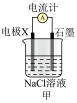 | 1.按图连接好装置,准确读取电流表读数。 | 电流表指针偏转,读数为I |
| 2.取 | 产生蓝色沉淀。 |
 时,电流表读数为
时,电流表读数为 ,推测电极X为
,推测电极X为 时电流表读数的范围是
时电流表读数的范围是
您最近半年使用:0次
2023-03-04更新
|
1037次组卷
|
4卷引用:广东省汕头市2023届高三一模化学试题
7 . 某小组同学利用下图所示装置进行铁的电化学腐蚀原理的探究实验:
(1)小组同学认为以上两种检验方法,均能证明铁发生了吸氧腐蚀。
①实验i中的现象是________ 。
②用电极反应式解释实验i中的现象________ 。
(2)查阅资料: 具有氧化性。
具有氧化性。
①据此有同学认为仅通过ii中现象不能证明铁发生了电化学腐蚀,理由是________ 。
②进行下列实验,在实验几分钟后的记录如下:
以上实验表明:在有________ 存在条件下, 溶液可以与铁片发生反应。为进一步证明该影响,小组同学将铁片酸洗(用稀硫酸浸泡后洗净)后再进行实验iii,发现铁片表面产生蓝色沉淀。此补充实验表明
溶液可以与铁片发生反应。为进一步证明该影响,小组同学将铁片酸洗(用稀硫酸浸泡后洗净)后再进行实验iii,发现铁片表面产生蓝色沉淀。此补充实验表明 的作用是
的作用是________ 。
(3)有同学认为上述实验仍不够严谨。为进一步探究 的氧化性对实验ii结果的影响,又利用(2)中装置继续实验。其中能证实以上影响确实存在的是
的氧化性对实验ii结果的影响,又利用(2)中装置继续实验。其中能证实以上影响确实存在的是________ (填字母序号)。
(4)综合以上实验分析,利用实验ii中试剂能证实铁发生了电化学腐蚀的实验方案是:连好装置一段时间后,________ (相关操作、现象),则说明负极附近溶液中产生了 ,即发生了电化学腐蚀。
,即发生了电化学腐蚀。
装置 | 分别进行的操作 | 现象 |
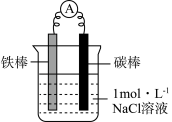 | i.连好装置一段时间后,向烧杯中滴加酚酞 | |
ii.连好装置一段时间后,向烧杯中滴加 溶液 溶液 | 铁片表面产生蓝色沉淀 |
①实验i中的现象是
②用电极反应式解释实验i中的现象
(2)查阅资料:
 具有氧化性。
具有氧化性。①据此有同学认为仅通过ii中现象不能证明铁发生了电化学腐蚀,理由是
②进行下列实验,在实验几分钟后的记录如下:
实验 | 滴管 | 试管 | 现象 |
|
| iii.蒸馏水 | 无明显变化 |
iv.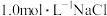 溶液 溶液 | 铁片表面产生大量蓝色沉淀 | ||
v.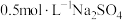 溶液 溶液 | 无明显变化 |
 溶液可以与铁片发生反应。为进一步证明该影响,小组同学将铁片酸洗(用稀硫酸浸泡后洗净)后再进行实验iii,发现铁片表面产生蓝色沉淀。此补充实验表明
溶液可以与铁片发生反应。为进一步证明该影响,小组同学将铁片酸洗(用稀硫酸浸泡后洗净)后再进行实验iii,发现铁片表面产生蓝色沉淀。此补充实验表明 的作用是
的作用是(3)有同学认为上述实验仍不够严谨。为进一步探究
 的氧化性对实验ii结果的影响,又利用(2)中装置继续实验。其中能证实以上影响确实存在的是
的氧化性对实验ii结果的影响,又利用(2)中装置继续实验。其中能证实以上影响确实存在的是实验 | 试剂 | 现象 |
A | 酸洗后的铁片、 溶液(已除 溶液(已除 ) ) | 产生蓝色沉淀 |
B | 酸洗后的铁片、 和NaCl混合溶液(未除 和NaCl混合溶液(未除 ) ) | 产生蓝色沉淀 |
C | 铁片、 和NaCl混合溶液(已除 和NaCl混合溶液(已除 ) ) | 产生蓝色沉淀 |
D | 铁片、 和盐酸混合溶液(已除 和盐酸混合溶液(已除 ) ) | 产生蓝色沉淀 |
 ,即发生了电化学腐蚀。
,即发生了电化学腐蚀。
您最近半年使用:0次
名校
8 . 下列说法中正确的有几项
①钠在空气中燃烧生成淡黄色的Na2O2
②配制480mL0.5mol/L的NaOH溶液,需要用托盘天平称量氢氧化钠固体9.6g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeCl2、H2SiO3都不直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的氨水等体积混合后,所得溶液中溶质的质量分数大于15%
⑦干燥的Cl2和氯水均能使鲜花褪色
⑧中和热测定实验中需要用到的玻璃仪器只有烧杯、温度计和环形玻璃搅拌棒三种
⑨纯银器在空气中久置变黑是因为发生了化学腐蚀
①钠在空气中燃烧生成淡黄色的Na2O2
②配制480mL0.5mol/L的NaOH溶液,需要用托盘天平称量氢氧化钠固体9.6g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeCl2、H2SiO3都不直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的氨水等体积混合后,所得溶液中溶质的质量分数大于15%
⑦干燥的Cl2和氯水均能使鲜花褪色
⑧中和热测定实验中需要用到的玻璃仪器只有烧杯、温度计和环形玻璃搅拌棒三种
⑨纯银器在空气中久置变黑是因为发生了化学腐蚀
| A.3项 | B.4项 | C.5项 | D.6项 |
您最近半年使用:0次
2016-12-09更新
|
762次组卷
|
4卷引用:2016届河北省衡水中学高三上学期四调考试化学试卷
9 . 金属腐蚀现象遍及国民经济和国防建设各个领域,危害十分严重。近几十年来,金属的腐蚀与防腐已成为一门独立的综合性边缘学科。某实验小组利用如图所示装置进行铁的电化学腐蚀原理及防护的探究实验:
(1)已知,Fe2+遇K3[Fe(CN)6]溶液生成蓝色沉淀。
小组同学认为以下两种检验方法,均能证明铁发生了吸氧腐蚀。
①用电极反应式解释实验i中的现象:___________ 。
②查阅资料:K3[Fe(CN)6]具有氧化性。有同学认为仅通过ii中现象不能证明铁发生了电化学腐蚀,理由是___________ 。
③为进一步探究K3[Fe(CN)6]的氧化性对实验ii结果的影响,进行下列实验,几分钟后的记录如下:
a. 以上实验表明:在Cl-存在条件下,K3[Fe(CN)6]溶液可以与铁片发生反应。
b. 为探究Cl-的存在对反应的影响,小组同学将铁片酸洗(用稀硫酸浸泡后洗净)后再进行实验iii,发现铁片表面产生蓝色沉淀。此补充实验表明Cl-的作用是___________ 。
(2)实验二:乙小组同学向如图所示装置的容器a、b中分别加入30 mL3.5%的NaCl溶液,闭合K,电流计指针未发生偏转。加热容器a,电流计指针向右偏转。
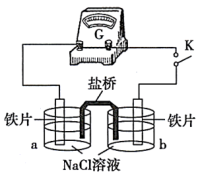
①分别取少量容器a、b中的溶液于试管中,滴加K3[Fe(CN)6]溶液,容器a中的溶液所在的试管中出现蓝色沉淀,容器b中的溶液所在的试管中无变化,容器b中铁片做___________ 极。
②加热后,电流计指针发生偏转的原因可能是___________ 。
(3)金属阳极钝化是一种电化学防护方法。将Fe作阳极置于H2SO4溶液中,一定条件下,Fe钝化形成致密Fe3O4氧化膜,试写出该阳极的电极反应式___________ 。
(1)已知,Fe2+遇K3[Fe(CN)6]溶液生成蓝色沉淀。
小组同学认为以下两种检验方法,均能证明铁发生了吸氧腐蚀。
| 装置 | 分别进行的操作 | 现象 |
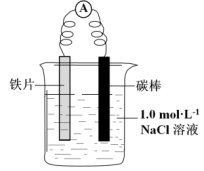 | i.连好装置一段时间后,向烧杯中滴加酚酞 | 碳棒附近溶液变红 |
| ii.连好装置一段时间后,向烧杯中滴加K3[Fe(CN)6]溶液 | 铁片表面产生蓝色沉淀 |
②查阅资料:K3[Fe(CN)6]具有氧化性。有同学认为仅通过ii中现象不能证明铁发生了电化学腐蚀,理由是
③为进一步探究K3[Fe(CN)6]的氧化性对实验ii结果的影响,进行下列实验,几分钟后的记录如下:
| 实验 | 胶头滴管 | 试管 | 现象 |
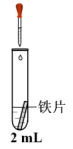 | 0.5 mol/L K3[Fe(CN)6]溶液 | iii.蒸馏水 | 无明显变化 |
iv. 溶液 溶液 | 铁片表面产生大量蓝色沉淀 | ||
v. 溶液 溶液 | 无明显变化 |
b. 为探究Cl-的存在对反应的影响,小组同学将铁片酸洗(用稀硫酸浸泡后洗净)后再进行实验iii,发现铁片表面产生蓝色沉淀。此补充实验表明Cl-的作用是
(2)实验二:乙小组同学向如图所示装置的容器a、b中分别加入30 mL3.5%的NaCl溶液,闭合K,电流计指针未发生偏转。加热容器a,电流计指针向右偏转。

①分别取少量容器a、b中的溶液于试管中,滴加K3[Fe(CN)6]溶液,容器a中的溶液所在的试管中出现蓝色沉淀,容器b中的溶液所在的试管中无变化,容器b中铁片做
②加热后,电流计指针发生偏转的原因可能是
(3)金属阳极钝化是一种电化学防护方法。将Fe作阳极置于H2SO4溶液中,一定条件下,Fe钝化形成致密Fe3O4氧化膜,试写出该阳极的电极反应式
您最近半年使用:0次
2021-10-11更新
|
308次组卷
|
2卷引用:山东省2021-2022学年高二10月“山东学情”联考化学试题(B)
10 . 某小组同学利用如图所示装置进行铁的电化学腐蚀原理的探究实验:
(1)小组同学认为以上两种检验方法,均能证明铁发生了吸氧腐蚀。
①实验i中的现象是________ 。
②用电极反应式解释实验i中的现象:________ 。
(2)查阅资料: 具有氧化性。
具有氧化性。
①据此有同学认为仅通过ii中现象不能证明铁发生了电化学腐蚀,理由是________ 。
②进行下列实验,几分钟后的记录如下:
a.以上实验表明:在________ 条件下, 溶液可以与铁片发生反应。
溶液可以与铁片发生反应。
b.为探究 的存在对反应的影响,小组同学将铁片酸洗(用稀硫酸浸泡后洗净)后再进行实验iii,发现铁片表面产生蓝色沉淀。此补充实验表明
的存在对反应的影响,小组同学将铁片酸洗(用稀硫酸浸泡后洗净)后再进行实验iii,发现铁片表面产生蓝色沉淀。此补充实验表明 的作用是
的作用是________ 。
装置 | 分别进行的操作 | 现象 |
| i.连好装置一段时间后,向烧杯中滴加酚酞 | |
ii.连好装置一段时间后,向烧杯中滴加 溶液 溶液 | 铁片表面产生蓝色沉淀 |
①实验i中的现象是
②用电极反应式解释实验i中的现象:
(2)查阅资料:
 具有氧化性。
具有氧化性。①据此有同学认为仅通过ii中现象不能证明铁发生了电化学腐蚀,理由是
②进行下列实验,几分钟后的记录如下:
实验 | 滴管 | 试管 | 现象 |
| 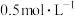  溶液 溶液 | iii.蒸馏水 | 无明显变化 |
iv.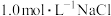 溶液 溶液 | 铁片表面产生大量蓝色沉淀 | ||
v. 溶液 溶液 | 无明显变化 |
 溶液可以与铁片发生反应。
溶液可以与铁片发生反应。b.为探究
 的存在对反应的影响,小组同学将铁片酸洗(用稀硫酸浸泡后洗净)后再进行实验iii,发现铁片表面产生蓝色沉淀。此补充实验表明
的存在对反应的影响,小组同学将铁片酸洗(用稀硫酸浸泡后洗净)后再进行实验iii,发现铁片表面产生蓝色沉淀。此补充实验表明 的作用是
的作用是
您最近半年使用:0次

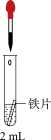
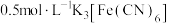 溶液
溶液