名校
1 . 化学是以实验为基础的科学。用下列装置进行实验(夹持装置略)不能达到目的的是
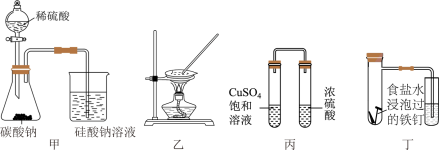

| A.用甲装置证明非金属性:S>C>Si | B.图②装置可由FeCl3•6H2O制取无水FeCl3固体 |
| C.用丙装置验证浓硫酸的吸水性 | D.用丁可模拟钢铁的吸氧腐蚀 |
您最近一年使用:0次
名校
解题方法
2 . 某小相同学为探究电极对金属腐蚀与防护的影响,设计如下实验:将饱和食盐水与琼脂(凝固剂,不参与反应)的混合液置于两个培养皿中,向其中滴入少量酚酞溶液和 溶液,混合均匀,分别将包裹锌片和铜片的铁钉放入两个培养皿中,观察现象如表。已知:
溶液,混合均匀,分别将包裹锌片和铜片的铁钉放入两个培养皿中,观察现象如表。已知: 遇到
遇到 能产生蓝色沉淀,对有关实验现象及分析不正确的是
能产生蓝色沉淀,对有关实验现象及分析不正确的是
 溶液,混合均匀,分别将包裹锌片和铜片的铁钉放入两个培养皿中,观察现象如表。已知:
溶液,混合均匀,分别将包裹锌片和铜片的铁钉放入两个培养皿中,观察现象如表。已知: 遇到
遇到 能产生蓝色沉淀,对有关实验现象及分析不正确的是
能产生蓝色沉淀,对有关实验现象及分析不正确的是变红变蓝 | 变红 |
| ⅰ.包裹铜片的铁钉 | ⅱ.包裹锌片的铁钉 |
| A.两个培养皿中金属均发生吸氧腐蚀,且铁钉腐蚀速度ⅰ快 |
| B.该实验证明,若给金属表面镀活泼性比被保护金属强的金属,则破损后依旧可以防护 |
| C.培养皿ⅱ中对铁钉的防护是牺牲阳极的阴极保护法 |
| D.随着反应的进行,培养皿ⅰ和ⅱ中均出现红褐色浑浊 |
您最近一年使用:0次
2023-11-16更新
|
397次组卷
|
2卷引用:福建省龙岩第一中学2023-2024学年高二上学期第三次月考化学试题
3 . 下列事实中,能用勒夏特列原理解释的是
| A.用牺牲阳极的阴极保护法保护船舶的外壳 |
| B.压缩氢气与碘蒸气的平衡混合体系,气体颜色变深 |
| C.夏天打开冰镇啤酒,把啤酒倒入玻璃杯中,杯中立即泛起大量泡沫 |
D.500℃左右比常温下更有利于 和 和 反应生成 反应生成 |
您最近一年使用:0次
2023-11-13更新
|
155次组卷
|
2卷引用:福建省泉州市2023-2024学年高二上学期期中考试化学试题
名校
解题方法
4 . 下列叙述中正确的是
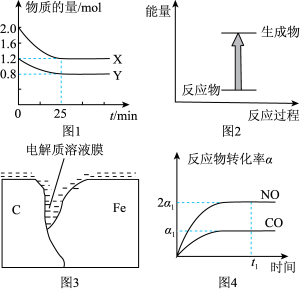

A.图 表示 表示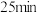 内,用 内,用 表示的平均反应速率为 表示的平均反应速率为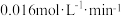 |
B.图 可表示碳与二氧化碳反应的键能变化 可表示碳与二氧化碳反应的键能变化 |
C.图 表示在钢铁内部电流由碳一侧流向铁一侧 表示在钢铁内部电流由碳一侧流向铁一侧 |
D.图 表示反应 表示反应 中 中 和 和 转化率为 转化率为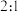 时,反应达平衡状态 时,反应达平衡状态 |
您最近一年使用:0次
名校
5 . 下列说法正确的是
| A.在电镀中,镀层金属作阳极,待镀金属作阴极 |
| B.已知C(石墨,s)=C(金刚石,s) ∆H=+1.9kJ·mol-1,则金刚石比石墨稳定 |
| C.水库的钢闸门与电源负极相连以防止其生锈,此为牺牲阳极的阴极保护法 |
| D.增大浓度能增大单位体积内活化分子的百分数,从而增大反应速率 |
您最近一年使用:0次
名校
解题方法
6 . 用如图所示装置及试剂进行铁的电化学腐蚀实验探究,测定具支锥形瓶中压强随时间变化关系以及溶解氧随时间变化关系的曲线如下。下列说法正确的是
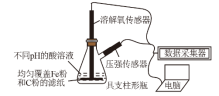



| A.pH=6.0时,正极电极反应式为:O2+2H2O+4e-=4OH– |
| B.整个过程中,负极电极反应式均为:Fe–3e-=Fe3+ |
| C.pH=4.0时,同时发生析氢腐蚀和吸氧腐蚀 |
| D.将铁换成铜进行实验,pH=2.0时,压强随时间变化的曲线走势与铁基本相同 |
您最近一年使用:0次
2023-11-11更新
|
248次组卷
|
3卷引用:福建省福州市八县一中2023-2024学年高二上学期11月期中化学试题
7 . NA代表阿伏加德罗常数的值。下列说法正确的是
| A.在氢氧燃料电池中,负极有11.2L(标准状况)气体参与反应时,转移的电子数为2NA |
| B.在氯碱工业中,制备80g烧碱时,阴极生成气体的分子数为NA |
| C.在钢铁吸氧腐蚀中,若有1mol Fe被腐蚀,被还原的O2分子数最多为0.5NA |
| D.甲烷燃烧热ΔH=-890kJ·mol-1,当0.5mol甲烷完全燃烧放出445kJ热量时,生成H2O(g)为NA |
您最近一年使用:0次
2023-11-11更新
|
149次组卷
|
2卷引用:福建省福州市八县一中2023-2024学年高二上学期11月期中化学试题
名校
8 . 化学中基本概念多,化学反应类型复杂,下列正确的叙述有
① 、
、 、
、 均为酸性氧化物
均为酸性氧化物
②盐一定由金属元素和非金属元素组成
③需要通电才可进行的有:电离、电解、电泳、电镀、电化腐蚀
④氯化铁溶液与氢氧化铁胶体具有的共同性质是:能透过滤纸,蒸干、灼烧后都有氧化铁生成
①
 、
、 、
、 均为酸性氧化物
均为酸性氧化物②盐一定由金属元素和非金属元素组成
③需要通电才可进行的有:电离、电解、电泳、电镀、电化腐蚀
④氯化铁溶液与氢氧化铁胶体具有的共同性质是:能透过滤纸,蒸干、灼烧后都有氧化铁生成
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
名校
解题方法
9 . 关于下列各装置图的叙述中正确的是
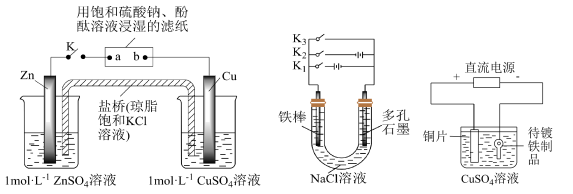

| A.装置①中K闭合时,片刻后可观察到滤纸a点变红色 |
B.装置①中K闭合时,片刻后 溶液中 溶液中 增大 增大 |
C.装置②中铁腐蚀的速率由大到小的顺序是:只闭合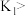 只闭合 只闭合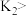 只闭合 只闭合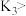 开关都断开 开关都断开 |
D.装置③中当铁制品上析出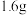 铜时,电源负极输出的电子数为 铜时,电源负极输出的电子数为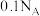 ( ( 为阿伏加德罗常数的值) 为阿伏加德罗常数的值) |
您最近一年使用:0次
2023-11-08更新
|
519次组卷
|
4卷引用:福建省泉州市永春第一中学2023-2024学年高二下学期开学化学试题
10 . 如图所示各容器中盛有海水,铁在其中被腐蚀由快到慢的顺序是
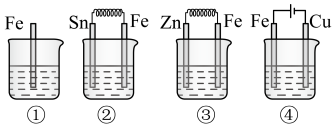
| A.④>②>①>③ | B.②>①>③>④ | C.③>②>④>① | D.④>②>③>① |
您最近一年使用:0次
2023-11-01更新
|
98次组卷
|
2卷引用:福建省福州第二中学2023-2024学年高二上学期10月月考化学试卷题



