名校
解题方法
1 . 某学生欲制作一个原电池,电池反应的离子方程式为 ,下列组合可实现的是
,下列组合可实现的是
 ,下列组合可实现的是
,下列组合可实现的是选项 | A |
| C |
|
正极材料 |
|
|
|
|
负极材料 |
|
|
|
|
电解质溶液 |
|
|
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 依据氧化还原反应 设计的原电池如图所示。
设计的原电池如图所示。
(1)电极X的材料是___________ ,电解质溶液Y是___________ 。
(2)银电极的电极反应式是___________ ;X电极的电极反应式是___________ 。
(3)外电路中的电子是从___________ 极流向___________ 极。
 设计的原电池如图所示。
设计的原电池如图所示。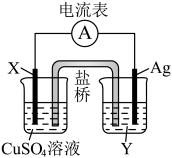
(1)电极X的材料是
(2)银电极的电极反应式是
(3)外电路中的电子是从
您最近一年使用:0次
解题方法
3 . 锌溴液流电池是液流电池的一种,能够大容量、长时间的充放电。放电时总反应为Zn+Br2= ZnBr2。下列说法正确的是
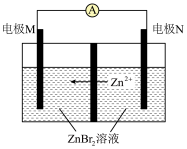
| A.放电时电极M为负极 |
| B.放电时负极的电极反应式为Zn-2e-=Zn2+ |
| C.充电时ZnBr2溶液的浓度增大 |
| D.电池中间使用阳离子交换膜或阴离子交换膜都可以 |
您最近一年使用:0次
名校
4 . 化学电源与我们的生活密切相关,回答下列问题:
(1)在铜锌原电池中,以硫酸为电解质溶液,铜电极反应式为_______ 。
(2)若将电解质溶液换成硫酸铜,如图所示,则铜为_______ 极,电极上发生的是_______ (填“氧化”或“还原”)反应,铜电极反应式是_______ ;向锌电极移动的离子为_______ 。随着实验地进行,溶液质量_______ (填增加、减小或不变),若溶液质量变化2g,则转移的电子数为_______ (NA表示阿伏伽德罗的数值)。
(1)在铜锌原电池中,以硫酸为电解质溶液,铜电极反应式为
(2)若将电解质溶液换成硫酸铜,如图所示,则铜为

您最近一年使用:0次
名校
解题方法
5 . 有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
由此可判断这四种金属的活动性顺序是
实验装置 |
装置一 |
装置二 |
| 部分实验现象 | a极质量减小,b极质量增大 | b极有气体产生,c极无变化 |
实验装置 |
装置三 |
装置四 |
| 部分实验现象 | d极溶解,c极有气体产生 | 电子从d极流向a极 |
| A.a>b>c>d | B.b>c>d>a | C.d>a>b>c | D.a>b>d>c |
您最近一年使用:0次
2024-04-24更新
|
450次组卷
|
2卷引用:广东省江门市第一中学2023-2024学年高一下学期第一次段考化学试题
2024高三下·全国·专题练习
解题方法
6 . (氮是空气中含量最多的元素,在自然界中的存在十分广泛,实验小组对不同含氮物质做了相关研究。
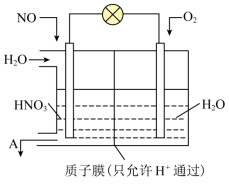
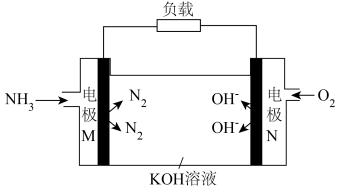
(1)利用电化学原理脱硝可同时获得电能,其工作原理如图所示。则负极发生的电极反应式为___________ ,当外电路中有2mol电子通过时,理论上通过质子膜的微粒的物质的量为___________ 。
(1)利用电化学原理脱硝可同时获得电能,其工作原理如图所示。则负极发生的电极反应式为
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
7 . 利用 催化加氢制二甲醚,可以实现
催化加氢制二甲醚,可以实现 的再利用,涉及以下主要反应:
的再利用,涉及以下主要反应:
I.

Ⅱ.

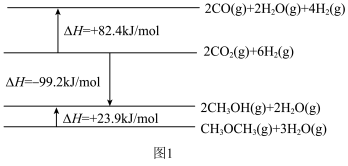
相关物质及能量变化的示意图如图1所示。
(1)如图所示是绿色电源“二甲醚( )燃料电池”的工作原理示意图(a、b均为多孔性
)燃料电池”的工作原理示意图(a、b均为多孔性 电极)。负极是
电极)。负极是___________ (填写“a”或“b”),该电极的电极反应式是___________ ,若有 氢离子通过质子交换膜,则b电极在标准状况下吸收
氢离子通过质子交换膜,则b电极在标准状况下吸收___________  氧气。
氧气。
 催化加氢制二甲醚,可以实现
催化加氢制二甲醚,可以实现 的再利用,涉及以下主要反应:
的再利用,涉及以下主要反应:I.


Ⅱ.


相关物质及能量变化的示意图如图1所示。
(1)如图所示是绿色电源“二甲醚(
 )燃料电池”的工作原理示意图(a、b均为多孔性
)燃料电池”的工作原理示意图(a、b均为多孔性 电极)。负极是
电极)。负极是 氢离子通过质子交换膜,则b电极在标准状况下吸收
氢离子通过质子交换膜,则b电极在标准状况下吸收 氧气。
氧气。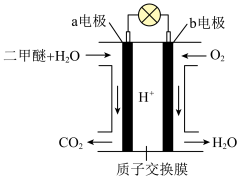
您最近一年使用:0次
名校
解题方法
8 . 研究化学能与热能、电能的转化具有重要价值。回答下列问题:
(1)下列化学反应过程中的能量变化符合图示的是_________ (填序号)。
①酸碱中和反应②碳酸钙分解③金属钠与水反应④酒精燃烧⑤灼热的碳与二氧化碳反应⑥ 与
与 反应
反应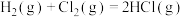 的反应过程如图所示:
的反应过程如图所示: 和
和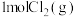 充分反应,则反应物中旧键断裂共吸收
充分反应,则反应物中旧键断裂共吸收_________  能量,生成物中新键形成共放出
能量,生成物中新键形成共放出_________  能量,该反应为
能量,该反应为_________ (填“吸热”或“放热”)反应。
(3)若利用反应 设计一个原电池,请在如图内完善实验装置
设计一个原电池,请在如图内完善实验装置__________ 。_____________ 。
(1)下列化学反应过程中的能量变化符合图示的是
①酸碱中和反应②碳酸钙分解③金属钠与水反应④酒精燃烧⑤灼热的碳与二氧化碳反应⑥
 与
与 反应
反应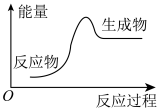
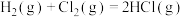 的反应过程如图所示:
的反应过程如图所示: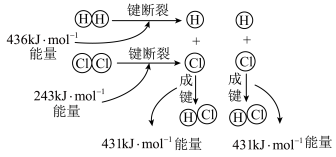
 和
和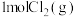 充分反应,则反应物中旧键断裂共吸收
充分反应,则反应物中旧键断裂共吸收 能量,生成物中新键形成共放出
能量,生成物中新键形成共放出 能量,该反应为
能量,该反应为(3)若利用反应
 设计一个原电池,请在如图内完善实验装置
设计一个原电池,请在如图内完善实验装置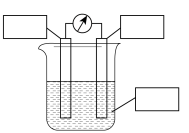
您最近一年使用:0次
名校
解题方法
9 . 回答下列问题:
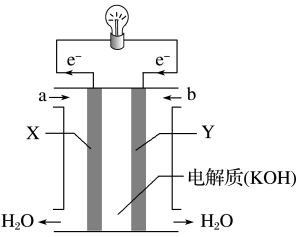
(1)如图为氢氧燃料电池的构造示意图,根据电子运动方向,可知氧气从___________ 口通入(填“a”或“b”),X极为电池的___________ (填“正”或“负”)极,Y极的电极方程式为___________ 。
A极:2H2+2O2--4e-=2H2O
B极:O2+4e-=2O2-
则A极是电池的___________ 极;电子从该极___________ (填“流入”或“流出”)。
(3)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为:
Zn+2OH-2e-=ZnO+H2O Ag2O+H2O+2e-=2Ag+2OH-
总反应为Ag2O+Zn=ZnO+2Ag
①Zn是___________ 极,Ag2O发生___________ 反应。
②电子由___________ 极流向___________ 极(填“Zn”或“Ag2O”),当电路通过1 mol电子时,负极消耗物质的质量是___________ g。
③在使用过程中,电解质溶液中KOH的物质的量___________ (填“增大”“减小”或“不变”)。
(1)如图为氢氧燃料电池的构造示意图,根据电子运动方向,可知氧气从
A极:2H2+2O2--4e-=2H2O
B极:O2+4e-=2O2-
则A极是电池的
(3)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为:
Zn+2OH-2e-=ZnO+H2O Ag2O+H2O+2e-=2Ag+2OH-
总反应为Ag2O+Zn=ZnO+2Ag
①Zn是
②电子由
③在使用过程中,电解质溶液中KOH的物质的量
您最近一年使用:0次
解题方法
10 . 铝—空气燃料电池是一种新型高能量电池,具有能量密度大、无污染、可靠性高等优点。图1是一种盐水铝空气电池装置原理图,图2是石墨空气电极结构示意图。下列说法正确的是
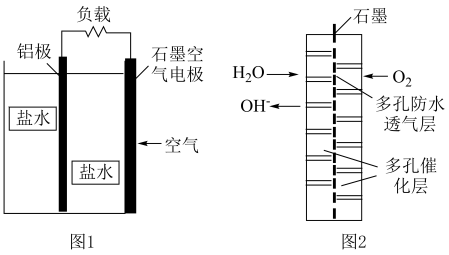

| A.铝极为负极,发生还原反应 |
B.工作一段时间后,含铝微粒的存在形式为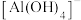 |
C.石墨空气电极的电极反应式: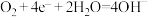 |
D.在石墨空气电极中, 会穿过多孔防水透气层进入电极右侧 会穿过多孔防水透气层进入电极右侧 |
您最近一年使用:0次