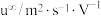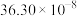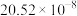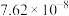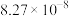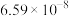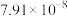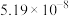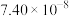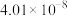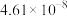1 . 微生物脱盐池的a极上加入了呼吸细菌,工作时可将工业废水中的有机污染物转化为 ,其工作原理如图所示。下列说法正确的是
,其工作原理如图所示。下列说法正确的是
 ,其工作原理如图所示。下列说法正确的是
,其工作原理如图所示。下列说法正确的是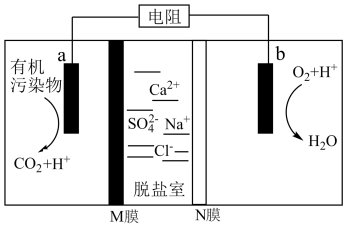
A.工作时, 极发生还原反应,电子从 极发生还原反应,电子从 极流向 极流向 极 极 |
B. 膜为阴离子交换膜,脱盐室最终可得到淡盐水 膜为阴离子交换膜,脱盐室最终可得到淡盐水 |
C. 极上消耗 极上消耗 气体,则通过 气体,则通过 膜的离子的物质的量为 膜的离子的物质的量为 |
D.若有机物的分子式为 ,则 ,则 极的电极反应式为 极的电极反应式为 |
您最近一年使用:0次
2 . 学校化学兴趣小组模拟铝的电化学腐蚀实验从而探究铝制品表面出现白斑的原因,装置如图所示,下列说法错误的是
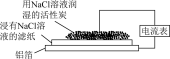
| A.铝在发生腐蚀的过程中将化学能转变成电能和热能 |
| B.电流从铝箔通过电流表流向活性炭 |
| C.活性炭粉的存在加速了铝箔的腐蚀 |
D.该反应总反应为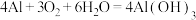 ,生成的进一步脱水形成白斑 ,生成的进一步脱水形成白斑 |
您最近一年使用:0次
解题方法
3 . 我国科学家最近发明了一种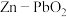 电池,电解质为
电池,电解质为 、
、 和
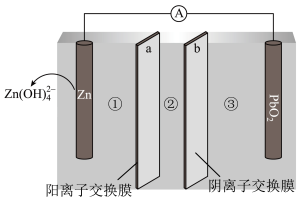
和 ,由a和b两种离子交换膜隔开,形成①、②、③三个电解质溶液区域,结构示意图如图所示。下列说法正确的是
,由a和b两种离子交换膜隔开,形成①、②、③三个电解质溶液区域,结构示意图如图所示。下列说法正确的是
 电池,电解质为
电池,电解质为 、
、 和
和 ,由a和b两种离子交换膜隔开,形成①、②、③三个电解质溶液区域,结构示意图如图所示。下列说法正确的是
,由a和b两种离子交换膜隔开,形成①、②、③三个电解质溶液区域,结构示意图如图所示。下列说法正确的是
A.Zn极的电极反应式: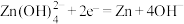 |
| B.消耗6.5gZn,理论上③区溶液质量减少16g |
C.②区域的电解质溶液为 溶液 溶液 |
D.电子从Zn极经导线流向 极,然后经过电解质溶液流回Zn极 极,然后经过电解质溶液流回Zn极 |
您最近一年使用:0次
4 .  是实验室常用试剂.回答下列问题:
是实验室常用试剂.回答下列问题:
(1)实验室配制一定浓度的 溶液(橙红色)并标定的实验步骤如下:
溶液(橙红色)并标定的实验步骤如下:
步骤Ⅰ.称取约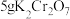 于烧杯中,加入少量蒸馏水溶解,配制成
于烧杯中,加入少量蒸馏水溶解,配制成 溶液;
溶液;
步骤Ⅱ.移取 已配制的
已配制的 溶液于碘量瓶中,加入
溶液于碘量瓶中,加入 过量
过量 ,再加
,再加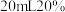 的硫酸,摇匀(
的硫酸,摇匀( 还原为亮绿色的
还原为亮绿色的 ),在暗处放置
),在暗处放置 ,加水稀释,用
,加水稀释,用 的
的 标准溶液滴定
标准溶液滴定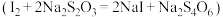 ,接近终点时,加入
,接近终点时,加入 淀粉溶液,继续滴定至终点,消耗
淀粉溶液,继续滴定至终点,消耗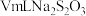 溶液.
溶液.
①步骤Ⅰ需要的玻璃仪器除容量瓶、烧杯、量筒、玻璃棒外,还需要_____________ ;
②滴定至终点时溶液的颜色变化是_____________ ;
③ 溶液的物质的量浓度为
溶液的物质的量浓度为_____________ (用含c、V的代数式表示);
(2)为验证 与
与 的氧化还原能力,利用下列电池装置进行实验。
的氧化还原能力,利用下列电池装置进行实验。
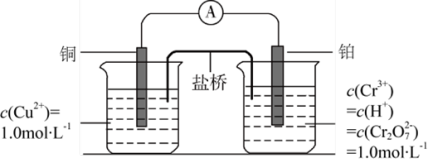
①电池装置中,盐桥用于连接两电极电解质溶液,盐桥中的阴、阳离子应满足下列条件:
i.不与溶液中的物质发生化学反应;ii.离子的电迁移率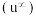 应尽可能地相近.根据下表数据,盐桥中应选择
应尽可能地相近.根据下表数据,盐桥中应选择_____________ 作为电解质;
 无限稀溶液中离子的电迁移率
无限稀溶液中离子的电迁移率
②一段时间后铜电极溶液中 变为
变为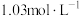 ,铂电极溶液中
,铂电极溶液中 的浓度为
的浓度为_____________  (假设两边溶液体积相等且不变化);铂电极的电极反应式为
(假设两边溶液体积相等且不变化);铂电极的电极反应式为_____________ ;
③由实验结果可确定还原性:
_____________ (填“大于”或“小于”) 。
。
 是实验室常用试剂.回答下列问题:
是实验室常用试剂.回答下列问题:(1)实验室配制一定浓度的
 溶液(橙红色)并标定的实验步骤如下:
溶液(橙红色)并标定的实验步骤如下:步骤Ⅰ.称取约
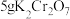 于烧杯中,加入少量蒸馏水溶解,配制成
于烧杯中,加入少量蒸馏水溶解,配制成 溶液;
溶液;步骤Ⅱ.移取
 已配制的
已配制的 溶液于碘量瓶中,加入
溶液于碘量瓶中,加入 过量
过量 ,再加
,再加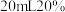 的硫酸,摇匀(
的硫酸,摇匀( 还原为亮绿色的
还原为亮绿色的 ),在暗处放置
),在暗处放置 ,加水稀释,用
,加水稀释,用 的
的 标准溶液滴定
标准溶液滴定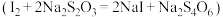 ,接近终点时,加入
,接近终点时,加入 淀粉溶液,继续滴定至终点,消耗
淀粉溶液,继续滴定至终点,消耗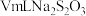 溶液.
溶液.①步骤Ⅰ需要的玻璃仪器除容量瓶、烧杯、量筒、玻璃棒外,还需要
②滴定至终点时溶液的颜色变化是
③
 溶液的物质的量浓度为
溶液的物质的量浓度为(2)为验证
 与
与 的氧化还原能力,利用下列电池装置进行实验。
的氧化还原能力,利用下列电池装置进行实验。
①电池装置中,盐桥用于连接两电极电解质溶液,盐桥中的阴、阳离子应满足下列条件:
i.不与溶液中的物质发生化学反应;ii.离子的电迁移率
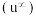 应尽可能地相近.根据下表数据,盐桥中应选择
应尽可能地相近.根据下表数据,盐桥中应选择 无限稀溶液中离子的电迁移率
无限稀溶液中离子的电迁移率阳离子 |
| 阴离子 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
 变为
变为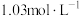 ,铂电极溶液中
,铂电极溶液中 的浓度为
的浓度为 (假设两边溶液体积相等且不变化);铂电极的电极反应式为
(假设两边溶液体积相等且不变化);铂电极的电极反应式为③由实验结果可确定还原性:

 。
。
您最近一年使用:0次
解题方法
5 . 欧洲足球锦标赛事中的拍摄车,装着“绿色心脏”-质子交换膜燃料电池,其工作原理如图所示。下列叙述中正确的是
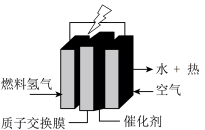

| A.装置中的能量变化为电能转化为化学能 |
| B.通入氢气的电极发生还原反应 |
| C.通入空气的电极反应式:O2+4e-+ 4H+=2H2O |
| D.装置中电子从通入空气的电极经过导线流向通入氢气的电极 |
您最近一年使用:0次
名校
解题方法
6 . 普通水泥在固化过程中其自由水分子减少并形成碱性溶液。根据这一物理、化学特点,科学家发明了电动势法测水泥的初凝时间。此法的原理如图所示,反应的总方程式为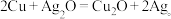 下列说法错误的是
下列说法错误的是
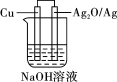
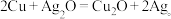 下列说法错误的是
下列说法错误的是
A.正极的电极反应式为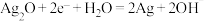 |
B.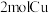 和 和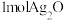 的总能量高于 的总能量高于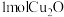 和 和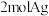 的总能量 的总能量 |
C.电池工作时, 向 向 电极移动 电极移动 |
D.测量原理示意图中,电流方向从 流向 流向 |
您最近一年使用:0次
2024-02-13更新
|
639次组卷
|
2卷引用:陕西省咸阳市实验中学2022-2023学年高二上学期开学质量检测化学试题
名校
解题方法
7 . 高能LiFePO4电池,多应用于公共交通。电池中间是聚合物的隔膜,主要作用是在反应过程中只让Li+通过。结构如图所示:
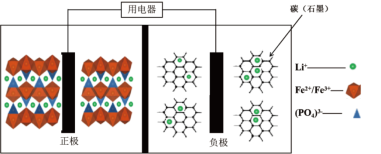
原理为:(1− x)LiFePO4+xFePO4+LixCn LiFePO4+nC。下列说法
LiFePO4+nC。下列说法不正确 的是

原理为:(1− x)LiFePO4+xFePO4+LixCn
 LiFePO4+nC。下列说法
LiFePO4+nC。下列说法A.放电时,导线中每流过 ,理论上就有2 mol Li+从正极区经聚合物隔膜向负极区移动并嵌入石墨中 ,理论上就有2 mol Li+从正极区经聚合物隔膜向负极区移动并嵌入石墨中 |
| B.正极和负极的质量变化相等 |
| C.拆解废电池前先进行充电处理既可以保证安全又有利于回收锂 |
| D.放电时,正极电极反应式:xFePO4+xLi++xe− =xLiFePO4 |
您最近一年使用:0次
名校
解题方法
8 . 为了实现碳中和, 的处理成为各国科学家的研究重点。
的处理成为各国科学家的研究重点。
Ⅰ.将二氧化碳转化为绿色液体燃料甲醇,制备原理为 。已知某些化学键的键能数据如表所示。
。已知某些化学键的键能数据如表所示。
(1)当反应 生成
生成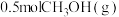 时,
时,_____ (填“放出”或“吸收”)_____  能量。
能量。
(2)在体积为 的恒温、恒容密闭容器中,充入
的恒温、恒容密闭容器中,充入 和
和 进行反应
进行反应 (不考虑其他副反应)。
(不考虑其他副反应)。 时,测得
时,测得 和
和 的体积分数之比为
的体积分数之比为 且比值不再随时间变化。回答下列问题:
且比值不再随时间变化。回答下列问题:
①反应开始到平衡时,以 的浓度变化表示反应的平均速率v(H2)=
的浓度变化表示反应的平均速率v(H2)=_____  。
。
② 时,正、逆反应速率的大小关系为
时,正、逆反应速率的大小关系为
_____  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
③该条件下反应达到平衡的标志有_____ (填字母)。
A. 和
和 的浓度之比为
的浓度之比为
B.断裂 键的同时生成
键的同时生成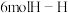 键
键
C.容器内混合气体的密度保持不变
D.容器内混合气体的平均摩尔质量保持不变
Ⅱ.用二氧化碳作原料设计 辅助
辅助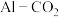 电池,电池反应产物为
电池,电池反应产物为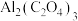 ,电池工作原理如图所示。正极的电极反应式为
,电池工作原理如图所示。正极的电极反应式为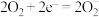 、
、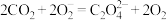 。
。_____ (填“ ”或“多孔碳”)电极流出,电池的负极反应式为
”或“多孔碳”)电极流出,电池的负极反应式为_____ 。
 的处理成为各国科学家的研究重点。
的处理成为各国科学家的研究重点。Ⅰ.将二氧化碳转化为绿色液体燃料甲醇,制备原理为
 。已知某些化学键的键能数据如表所示。
。已知某些化学键的键能数据如表所示。| 化学键 |  |  |  |  |  |
键能/( ) ) | 413.6 | 436.0 | 351.0 | 745.0 | 462.8 |
(1)当反应
 生成
生成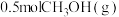 时,
时, 能量。
能量。(2)在体积为
 的恒温、恒容密闭容器中,充入
的恒温、恒容密闭容器中,充入 和
和 进行反应
进行反应 (不考虑其他副反应)。
(不考虑其他副反应)。 时,测得
时,测得 和
和 的体积分数之比为
的体积分数之比为 且比值不再随时间变化。回答下列问题:
且比值不再随时间变化。回答下列问题:①反应开始到平衡时,以
 的浓度变化表示反应的平均速率v(H2)=
的浓度变化表示反应的平均速率v(H2)= 。
。②
 时,正、逆反应速率的大小关系为
时,正、逆反应速率的大小关系为
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。③该条件下反应达到平衡的标志有
A.
 和
和 的浓度之比为
的浓度之比为
B.断裂
 键的同时生成
键的同时生成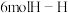 键
键C.容器内混合气体的密度保持不变
D.容器内混合气体的平均摩尔质量保持不变
Ⅱ.用二氧化碳作原料设计
 辅助
辅助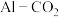 电池,电池反应产物为
电池,电池反应产物为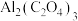 ,电池工作原理如图所示。正极的电极反应式为
,电池工作原理如图所示。正极的电极反应式为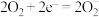 、
、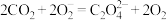 。
。
 ”或“多孔碳”)电极流出,电池的负极反应式为
”或“多孔碳”)电极流出,电池的负极反应式为
您最近一年使用:0次
名校
解题方法
9 . 已知氧化性 >Fe3+,设计如图所示原电池,盐桥中装有饱和K2SO4溶液。下列说法不正确的是
>Fe3+,设计如图所示原电池,盐桥中装有饱和K2SO4溶液。下列说法不正确的是
 >Fe3+,设计如图所示原电池,盐桥中装有饱和K2SO4溶液。下列说法不正确的是
>Fe3+,设计如图所示原电池,盐桥中装有饱和K2SO4溶液。下列说法不正确的是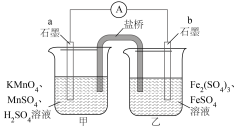
| A.a为电池的负极,b为电池的正极 |
| B.电流从a经过外电路流向b |
C.电池工作时,盐桥中的 移向乙烧杯 移向乙烧杯 |
D.A电极上发生的反应为: +8H++5e- = Mn2++4H2O +8H++5e- = Mn2++4H2O |
您最近一年使用:0次
名校
10 . 碱性锌锰干电池是一种使用广泛的便携式电源,电池总反应为Zn+2MnO2+H2O=ZnO+2MnOOH。下列说法错误的是
| A.MnOOH中Mn的化合价为+3 |
| B.参与正极反应的物质为MnO2和H2O |
| C.负极的电极反应为Zn-2e-=Zn2+ |
| D.电池工作时,电子由负极通过外电路流向正极 |
您最近一年使用:0次