解题方法
1 . 某学习小组的同学查阅相关资料知氧化性: ,设计了盐桥式原电池,如图。盐桥中装有琼脂与饱和
,设计了盐桥式原电池,如图。盐桥中装有琼脂与饱和 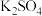 溶液。下列叙述中正确的是
溶液。下列叙述中正确的是

 ,设计了盐桥式原电池,如图。盐桥中装有琼脂与饱和
,设计了盐桥式原电池,如图。盐桥中装有琼脂与饱和 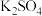 溶液。下列叙述中正确的是
溶液。下列叙述中正确的是
| A.甲烧杯的溶液中发生还原反应 |
B.电池工作时,盐桥中的 移向乙烧杯 移向乙烧杯 |
C.外电路的电流方向是从 到 到  |
D.乙烧杯中发生的电极反应为: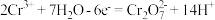 |
您最近一年使用:0次
名校
解题方法
2 . 直接H2O2-H2O2电池是一种新型化学电源,其工作原理如图所示。电池放电时,下列说法不正确的是


| A.电极Ⅰ电势低 |
| B.电极Ⅱ的反应为H2O2-2e- +2H+=2H2O |
| C.内电路电流方向:电极Ⅰ→电极Ⅱ |
| D.该电池的设计利用了H2O2在酸碱性不同条件下氧化性、还原性的差异 |
您最近一年使用:0次
2023-11-11更新
|
121次组卷
|
2卷引用:黑龙江省哈尔滨市第九中学2023-2024学年高三上学期10月月考化学试题
名校
解题方法
3 . 将铜棒插入浓、稀 溶液中(装置如图)、观察到电流计指针发生偏转,一段时间后,浸入浓
溶液中(装置如图)、观察到电流计指针发生偏转,一段时间后,浸入浓 溶液的铜棒变粗。下列说法不正确的是
溶液的铜棒变粗。下列说法不正确的是
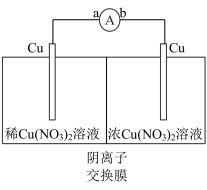
 溶液中(装置如图)、观察到电流计指针发生偏转,一段时间后,浸入浓
溶液中(装置如图)、观察到电流计指针发生偏转,一段时间后,浸入浓 溶液的铜棒变粗。下列说法不正确的是
溶液的铜棒变粗。下列说法不正确的是
A.铜棒变粗的反应: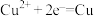 |
| B.导线中电子移动的方向:b→a |
C.随着反应的进行,浓、稀 溶液的浓度逐渐接近 溶液的浓度逐渐接近 |
D. 的氧化性随 的氧化性随 增大而增强,Cu的还原性随 增大而增强,Cu的还原性随 增大而减弱 增大而减弱 |
您最近一年使用:0次
2023-03-30更新
|
504次组卷
|
4卷引用:北京市朝阳区2023届高三一模考试化学试题
名校
解题方法
4 . 某同学利用下列电池装置进行实验,探究 的氧化性和还原性。
的氧化性和还原性。
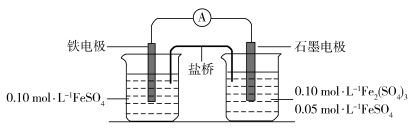
根据实验现象,下列分析不正确 的是
 的氧化性和还原性。
的氧化性和还原性。
根据实验现象,下列分析
| A.电流表显示电子由铁电极流向石墨电极,可知盐桥中的阳离子进入石墨电极溶液中 |
B.一段时间后石墨电极上未见 析出且铁电极溶液中 析出且铁电极溶液中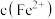 增大,可知石墨电极溶液中 增大,可知石墨电极溶液中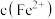 也增大 也增大 |
C.由A、B中的现象可知, 还原性小于 还原性小于 、氧化性小于 、氧化性小于 |
D.一段时间后两极溶液中的 浓度若相等,说明反应已达到平衡状态 浓度若相等,说明反应已达到平衡状态 |
您最近一年使用:0次
2022-06-03更新
|
796次组卷
|
6卷引用:北京市和平街第一中学2021-2022学年高三下学期保温化学试题
北京市和平街第一中学2021-2022学年高三下学期保温化学试题(已下线)第09讲 铁及其重要化合物(讲)-2023年高考化学一轮复习讲练测(全国通用)(已下线)易错点06 铁及其化合物-备战2023年高考化学考试易错题(已下线)专题12 电化学的综合应用(已下线)2022年北京高考真题化学试题变式题(选择题11-14)广东省梅州市大埔县虎山中学2022-2023学年高三上学期12月月考化学试题
名校
解题方法
5 . 已知氧化性 >Fe3+,设计如图所示原电池,盐桥中装有饱和K2SO4溶液。下列说法不正确的是
>Fe3+,设计如图所示原电池,盐桥中装有饱和K2SO4溶液。下列说法不正确的是
 >Fe3+,设计如图所示原电池,盐桥中装有饱和K2SO4溶液。下列说法不正确的是
>Fe3+,设计如图所示原电池,盐桥中装有饱和K2SO4溶液。下列说法不正确的是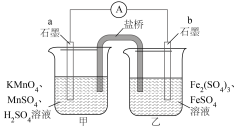
| A.a为电池的负极,b为电池的正极 |
| B.电流从a经过外电路流向b |
C.电池工作时,盐桥中的 移向乙烧杯 移向乙烧杯 |
D.A电极上发生的反应为: +8H++5e- = Mn2++4H2O +8H++5e- = Mn2++4H2O |
您最近一年使用:0次
22-23高三上·广东深圳·阶段练习
名校
6 . 羟基自由基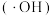 是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为
是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为 、
、 的原电池一电解池组合装置(如图所示),该装置能实现发电、环保二位一体。下列说法错误的是
的原电池一电解池组合装置(如图所示),该装置能实现发电、环保二位一体。下列说法错误的是
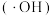 是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为
是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为 、
、 的原电池一电解池组合装置(如图所示),该装置能实现发电、环保二位一体。下列说法错误的是
的原电池一电解池组合装置(如图所示),该装置能实现发电、环保二位一体。下列说法错误的是
A.a为正极,其电极的电极反应式为: |
B.工作一段时间,b极附近 减小 减小 |
| C.系统工作时,电流由b极经III、II、I室流向a极 |
D.系统工作时,每转移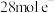 消耗 消耗 苯酚 苯酚 |
您最近一年使用:0次
解题方法
7 . 某同学研究FeSO4溶液和AgNO3溶液的反应,设计如下对比实验。
下列说法不正确的是
| 实验 | 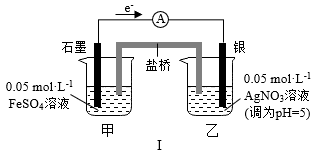 | 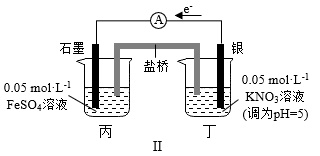 |
| 现象 | 连通电路后,电流表指针向右偏转,分别取反应前和反应一段时间后甲烧杯中的溶液,滴加KSCN溶液,前者几乎无色,后者显红色 | 连通电路后,电流表指针向左发生微小的偏转,丙、丁烧杯中均无明显现象 |
| A.仅由Ⅰ中的现象不能推知Ag+的氧化性强于Fe3+ |
| B.Ⅱ中电流表指针向左偏转的原因可能是银发生了电化学腐蚀 |
| C.Ⅱ中若将银电极换成石墨电极,电流表指针可能不再向左偏转 |
D.对比Ⅰ、Ⅱ可知,Ⅰ中 氧化了Fe2+ 氧化了Fe2+ |
您最近一年使用:0次
解题方法
8 . 为了探究原电池和电解池的工作原理,某研究性学习小组分别用如图甲、乙所示的装置进行实验,回答下列问题。
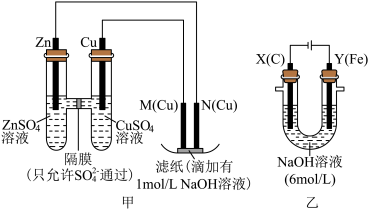
Ⅰ.用甲装置进行第一组实验:
(1)甲中电子的流向正确的是_____ (填序号)。
A.由Cu流向M,M流向N,N流向Zn
B.由Cu沿导线流向M,由N沿导线流向Zn
C.由Zn沿导线流向N,由M沿导线流向Cu
(2)在保证电极反应不变的情况下,下列材料能代替硫酸铜溶液中Cu电极的是_____(填序号)。
(3)实验过程中,甲池左侧的 浓度
浓度_____ (填“增大”或“减小”),滤纸上能观察到的现象是_____ 。
Ⅱ.该小组同学用乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子( )在溶液中呈紫红色。请根据实验现象及资料信息,填写下列空白:
)在溶液中呈紫红色。请根据实验现象及资料信息,填写下列空白:
(4)可用碱性甲烷燃料电池作为乙池的外加电源,写出该燃料电池负极的电极反应式_____ 。
(5)电解过程中,X极附近溶液的碱性_____ (填“增强”“减弱”或“不变”)。
(6)电解过程中,Y极发生的电极反应为 和
和_____ 。

Ⅰ.用甲装置进行第一组实验:
(1)甲中电子的流向正确的是
A.由Cu流向M,M流向N,N流向Zn
B.由Cu沿导线流向M,由N沿导线流向Zn
C.由Zn沿导线流向N,由M沿导线流向Cu
(2)在保证电极反应不变的情况下,下列材料能代替硫酸铜溶液中Cu电极的是_____(填序号)。
| A.石墨 | B.铂 | C.铝 | D.镁 |
 浓度
浓度Ⅱ.该小组同学用乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子(
 )在溶液中呈紫红色。请根据实验现象及资料信息,填写下列空白:
)在溶液中呈紫红色。请根据实验现象及资料信息,填写下列空白:(4)可用碱性甲烷燃料电池作为乙池的外加电源,写出该燃料电池负极的电极反应式
(5)电解过程中,X极附近溶液的碱性
(6)电解过程中,Y极发生的电极反应为
 和
和
您最近一年使用:0次
名校
9 . 某研究性学习小组的同学设计了一个原电池如图所示:
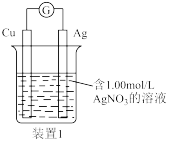
Ⅰ.根据上述原电池,请回答下列问题:
(1)Ag电极是_______ 极(填“正”或“负”),铜电极上发生的电极反应式是_______ 。
(2)溶液中的NO3-的移动方向为_______ (填“自右向左” 或“自左向右”)。
Ⅱ.研究性学习小组的同学们对该原电池中应出现的实验现象进行了预测,他们认为应该有这些现象:
①Cu电极要发生溶解;
②电流计中指针发生偏转;
③Ag电极上有固体物质析出;
④……
请回答下列问题:
(3)预测④的现象为_______ 。
(4)但同学们发现,除了以上预测的现象之外,在银电极附近出现了无色气泡,一段时间后银电极上方的空气中出现红棕色。该红棕色气体为_______ 。
(5)为了探究出现该现象的原因,同学们测定了电解质溶液的pH,发现溶液中的H+浓度为0.80mol/L,据此推断,原电池体系中应存在化学反应_______ (写出该反应的离子方程式)。
(6)同学们通过查阅资料了解到,常温下1.00mol/L的AgNO3溶液pH为5(即H+ 为10-5mol/L),说明装置1中硝酸银溶液已用硝酸进行了酸化。于是又设计了另一个原电池(装置2)以说明上述原电池中的确存在这一反应,如图所示,以下最宜 选用为该电池电解质溶液的是_______ (填标号)。
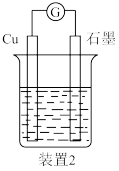
a.0.80mol/L HNO3
b.0.80mol/L HCl和1.00 mol/L NaNO3的混合液
c.0.40mol/L H2SO4和1.80mol/L NaNO3的混合溶液
d.0.80mol/L CH3COOH和1.00mol/L NaNO3的混合溶液
通过实验,发现该电池在一段时间后出现与(2)中相同的现象,说明原电池中的确存在该反应。
Ⅲ.为了进一步探究电解质溶液的浓度对电池反应速率的影响,同学们准备了两组装置,并分别在它们的银电极上安装了重力传感器,其中一组电解质溶液为500mL 1.00mol/L AgNO3溶液;另一组为500mL 0.50mol/L AgNO3溶液(两组硝酸银溶液均已净化,为单一组分),由传感器所得数据作图如图:
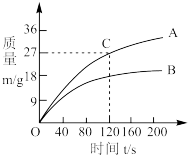
(7)其中代表电解质为0.50mol/L AgNO3溶液的一组的曲线是_______ (填“A”或“B”) 。
(8)对于A曲线,以硝酸银溶液浓度变化来表示120s内的反应速率υ=_______ (保留2位有效数字,忽略溶液的体积变化)。

Ⅰ.根据上述原电池,请回答下列问题:
(1)Ag电极是
(2)溶液中的NO3-的移动方向为
Ⅱ.研究性学习小组的同学们对该原电池中应出现的实验现象进行了预测,他们认为应该有这些现象:
①Cu电极要发生溶解;
②电流计中指针发生偏转;
③Ag电极上有固体物质析出;
④……
请回答下列问题:
(3)预测④的现象为
(4)但同学们发现,除了以上预测的现象之外,在银电极附近出现了无色气泡,一段时间后银电极上方的空气中出现红棕色。该红棕色气体为
(5)为了探究出现该现象的原因,同学们测定了电解质溶液的pH,发现溶液中的H+浓度为0.80mol/L,据此推断,原电池体系中应存在化学反应
(6)同学们通过查阅资料了解到,常温下1.00mol/L的AgNO3溶液pH为5(即H+ 为10-5mol/L),说明装置1中硝酸银溶液已用硝酸进行了酸化。于是又设计了另一个原电池(装置2)以说明上述原电池中的确存在这一反应,如图所示,以下

a.0.80mol/L HNO3
b.0.80mol/L HCl和1.00 mol/L NaNO3的混合液
c.0.40mol/L H2SO4和1.80mol/L NaNO3的混合溶液
d.0.80mol/L CH3COOH和1.00mol/L NaNO3的混合溶液
通过实验,发现该电池在一段时间后出现与(2)中相同的现象,说明原电池中的确存在该反应。
Ⅲ.为了进一步探究电解质溶液的浓度对电池反应速率的影响,同学们准备了两组装置,并分别在它们的银电极上安装了重力传感器,其中一组电解质溶液为500mL 1.00mol/L AgNO3溶液;另一组为500mL 0.50mol/L AgNO3溶液(两组硝酸银溶液均已净化,为单一组分),由传感器所得数据作图如图:

(7)其中代表电解质为0.50mol/L AgNO3溶液的一组的曲线是
(8)对于A曲线,以硝酸银溶液浓度变化来表示120s内的反应速率υ=
您最近一年使用:0次
2022-07-07更新
|
153次组卷
|
2卷引用:重庆市七校2021-2022学年高一下学期期末考试化学试题
名校
10 . 以肼 为燃料、空气为助燃剂可设计碱性燃料电池,其工作原理如图所示。该电池的优势是能源转化率高,且产物无污染。下列说法错误的是
为燃料、空气为助燃剂可设计碱性燃料电池,其工作原理如图所示。该电池的优势是能源转化率高,且产物无污染。下列说法错误的是
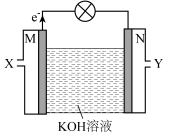
 为燃料、空气为助燃剂可设计碱性燃料电池,其工作原理如图所示。该电池的优势是能源转化率高,且产物无污染。下列说法错误的是
为燃料、空气为助燃剂可设计碱性燃料电池,其工作原理如图所示。该电池的优势是能源转化率高,且产物无污染。下列说法错误的是
| A.空气由Y口通入 |
B.M极的电极反应为 |
C.电池的总反应为 |
| D.电池工作时,溶液的pH增大 |
您最近一年使用:0次
2024-01-15更新
|
431次组卷
|
2卷引用:河北省沧州市部分学校2023-2024学年高三上学期12月联考化学试题



