1 . 水伏发电的原理如图。水溶液进入表面修饰了羟基等亲水基团的毛细管后,因毛细作用和蒸发驱动,携带与管内壁表面电性相反的离子上移,在管内溶液上下两端形成流动电势差。
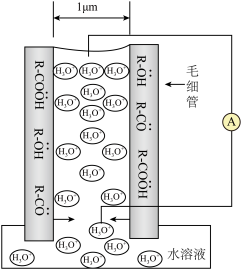
| A.管内溶液下端为负极 |
| B.提高环境温度有利于提高发电效率 |
C.放电时正极发生的反应是 |
| D.水溶液中盐的浓度和阳离子电荷数会影响其电势差 |
您最近一年使用:0次
名校
解题方法
2 . 科研人员利用酸性和碱性两种电解质溶液之间存在的氢离子浓度差,设计了一种如图所示的全氢电池。下列有关叙述错误的是

| A.该电池可将酸碱中和能转化为电能 |
| B.该电池中的氢气可循环利用 |
| C.钠离子通过离子交换膜向左侧迁移 |
D.电极M发生的电极反应式为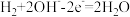 |
您最近一年使用:0次
2024-09-06更新
|
209次组卷
|
2卷引用:云南省昆明市第一中学2024-2025学年高三上学期8月月考化学试题
3 . 铝、铁、硅的单质及化合物在工业生产中具有广泛应用,工业上常用某矿石(主要成分有 、
、 、FeO、
、FeO、 等)来制备绿矾
等)来制备绿矾 和
和 ,其工艺流程如图:
,其工艺流程如图: 是酸性氧化物,不溶于盐酸。回答下列问题:
是酸性氧化物,不溶于盐酸。回答下列问题:
(1)发生过程1时,通常会将“矿石”粉碎,其目的是_______ 。
(2)滤渣1的成分是:_______ (填化学式)。
(3)向溶液A中加入过量铁粉的目的是_______ ,涉及到的离子方程式为_______ 。
(4)写出由滤液1生成滤液2的离子方程式为:_______ 。
(5)由溶液B得到绿矾的实验操作是_______ 。
(6)某原电池用镁、铝作电极,电解质溶液为KOH溶液。该电池的正极为_______ 。负极反应式为_______ 。
 、
、 、FeO、
、FeO、 等)来制备绿矾
等)来制备绿矾 和
和 ,其工艺流程如图:
,其工艺流程如图: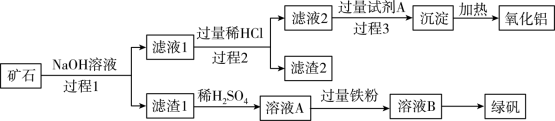
 是酸性氧化物,不溶于盐酸。回答下列问题:
是酸性氧化物,不溶于盐酸。回答下列问题:(1)发生过程1时,通常会将“矿石”粉碎,其目的是
(2)滤渣1的成分是:
(3)向溶液A中加入过量铁粉的目的是
(4)写出由滤液1生成滤液2的离子方程式为:
(5)由溶液B得到绿矾的实验操作是
(6)某原电池用镁、铝作电极,电解质溶液为KOH溶液。该电池的正极为
您最近一年使用:0次
解题方法
4 . 为探究电化学电极反应及产物性质,某化学实验小组按照如图所示接通线路,反应一段时间后,回答下列问题:_____ 极,其电极反应式为_____ 。
(2)U形管内产生的现象为_____ 。
(3)写出有关反应的化学方程式。
A:_____ ; a:_____ ; B:_____ 。
(4)a、b两烧杯中发生的现象分别为_____ 。
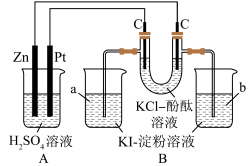
(2)U形管内产生的现象为
(3)写出有关反应的化学方程式。
A:
(4)a、b两烧杯中发生的现象分别为
您最近一年使用:0次
名校
解题方法
5 . 目前一款新型甲醇燃料电池已投放市场,该电池通过特殊的装置进行电能输出,不会造成任何污染,是一种相当环保的绿色电池。如图是甲醇燃料电池的实验装置图。下列有关说法不正确的是
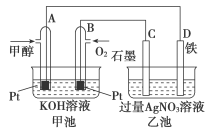
| A.甲池是燃料电池,乙池是电解池 |
B.甲池中负极的电极反应式为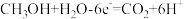 |
| C.A为负极,C为阳极 |
| D.乙池中D电极质量增加5.40g时,理论上甲池中转移0.05mol电子 |
您最近一年使用:0次
名校
解题方法
6 . 银锌电池是一种常见化学电源,其反应原理: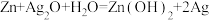 ,下图是其工作示意图。下列说法正确的是
,下图是其工作示意图。下列说法正确的是
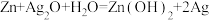 ,下图是其工作示意图。下列说法正确的是
,下图是其工作示意图。下列说法正确的是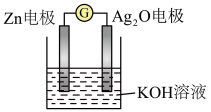
| A.Zn电极是电源的正极 |
B. 电极是发生氧化反应 电极是发生氧化反应 |
C.电池工作时,电子从Zn电极经导线流向 电极,再出 电极,再出 电极经电解质溶液流向Zn电极 电极经电解质溶液流向Zn电极 |
D.Zn电极上发生的反应: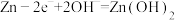 |
您最近一年使用:0次
名校
解题方法
7 . 电池在生产生活中的应用越来越广泛。某小组设计实验,探究Al片和Cu片为电极,浓硝酸为电解液的原电池原理:
(1)浓硝酸浓度的测定:准确量取4.000 mL浓硝酸,稀释至500 mL,得到溶液X。移取20.00 mL溶液X,用0.1250 mol/LNaOH溶液滴定,重复三次,平均每次消耗NaOH溶液19.20 mL。
①上述操作没有用到的仪器有_________ (填正确答案的编号)。_________  。
。
用此浓硝酸完成(2)和(3)中实验。
(2)将Cu片置于浓硝酸中,Cu片逐渐溶解,产生大量红棕色气泡,反应的离子方程式为__________ 。
(3)探究以Al片、Cu片为电极,浓硝酸为电解液形成原电池的机理,示意图和实验记录如下:
__________ 。
②7s左右电流表指针由左向右偏转的原因是__________ 。
③实验过程中均有气体产生,31 min前和31min后产生的气体不同,请结合题目信息和步骤Ⅰ气体的现象描述,分析31 min以后产生的气体是什么,并描述相关现象__________ 。
(1)浓硝酸浓度的测定:准确量取4.000 mL浓硝酸,稀释至500 mL,得到溶液X。移取20.00 mL溶液X,用0.1250 mol/LNaOH溶液滴定,重复三次,平均每次消耗NaOH溶液19.20 mL。
①上述操作没有用到的仪器有
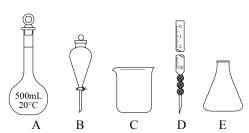
 。
。用此浓硝酸完成(2)和(3)中实验。
(2)将Cu片置于浓硝酸中,Cu片逐渐溶解,产生大量红棕色气泡,反应的离子方程式为
(3)探究以Al片、Cu片为电极,浓硝酸为电解液形成原电池的机理,示意图和实验记录如下:
| 步骤 | 操作及记录 |
| Ⅰ | 图a装置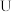 型管内盛有浓硝酸,插入新打磨的Al片和Cu片,电流表指针迅速向左偏转(如图b),Cu片周围产生红棕色气体 型管内盛有浓硝酸,插入新打磨的Al片和Cu片,电流表指针迅速向左偏转(如图b),Cu片周围产生红棕色气体 |
| Ⅱ | 一段时间后,电流表读数逐渐变小,7 s时电流表读数减小为0 |
| Ⅲ | 电流表指针又向右偏转,读数迅速变大后稳定 |
| Ⅳ | 稳定一段时间后电流表读数逐渐变小,31 min时电流表读数为0 |
| Ⅴ | 电流表指针又向左偏转,读数逐渐变大后趋于稳定 |
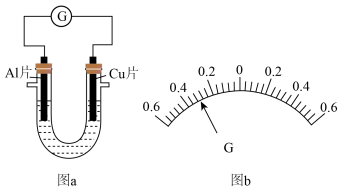
②7s左右电流表指针由左向右偏转的原因是
③实验过程中均有气体产生,31 min前和31min后产生的气体不同,请结合题目信息和步骤Ⅰ气体的现象描述,分析31 min以后产生的气体是什么,并描述相关现象
您最近一年使用:0次
8 . 科学家开发了基于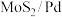 压电催化和能带弯曲的力场辅助超声波激活
压电催化和能带弯曲的力场辅助超声波激活 电池,电池反应为
电池,电池反应为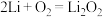 ,电池示意图如图所示。下列叙述正确的是
,电池示意图如图所示。下列叙述正确的是
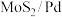 压电催化和能带弯曲的力场辅助超声波激活
压电催化和能带弯曲的力场辅助超声波激活 电池,电池反应为
电池,电池反应为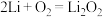 ,电池示意图如图所示。下列叙述正确的是
,电池示意图如图所示。下列叙述正确的是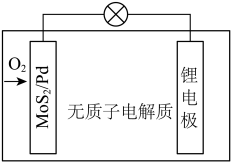
A.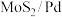 极为负极,发生氧化反应 极为负极,发生氧化反应 |
B.金属Li在 中燃烧可生成 中燃烧可生成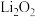 |
C.锂电极的电极反应式为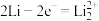 |
D.2.24 L  (标准状况)完全反应时转移0.2 mol电子 (标准状况)完全反应时转移0.2 mol电子 |
您最近一年使用:0次
2024-07-17更新
|
224次组卷
|
2卷引用:云南省楚雄彝族自治州2023-2024学年高二下学期7月期末考试化学试题
解题方法
9 . 利用微生物可将水中苯酚的化学能直接转化为电能,装置如图所示,电池工作时,下列说法错误的是

A.左侧工作室的电极反应式为 (苯酚) (苯酚)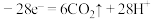 |
B.右侧工作室发生还原反应, 得到电子 得到电子 |
C. 和 和 均为非可燃性气体,且均有氧化性 均为非可燃性气体,且均有氧化性 |
| D.左侧离子交换膜为阳离子交换膜,右侧离子交换膜为阴离子交换膜 |
您最近一年使用:0次
名校
10 . 电池的应用对人类社会的发展作出了巨大贡献。试运用化学反应与电能知识回答下列问题。
(1)用下图甲、乙所示装置进行实验。请回答下列问题:___________ ;乙中:化学能→___________ 。
②乙装置中锌棒上发生的反应为___________ ;若反应前Zn棒和Cu棒的质量相同,当导线中转移0.1mol电子时,两金属电极的质量之差为___________ g。
(2)某实验小组设计了如图所示原电池装置。___________ (填“铝棒”或“镁棒”),Al棒上发生的电极反应式为___________ 。
②若电解质溶液X为稀硫酸,Mg棒上发生的电极反应式是___________ ,外导线中电子的流动方向是___________ (填“Al→Mg”或“Mg→Al”)。
(1)用下图甲、乙所示装置进行实验。请回答下列问题:
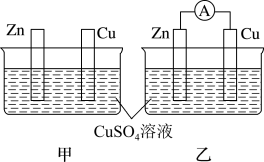
②乙装置中锌棒上发生的反应为
(2)某实验小组设计了如图所示原电池装置。

②若电解质溶液X为稀硫酸,Mg棒上发生的电极反应式是
您最近一年使用:0次



