1 . 原电池是化学对人类的一项重大贡献。某兴趣小组为研究原电池原理,设计了如图所示装置。
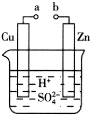
(1)a和b不连接时,烧杯中现象是_______ 。
(2)a和b用导线连接,Cu极为原电池___ (“正”或“负”)极,电极反应式为___ ;溶液中H+移向__ (填“Cu”或“Zn”)极。
(3)若电解质溶液改为AgNO3溶液,当转移0.2mol电子时,则理论上Cu片质量变化为_____ 。

(1)a和b不连接时,烧杯中现象是
(2)a和b用导线连接,Cu极为原电池
(3)若电解质溶液改为AgNO3溶液,当转移0.2mol电子时,则理论上Cu片质量变化为
您最近一年使用:0次
名校
解题方法
2 . 如图为某学生自制的番茄电池,下列说法正确的是
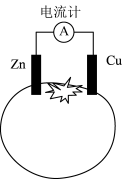

| A.锌作负极 |
| B.铜片质量减小 |
| C.电子由铜通过导线流向锌 |
| D.实现了电能向化学能的转化 |
您最近一年使用:0次
3 . 火星大气中含有大量 ,一种有
,一种有 参加反应的新型全固态电池有望为火星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时
参加反应的新型全固态电池有望为火星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时
 ,一种有
,一种有 参加反应的新型全固态电池有望为火星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时
参加反应的新型全固态电池有望为火星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时| A.负极上发生还原反应 | B. 在正极上得电子 在正极上得电子 |
| C.阳离子由正极移向负极 | D.将电能转化为化学能 |
您最近一年使用:0次
2021-06-11更新
|
12926次组卷
|
63卷引用:江西省南昌市第十中学2020-2021学年高一下学期期末考试化学试题
江西省南昌市第十中学2020-2021学年高一下学期期末考试化学试题甘肃省天水市田家炳中学2020-2021学年高一下学期期末考试化学试题2021年新高考广东化学高考真题四川省成都七中(高新校区)2020-2021学年高二下学期期末零诊模拟化学试题(已下线)课时30 新型原电池装置-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点21 原电池 化学电源-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点21 原电池 化学电源-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第16讲 原电池 (讲)— 2022年高考化学一轮复习讲练测(新教材新高考)上海交通大学附属中学2021-2022学年高三上学期摸底测试化学试卷题重庆市缙云教育联盟2021-2022学年高三9月月度质量检测化学试题(已下线)考向19 原电池 化学电源-备战2022年高考化学一轮复习考点微专题(已下线)专题11 电化学-备战2022年高考化学学霸纠错(全国通用)2021年广东省高考化学试卷变式题1-10题山西省晋城市第一中学2021-2022学年高二上学期12月月考化学试题河北省武安市第一中学2021-2022学年高二上学期第一次月考化学试题上海市南洋模范中学2021-2022学年高一下学期3月考化学试题上海市南洋模范中学2021-2022学年高一下学期3月月考化学试题广东省广州市第一中学2021-2022学年高一下学期期中考试化学试题广东珠海市斗门第一中学2021-2022学年高一下学期期中考试化学试题上海市同济大学第一附属中学2021-2022学年高一下学期等级阶段性测试2化学试题四川省内江市2021-2022学年高一下学期期末检测理科化学试题上海市吴淞中学2021-2022学年高一下学期期末考试化学试题广东省广州市广雅中学2021-2022学年高一下学期期末考试化学试题广东省揭阳华侨高级中学2021-2022学年高二上学期第三次阶段考试化学试题江西省樟树航天中学高三年级2021-2022学年高三上学期10月调研考试化学试题北京市第一六一中学2022-2023学年高一下学期期中考试化学试题广东省东莞实验中学2022-2023学年高一下学期第二次月考化学试题浙江省普通高中2023-2024学年高一下学期学考模拟考试化学试题(已下线)第12练 原电池原理及其应用-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)山西省怀仁市2021-2022学年高二上学期期末调研化学试题上海市徐汇区2022届高三一模化学试题(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题06 电化学原理应用—2022年高考化学二轮复习讲练测(全国版)-讲义(已下线)专题11 电化学-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题06 电化学原理应用—2022年高考化学二轮复习讲练测(全国版)-练习陕西省咸阳市武功县普集高级中学2021-2022学年高三上学期期末考试化学试题(已下线)押新高考卷12题 电化学基础-备战2022年高考化学临考题号押题(新高考通版)上海市敬业中学2021-2022学年高三下学期5月在线教学质量检测化学试题(已下线)专题08 电化学及其应用-三年(2020-2022)高考真题分项汇编(已下线)考点18 原电池 化学电源-备战2023年高考化学一轮复习考点帮(全国通用)福建省莆田华侨中学2021-2022学年高二上学期期中考试化学试题福建省莆田华侨中学2021-2022学年高二上学期期中考试化学试题(已下线)第15练 化学反应与能量变化-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第16讲 原电池 新型电源 (讲)-2023年高考化学一轮复习讲练测(新教材新高考)广东省广州市第十六中学2022-2023学年高二上学期期中化学试题(已下线)专题05 化学能与电能的转化(练)-2023年高考化学二轮复习讲练测(新高考专用)上海市长宁区2022-2023学年高二上学期教学质量检测化学试题广东省深圳市龙华区2021-2022学年高二上学期期末学业质量监测化学试题(已下线)专题16 新型电化学装置分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第六章 化学反应与能量 第35讲 原电池 化学电源(已下线)题型103 原电池的构成条件及工作原理上海市七宝中学2022-2023学年高二下学期开学等级考化学试题广东省揭阳市普宁市2022-2023学年高二上学期1月期末测试化学试题(已下线)专题10 电化学及其应用-2023年高考化学真题题源解密(全国通用)微专题(14) 新型化学电源(已下线)考点18 原电池 化学电源(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第3讲 原电池 化学电源第四章 化学反应与电能 第一节 原电池 第1课时 原电池的工作原理湖北省武汉市江汉区2023-2024学年高二上学期新起点摸底考试化学试题(已下线)考点2 原电池 新型电源(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)上海市徐汇区徐汇中学2022-2023学年高三上学期11月期中考试化学试题辽宁省沈阳市东北育才学校高中部2023-2024学年高二上学期第二次月考化学试题
4 . 根据如图所示的装置,完成下列各空。
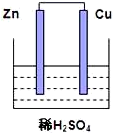
(1)该装置中的总反应式为___________ 。
(2)溶液中的H+移向___________ (填“Cu片”或“Zn片”)
(3)Zn电极的反应式为___________ ,发生 ___________ 反应,(填“氧化”或“还原”)
(4)Cu片为原电池的___________ 极(填“正”或“负”),现象为___________ 。

(1)该装置中的总反应式为
(2)溶液中的H+移向
(3)Zn电极的反应式为
(4)Cu片为原电池的
您最近一年使用:0次
名校
解题方法
5 . 某小组为研究原电池原理,设计如图装置。下列叙述正确的是
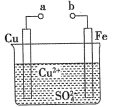

| A.a和b不连接时,铁片上会有H2产生 |
| B.a和b用导线连接时,铁片上发生的反应为Cu2++2e-=Cu |
| C.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
| D.a和b用导线连接时,电子由a流向b |
您最近一年使用:0次
2021-06-01更新
|
336次组卷
|
8卷引用:(人教版2019)必修第二册 第六章 化学反应与能量 第一节 化学反应与能量变化
解题方法
6 . 如图所示的原电池:当电解质溶液为稀H2SO4时,回答下列问题:
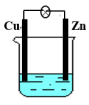
(1)Zn电极是___________ (填“正”或“负”)极,其电极反应为___________ ,该反应是___________ (填“氧化”或“还原”,下同)反应;
(2)Cu电极是___________ 极,其电极反应为___________ ,该反应是___________ 反应。
(3)装置中锌的作用是___________ ,稀硫酸的作用是___________
A.电极材料 B.电极反应物
C.电子导体 D.离子导体

(1)Zn电极是
(2)Cu电极是
(3)装置中锌的作用是
A.电极材料 B.电极反应物
C.电子导体 D.离子导体
您最近一年使用:0次
解题方法
7 . 电能是现代社会应用最广泛的能源之一,某原电池装置如图所示。

其中,Zn电极为原电池的___________ 极(填“正”或“负”),电极反应式是___________ 。Cu电极上发生的反应属于___________ (填“氧化”或“还原”) 反应,当铜表面析出22.4 L氢气(标准状况)时,导线中通过了___________ mol电子。

其中,Zn电极为原电池的
您最近一年使用:0次
解题方法
8 . 化学能在一定条件下可转化为电能。
(1)将锌片放入盛有稀硫酸的烧杯中,反应的化学方程式为_______ 。
(2)将锌片、铜片按照如图所示装置连接,锌片是_______ (填“正极”或“负极”)。能证明化学能转化为电能的实验现象是:_______ 、_______ 。锌片上的电极反应式为_______ 铜片上的电极反应式为_______ 。稀硫酸在如图所示装置中的作用是:传导离子、_______ 。
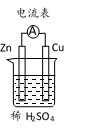
(3)下列反应通过原电池装置,可实现化学能直接转化为电能的是_______ (填序号)。
①2H2+O2 2H2O
2H2O
②Fe+Cu2+=Cu+Fe2+
③CaO+H2O=Ca(OH)2
(1)将锌片放入盛有稀硫酸的烧杯中,反应的化学方程式为
(2)将锌片、铜片按照如图所示装置连接,锌片是

(3)下列反应通过原电池装置,可实现化学能直接转化为电能的是
①2H2+O2
 2H2O
2H2O②Fe+Cu2+=Cu+Fe2+
③CaO+H2O=Ca(OH)2
您最近一年使用:0次
名校
解题方法
9 . 电池的发展是化学对人类的一项重大贡献。
I.用图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计。请回答下列问题:
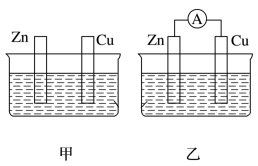
(1)以下叙述中,正确的是___________ (填选项字母)。
a.甲中锌片是负极,乙中铜片是正极
b.两烧杯中铜片表面均有气泡产生
c.两烧杯中溶液的c(H+)均减小
d.乙中电流从铜片经导线流向锌片
e.乙溶液中 向铜片方向移动
向铜片方向移动
(2)变化过程中能量转化的形式主要是:甲为___________ ;乙为___________ 。
(3)乙装置中负极的电极反应式为:___________ ;当乙中产生1.12 L标准状况下气体时,通过导线的电子数为___________ ;若电路导线上通过电子1 mol,则理论上两极的变化是___________ (填选项字母)。
a.锌片减少32.5 g b.锌片增重32.5 g
c.铜片析出1 g H2 d.铜片上析出1 mol H2
(4)为了避免锌片与Cu2+直接接触发生反应而影响原电池的放电效率,人们设计了如图装置。a处装置的名
称为___________ ,在工作时,其内部的阳离子移向___________ (填“正极”或“负极”)。
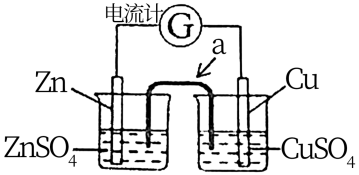
II.将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得OH-定向移向A电极,则___________ (填A或B)处电极入口通CH4,其电极反应式为:___________ 。
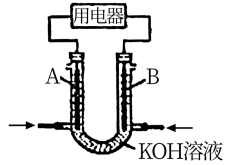
I.用图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计。请回答下列问题:

(1)以下叙述中,正确的是
a.甲中锌片是负极,乙中铜片是正极
b.两烧杯中铜片表面均有气泡产生
c.两烧杯中溶液的c(H+)均减小
d.乙中电流从铜片经导线流向锌片
e.乙溶液中
 向铜片方向移动
向铜片方向移动(2)变化过程中能量转化的形式主要是:甲为
(3)乙装置中负极的电极反应式为:
a.锌片减少32.5 g b.锌片增重32.5 g
c.铜片析出1 g H2 d.铜片上析出1 mol H2
(4)为了避免锌片与Cu2+直接接触发生反应而影响原电池的放电效率,人们设计了如图装置。a处装置的名
称为

II.将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得OH-定向移向A电极,则

您最近一年使用:0次
名校
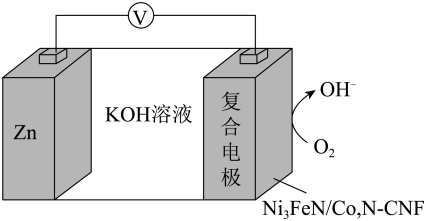
10 . 金属-空气电池因具有较高的能量密度而被广泛应用,一种新型锌-空气电池的工作原理如图所示。该电池工作时,Zn电极的电极反应式为Zn-2e-+4OH-=ZnO +2H2O。下列说法正确的是
+2H2O。下列说法正确的是
 +2H2O。下列说法正确的是
+2H2O。下列说法正确的是
| A.复合电极的电极反应式为O2+4e-+4H+=2H2O |
| B.电子流向:Zn电极→溶液→复合电极 |
| C.电池工作一段时间后,溶液碱性增强 |
| D.金属-空气电池具有较高能量密度的主要原因是空气不需要储存在电池内部 |
您最近一年使用:0次



