名校
解题方法
1 . 有关如图所示四个常用电化学装置的叙述中,正确的是
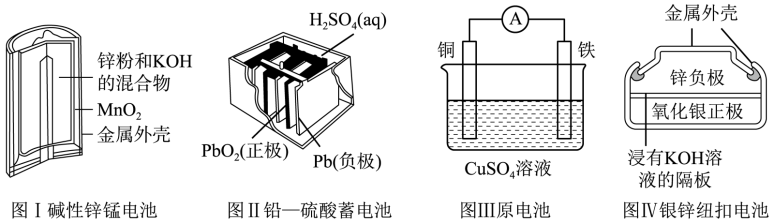

| A.图Ⅰ所示电池中,MnO2的作用是作催化剂 |
| B.图Ⅱ所示电池放电过程中,硫酸浓度不断增大 |
| C.图Ⅲ所示装置工作过程中,电解质溶液中Cu2+浓度始终不变 |
| D.图Ⅳ所示电池中,Ag2O是氧化剂,电池工作过程中被还原为Ag |
您最近一年使用:0次
解题方法
2 . 将A、B两个电极,分别用接线柱平行地固定在一块塑料板上,与电流表连结,插入盛有溶液C的小烧杯中。试回答下列问题:
(1)若A、B分别为铜和铝C为浓 ,原电池的负极为
,原电池的负极为_______ (填“铝”或“铜”)极,铝片上的电极反应式为:_______ 。
(2)若A、B分别为镁和铝,C为氢氧化钠溶液,原电池的负极为_______ (填“铝”或“镁”)极铝片上的电极反应式为:_______ 。
(3)若A、B分别为碳和铝,C为氯化钠溶液,原电池正极上的电极反应式为:_______ 。
(1)若A、B分别为铜和铝C为浓
 ,原电池的负极为
,原电池的负极为(2)若A、B分别为镁和铝,C为氢氧化钠溶液,原电池的负极为
(3)若A、B分别为碳和铝,C为氯化钠溶液,原电池正极上的电极反应式为:
您最近一年使用:0次
名校
解题方法
3 . 下列是某同学做铜锌原电池实验后得出的结论和认识,其中正确的是
| A.构成原电池正极和负极的材料必须是两种金属 |
| B.由铜、锌做电极与硫酸铜溶液组成的原电池中铜是负极 |
| C.电子由锌通过硫酸溶液流向铜电极 |
| D.铜锌原电池工作时,若有13g锌被溶解,则电路中有0.4mol电子通过 |
您最近一年使用:0次
名校
解题方法
4 . 一种新型的燃料电池可用于制取乙醛(CH3CHO),总反应式为 ,电池的主要构成要素如图所示,请回答下列问题:
,电池的主要构成要素如图所示,请回答下列问题:
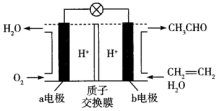
(1)该装置的能量转化形式为_______ 。
(2)a电极为燃料电池的_______ 极,该电极的电极反应式为_______ 。
(3)电池工作时,H+由_______ (填“a电极”或“b电极”,下同)移向_______ 。
(4)生成3.3g乙醛时,需要消耗标准状况下的氧气_______ mL。
 ,电池的主要构成要素如图所示,请回答下列问题:
,电池的主要构成要素如图所示,请回答下列问题:
(1)该装置的能量转化形式为
(2)a电极为燃料电池的
(3)电池工作时,H+由
(4)生成3.3g乙醛时,需要消耗标准状况下的氧气
您最近一年使用:0次
2021-04-24更新
|
241次组卷
|
3卷引用:四川省广安代市中学校2020-2021学年高一下学期第三次月考化学试题
解题方法
5 . 将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是
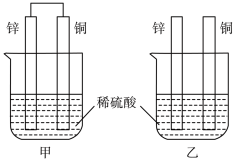

| A.甲中铜片是正极,表面有气泡产生;乙中铜片是负极,表面无气泡产生 |
| B.两烧杯中的SO42-均向铜片移动 |
| C.产生气泡的速度甲比乙快 |
| D.甲烧杯中溶液的pH增大,乙烧杯中溶液的pH减小 |
您最近一年使用:0次
名校
解题方法
6 . 如图为原电池装置示意图:
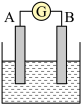
(1)若A为Zn,B为石墨棒,电解质溶液为稀硫酸,则A为_______ 极(填正或负),写出电极反应式:正极_______ ,负极_______ .总反应离子方程式为:_______ 。
(2)若A为铜片,B为铁片,电解质为FeCl3溶液,则A为_______ 极(填正或负),写出电极反应式:正极_______ ,负极_______ .总反应离子方程式为:_______ 。
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为燃料电池,通入氧气的一极为该电池的_______ 极(填正或负),写出电极反应式:正极______________ ,负极______ .总反应方程式为:______ 。

(1)若A为Zn,B为石墨棒,电解质溶液为稀硫酸,则A为
(2)若A为铜片,B为铁片,电解质为FeCl3溶液,则A为
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为燃料电池,通入氧气的一极为该电池的
您最近一年使用:0次
名校
解题方法
7 . 酒精检测仪可帮助交警测试驾驶员饮酒的多少,其工作原理示意图如图所示。反应原理为:CH3CH2OH+O2=CH3COOH+H2O,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量。下列说法正确的是( )
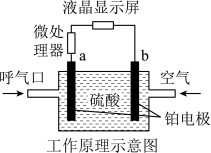

| A.b为正极,电极反应式为:O2+2H2O+4e-=4OH- |
| B.电解质溶液中的H+移向呼气口 |
| C.若有0.4mol电子转移,则在标准状况下消耗2.24L氧气 |
| D.呼出气体中酒精含量越低,微处理器中通过的电流越大 |
您最近一年使用:0次
2020-06-23更新
|
125次组卷
|
2卷引用:四川省资阳市外国语实验学校2021-2022学年高一下学期期中考试化学试题
8 . NO2和N2O4之间发生反应:N2O4 2NO2,一定温度下,体积为2L的密闭容器中,各物质的物质的量随时间变化的关系如图所示。请回答下列问题:
2NO2,一定温度下,体积为2L的密闭容器中,各物质的物质的量随时间变化的关系如图所示。请回答下列问题:
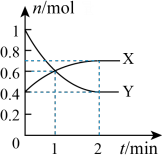
(1)曲线____________ (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线。在0到1min中内用X表示该反应的速率是________________ ,该反应达最大限度时Y的转化率_______ 。
(2)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中 v(NO2)=0.3 mol·L-1·min-1,乙中y(N2O4)=0.2 mol·L-1·min-1,则__________ 中反应更快。
(3)下列描述能表示反应达平衡状态的是______________________ 。
A.容器中X与Y的物质的量相等
B.容器内气体的颜色不再改变
C.2v(X)=v(Y)
D.容器内气体的平均相对分子质量不再改变
E.容器内气体的密度不再发生变化
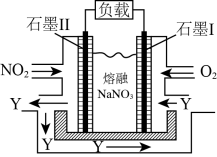
(4)NO2、O2和熔融NaNO3可制作燃料电池,其原理如右图,该电池在使用过程中石墨Ⅱ电极上生成氧化物Y(N2O5),则石墨I电极是______________ (填“正极”或“负极”),石墨Ⅱ的电极反应式为_________________________________ 。
 2NO2,一定温度下,体积为2L的密闭容器中,各物质的物质的量随时间变化的关系如图所示。请回答下列问题:
2NO2,一定温度下,体积为2L的密闭容器中,各物质的物质的量随时间变化的关系如图所示。请回答下列问题: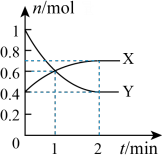
(1)曲线
(2)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中 v(NO2)=0.3 mol·L-1·min-1,乙中y(N2O4)=0.2 mol·L-1·min-1,则
(3)下列描述能表示反应达平衡状态的是
A.容器中X与Y的物质的量相等
B.容器内气体的颜色不再改变
C.2v(X)=v(Y)
D.容器内气体的平均相对分子质量不再改变
E.容器内气体的密度不再发生变化
(4)NO2、O2和熔融NaNO3可制作燃料电池,其原理如右图,该电池在使用过程中石墨Ⅱ电极上生成氧化物Y(N2O5),则石墨I电极是

您最近一年使用:0次
名校
解题方法
9 . 对于锌-铜-稀硫酸组成的原电池装置中,当导线中有0.1mol电子通过时,理论上的两极变化是( )
①锌片溶解了3.25g ②锌片增重3.25g
③铜片上析出0.1g H2 ④铜片上析出0.1mol H2
①锌片溶解了3.25g ②锌片增重3.25g
③铜片上析出0.1g H2 ④铜片上析出0.1mol H2
| A.①和③ | B.①和④ | C.②和③ | D.②和④ |
您最近一年使用:0次
名校
解题方法
10 . 如图是化学课外活动小组设计的用化学电源使LED灯发光的装置示意图。下列有关该装置的说法正确的是
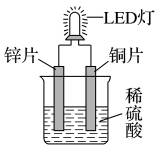

| A.其能量转化的形式主要是“化学能→电能→光能” |
| B.如果将锌片换成铁片,电路中的电流方向将改变 |
| C.铜片为负极,其附近的溶液变蓝,溶液中有Cu2+产生 |
| D.如果将稀硫酸换成柠檬汁,LED灯将不会发光 |
您最近一年使用:0次
2020-05-29更新
|
102次组卷
|
2卷引用:四川省绵阳南山中学2019-2020学年高一下学期期中考试化学试题



