解题方法
1 . 化学家正在研究尿素燃料电池,尿素燃料电池结构如图所示,用这种电池直接去除城市废水中的尿素,下列有关描述正确的是


| A.甲电极为电池的正极 |
B.乙电极的电极反应式为: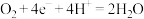 |
| C.电池工作时氢离子向甲电极移动 |
D.D.电池工作时,理论上净化1mol 消耗标准状况下33.6L 消耗标准状况下33.6L 浓度的废水 浓度的废水 |
您最近一年使用:0次
名校
2 . 有关下列四个电化学装置的叙述,正确的是

A.图Ⅰ装置,电子流向: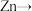 导线 导线 溶液→盐桥 溶液→盐桥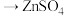 溶液 溶液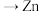 |
B.图Ⅱ装置, 做催化剂 做催化剂 |
C.图Ⅲ装置,正极反应式: |
D.图Ⅳ装置,气体A是 |
您最近一年使用:0次
2023-02-11更新
|
233次组卷
|
3卷引用:山东省济宁市2022-2023学年高二上学期期末考试化学试题
解题方法
3 . 处理含甲醇的废水并进行粗铜精炼的装置如图所示。下列说法错误的是
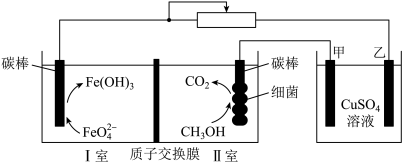

| A.甲电极应为粗铜 |
| B.理论上每产生标准状况下1.12LCO2,甲电极增重9.6g |
| C.装置工作一段时间后,I室中溶液的pH变小 |
| D.原电池负极反应式为CH3OH+H2O-6e-=CO2+6H+ |
您最近一年使用:0次
名校
解题方法
4 . 聚吡咯(PPy)是一种光敏型半导体,在紫外光照射时能快速产生PPyn+,其制成的纳米管反应如下: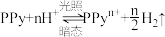 。通过PPy纳米管道一端正电荷分布密度的变化,在电解质溶液中产生离子电流。使用PPy构建一种浓差电池,用来提取天然水中的氢能,其构造如图。下列叙述错误的是
。通过PPy纳米管道一端正电荷分布密度的变化,在电解质溶液中产生离子电流。使用PPy构建一种浓差电池,用来提取天然水中的氢能,其构造如图。下列叙述错误的是

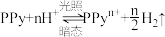 。通过PPy纳米管道一端正电荷分布密度的变化,在电解质溶液中产生离子电流。使用PPy构建一种浓差电池,用来提取天然水中的氢能,其构造如图。下列叙述错误的是
。通过PPy纳米管道一端正电荷分布密度的变化,在电解质溶液中产生离子电流。使用PPy构建一种浓差电池,用来提取天然水中的氢能,其构造如图。下列叙述错误的是
| A.a极的电势低于b极 |
B.a极电极反应式: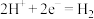 ↑ ↑ |
| C.PPy纳米管道右端正电荷分布密度大 |
| D.照射一段时间后关闭光源,纳米管道中仍能存在微弱电流 |
您最近一年使用:0次
2023-02-11更新
|
254次组卷
|
2卷引用:山东省淄博市2022-2023学年高二上学期期末考试化学试题
5 . 根据实验目的,下列实验及现象、结论都正确的是
| 选项 | 实验目的 | 实验及现象 | 结论 |
| A | 比较金属的活泼性 | Mg、Al做电极,NaOH溶液为离子导体构成原电池,Mg电极附近产生气泡 | Al为正极 |
| B | 探究沉淀的转化 | 向1mL0.01mol•L-1MgCl2溶液中先加入1mL0.05mol•L-1NaOH溶液,再逐滴加入0.1mol•L-1CuSO4溶液,先出现白色沉淀,后又出现蓝色沉淀 | Ksp:Mg(OH)2>Cu(OH)2 |
| C | 探究Mg(OH)2溶于铵盐的原理 | 向Mg(OH)2悬浊液中加入少量NH4Cl固体,溶液变澄清 | NH 水解产生的H+中和Mg(OH)2溶解平衡产生的OH-,使溶解平衡正向移动 水解产生的H+中和Mg(OH)2溶解平衡产生的OH-,使溶解平衡正向移动 |
| D | 比较H2SO3和H2CO3的Ka2 | 测定浓度均为0.1mol•L-1的Na2SO3和Na2CO3溶液的pH值,前者小于后者 | Ka2:H2SO3>H2CO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 高铁电池是一种新型高能高容量电池,某高铁电池的工作原理如图所示。下列说法正确的是
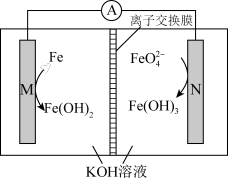

| A.M极电势高于N极电势 |
| B.电池工作时,电子移动方向:M→A→N→M |
C.N极的电极反应式为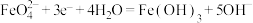 |
| D.电池工作一段时间后,正极区中H+的浓度增大 |
您最近一年使用:0次
2022-11-30更新
|
368次组卷
|
5卷引用:山东省泰安市宁阳县复圣中学2022-2023学年高二上学期期末考试化学试题
7 . 新研发的车载双电极镍氢电池于2021年7月投入量产,有助于实现“双碳”目标。其原理如图所示。放电时a、c电极的反应物为吸附了氢气的稀土合金,可表示为MH;充电时b、d电极的反应物为Ni(OH)2,下列叙述错误的是
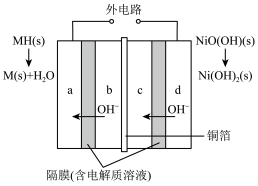

| A.b、d为电池的负极 |
| B.铜箔的作用是隔开电极,传递电子 |
| C.上图示过程中,b电极的电极反应式:NiO(OH)+e-+H2O=Ni(OH)2+OH- |
| D.充电时,每转移1mol电子,该电池的负极共增重1g |
您最近一年使用:0次
名校
解题方法
8 . 某同学欲用如图所示的装置实现反应: 2Fe3++Cu = 2Fe2++Cu2+, 将化学能转化为电能,下列关于此装置的几种构成中,能实现此转化的是
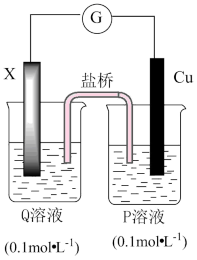

| 成分 选项 | X | Q | P |
| A | Fe | FeCl2 | CuSO4 |
| B | 石墨 | FeCl3 | CuSO4 |
| C | Cu | FeCl2 | CuSO4 |
| D | Fe | FeCl2 | H2SO4 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-22更新
|
363次组卷
|
5卷引用:山东省菏泽市2021-2022学年高二上学期期末教学质量检测化学试题
解题方法
9 . 全钒液流电池是一种活性物质循环流动的液态电池,以溶解于一定浓度硫酸溶液中的不同价态的钒离子为电极反应的活性物质,基本工作原理示意图如下:
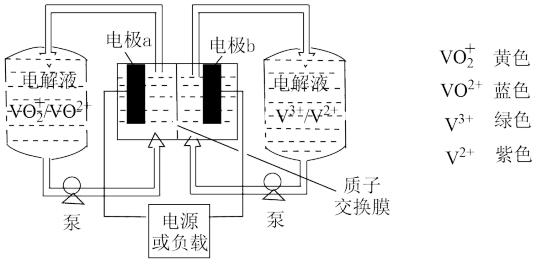
回答下列问题:
(1)钒在元素周期表中的位置是______ ,同周期中的基态原子的电子排布式中,未成对电子数最多的原子的价电子排布式是______ 。
(2)硫酸是铅蓄电池的电解质,在铅蓄电池中负极的电极反应式是________ 。
(3)全钒液流电池放电时,左槽溶液颜色逐渐由黄变蓝,则b电极的反应式是_______ 。若有0.2mol电子转移,质子交换膜左侧电解液质量______ (填“增加”或“减少”)质量为______ 。
(4)全钒液流电池充电时,电极a应连接电源的______ 极,电极反应式为______ 。

回答下列问题:
(1)钒在元素周期表中的位置是
(2)硫酸是铅蓄电池的电解质,在铅蓄电池中负极的电极反应式是
(3)全钒液流电池放电时,左槽溶液颜色逐渐由黄变蓝,则b电极的反应式是
(4)全钒液流电池充电时,电极a应连接电源的
您最近一年使用:0次
解题方法
10 . 由辉铜矿石(主要成分是 )制
)制 的工作原理如图所示。下列说法正确的是
的工作原理如图所示。下列说法正确的是

 )制
)制 的工作原理如图所示。下列说法正确的是
的工作原理如图所示。下列说法正确的是
| A.N极为负极 |
| B.X交换膜为阴离子交换膜 |
C.M极上的电极反应式为: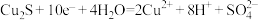 |
| D.该电池工作时温度越高,越有利于加快反应速率 |
您最近一年使用:0次



