解题方法
1 . 某学生利用下面实验装置探究盐桥式原电池的工作原理。
(1)锌电极为电池的___________ 极,电极上发生的是___________ 反应(“氧化”或“还原”),电极反应式为___________ ;铜电极为电池的___________ 极,电极上发生的是___________ 反应(“氧化”或“还原”),电极反应式为___________ 。
(2)导线中电子流向由___________ 流向___________ (用a、b表示)。
(3)若装置中铜电极的质量增加0.64g,则导线中转移的电子的物质的量为___________ ;
(4)若ZnSO4溶液中含有杂质Cu2+,会加速Zn电极的腐蚀、还可能导致电流在较短时间内衰减。欲除去Cu2+,最好选用下列试剂中的___________(填代号)。
(5)反应一段时间后右侧烧杯中Cu2+浓度是___________ (填增大,减小或不变)。
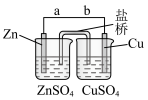
(1)锌电极为电池的
(2)导线中电子流向由
(3)若装置中铜电极的质量增加0.64g,则导线中转移的电子的物质的量为
(4)若ZnSO4溶液中含有杂质Cu2+,会加速Zn电极的腐蚀、还可能导致电流在较短时间内衰减。欲除去Cu2+,最好选用下列试剂中的___________(填代号)。
| A.NaOH | B.Zn | C.Fe | D.H2SO4 |
(5)反应一段时间后右侧烧杯中Cu2+浓度是
您最近半年使用:0次
2 . 氧化还原反应可拆分为氧化和还原两个“半反应”,某小组同学从“半反应”的角度探究反应规律。
(1)已知: 的转化在酸性条件下才能发生。
的转化在酸性条件下才能发生。
①该转化的还原半反应是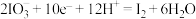 ,则相应的氧化半反应是
,则相应的氧化半反应是___________ 。
②分析上述还原半反应可知:增大 可促进
可促进 得到电子,使其
得到电子,使其___________ 性增强,进而与 发生反应。
发生反应。
(2)探究 与浓盐酸能否发生反应。
与浓盐酸能否发生反应。
①有同学认为 与浓盐酸不能发生反应产生氢气,其依据是
与浓盐酸不能发生反应产生氢气,其依据是___________ 。
用如下装置进行实验【硫酸与浓盐酸中 接近】。
接近】。
②甲实验的目的是___________ 。
③a.丙中气球变鼓是因为生成了___________ 气体(填化学式)。
b.经检测,丙中反应后溶液中存在 。从物质性质角度分析丙中反应能够发生的原因:
。从物质性质角度分析丙中反应能够发生的原因:___________ 。
(3)探究以下原电池的工作原理。
实验结果:产生电流,左侧 电极表面有
电极表面有 析出。
析出。
①该装置中左侧  电极作
电极作___________ (填“正”或“负”)极。
②写出该装置右侧 烧杯中的电极反应式___________ 。
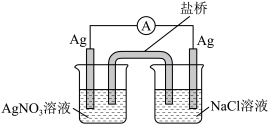
对该原电池的电极反应和总反应的反应类型进行分析,发现两极上分别发生氧化和还原反应,而总反应不一定是氧化还原反应。
③结合上述实验思考,仅由以下实验用品能否设计成原电池__________ 。
 片、
片、 浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
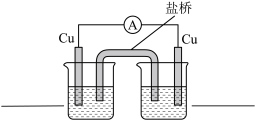
a.若能,在右装置图中填写烧杯中的试剂,并标出电子的移动方向 。
b.若不能,说明原因。
(1)已知:
 的转化在酸性条件下才能发生。
的转化在酸性条件下才能发生。①该转化的还原半反应是
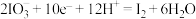 ,则相应的氧化半反应是
,则相应的氧化半反应是②分析上述还原半反应可知:增大
 可促进
可促进 得到电子,使其
得到电子,使其 发生反应。
发生反应。(2)探究
 与浓盐酸能否发生反应。
与浓盐酸能否发生反应。①有同学认为
 与浓盐酸不能发生反应产生氢气,其依据是
与浓盐酸不能发生反应产生氢气,其依据是用如下装置进行实验【硫酸与浓盐酸中
 接近】。
接近】。| 装置 | 序号 | 试管内药品 | 现象 |
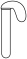 | 甲 | 浓盐酸 | 24小时后仍无明显变化 |
| 乙 |  粉+硫酸 粉+硫酸 | 24小时后仍无明显变化 | |
| 丙 |  粉+浓盐酸 粉+浓盐酸 | 24小时后气球变鼓 |
③a.丙中气球变鼓是因为生成了
b.经检测,丙中反应后溶液中存在
 。从物质性质角度分析丙中反应能够发生的原因:
。从物质性质角度分析丙中反应能够发生的原因:(3)探究以下原电池的工作原理。
实验结果:产生电流,左侧
 电极表面有
电极表面有 析出。
析出。①该装置中
 电极作
电极作②写出该装置

对该原电池的电极反应和总反应的反应类型进行分析,发现两极上分别发生氧化和还原反应,而总反应不一定是氧化还原反应。
③结合上述实验思考,仅由以下实验用品能否设计成原电池
 片、
片、 浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
a.若能,在右装置图中填写烧杯中的试剂,
b.若不能,说明原因。
您最近半年使用:0次
3 . 由辉铜矿石(主要成分是Cu2S)制CuSO4的工作原理如图所示。下列说法不正确的是
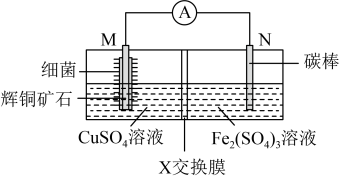

| A.N极为正极 |
| B.X交换膜为阴离子交换膜 |
C.M极上的电极反应式为:Cu2S+10e-+4H2O=2Cu2++8H++ |
| D.该电池工作时在某一温度范围内反应速率最快 |
您最近半年使用:0次
4 . 某化学实验探究小组探究MnO2与某些盐溶液的反应,设计如图装置。左烧杯中加入50mL6mol·L-1硫酸,右烧杯中加入50mL6mol·L-1CaCl2溶液,盐桥选择氯化钾琼脂。当闭合开关K时,电流表中出现指针偏转,下列说法正确的是
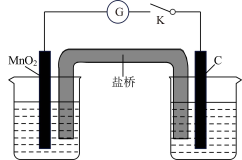
| A.该实验装置属于电解池 |
| B.左侧烧杯中的电极反应为MnO2+4H++2e-=Mn2++2H2O |
| C.右侧C电极上发生还原反应,产生的气体可使湿润的碘化钾淀粉试纸变蓝 |
| D.若将盐桥中氯化钾琼脂换成KNO3琼脂,则C电极上产生的气体的总量增加 |
您最近半年使用:0次
解题方法
5 . 利用光电化学方法将乙二醇( )转化为甲酸盐,同时产生绿色氢气。该装置以NaOH溶液为电解质溶液,工作原理示意图如图所示。已知:实验测定,实际上电路通过0.4mol电子时生成6.8gHCOONa;电解过程中的法拉第效率等于实际甲酸盐量与理论量之比。下列叙述正确的是
)转化为甲酸盐,同时产生绿色氢气。该装置以NaOH溶液为电解质溶液,工作原理示意图如图所示。已知:实验测定,实际上电路通过0.4mol电子时生成6.8gHCOONa;电解过程中的法拉第效率等于实际甲酸盐量与理论量之比。下列叙述正确的是
 )转化为甲酸盐,同时产生绿色氢气。该装置以NaOH溶液为电解质溶液,工作原理示意图如图所示。已知:实验测定,实际上电路通过0.4mol电子时生成6.8gHCOONa;电解过程中的法拉第效率等于实际甲酸盐量与理论量之比。下列叙述正确的是
)转化为甲酸盐,同时产生绿色氢气。该装置以NaOH溶液为电解质溶液,工作原理示意图如图所示。已知:实验测定,实际上电路通过0.4mol电子时生成6.8gHCOONa;电解过程中的法拉第效率等于实际甲酸盐量与理论量之比。下列叙述正确的是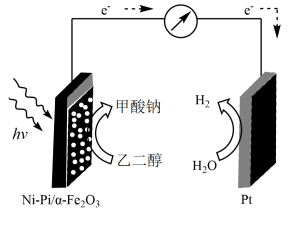
A. 极发生还原反应 极发生还原反应 |
B.装置工作时, 向Pt极迁移 向Pt极迁移 |
C.Pt极反应式为 |
| D.生成HCOONa的法拉第效率为75% |
您最近半年使用:0次
6 . 一种清洁、低成本的三步法氯碱工艺工作原理的示意图如下,下列说法正确的是
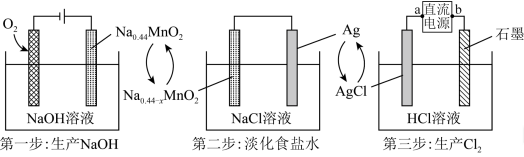
| A.第三步中a为直流电源的正极 |
B.第一步生产 的总反应为 的总反应为 |
| C.第二步为原电池,正极质量增加,负极质量减少 |
| D.第三步外电路上每转移4mol电子,电解池中就有4molHCl被电解 |
您最近半年使用:0次
2024-04-15更新
|
137次组卷
|
2卷引用:河北省金科大联考2023-2024学年高三上学期1月期末质量检测题化学试题
解题方法
7 . 一种电池装置如图所示,它能溶解辉铜矿石(主要成分是Cu2S)制得硫酸铜。下列说法不正确 的是
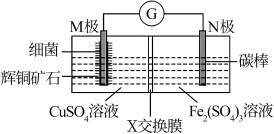
| A.N极为正极 |
| B.X交换膜为阴离子交换膜 |
C.M极产生的Cu2+和SO 的物质的量之比为2:1 的物质的量之比为2:1 |
| D.外电路上每通过2mol电子,左室溶液增重32g |
您最近半年使用:0次
8 . 电解工作原理的实际应用非常广泛。
(1)电解精炼银时,粗银作___________ ,阴极反应为___________ 。
(2)工业上为了处理含有Cr2O 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
(3)某同学设计了如图装置进行以下电化学实验。
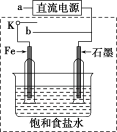
①当开关K与a连接时,两极均有气泡产生,则阴极为___________ 电极。
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为___________ 。请写出此时Fe电极上的电极反应___________ 。
(4)1 L某溶液中含有的离子如下表:
用惰性电极电解该溶液,当电路中有3 mol e-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是___________(填字母)。
(1)电解精炼银时,粗银作
(2)工业上为了处理含有Cr2O
 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。| A.阳极反应:Fe-2e-=Fe2+ | B.阴极反应:2H++2e-=H2↑ |
| C.在电解过程中工业废水由酸性变为碱性 | D.可以将铁电极改为石墨电极 |

①当开关K与a连接时,两极均有气泡产生,则阴极为
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为
(4)1 L某溶液中含有的离子如下表:
| 离子 | Cu2+ | Al3+ | NO | Cl- |
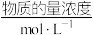 | 1 | 1 | a | 1 |
| A.电解后溶液呈酸性 | B.a=3 |
| C.阳极生成1.5 mol Cl2 | D.阴极析出的金属是铜与铝 |
您最近半年使用:0次
9 . 根据所学知识,回答下列问题。
I.铁片与稀硫酸反应的能量变化特征如图所示:
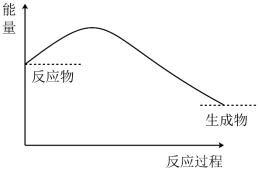
(1)该反应为___________ 反应(填“吸热”或“放热”)。
(2)若要使该反应速率加快,下列措施可行的是___________ (填正确选项的字母编号)。
A.改用铁粉 B.改用98%的硫酸 C.适当升高温度
II.以相同大小铜片和锌片为电极研究水果电池,得到的实验数据如下表所示:
(3)该实验目的是研究水果种类和___________ 对水果电池电流大小的影响。
(4)该实验装置中,正极的材料是___________ ,负极的电极反应式是___________ 。
(5)当有3.25gZn参与反应,转移的电子数目为___________ 。
I.铁片与稀硫酸反应的能量变化特征如图所示:

(1)该反应为
(2)若要使该反应速率加快,下列措施可行的是
A.改用铁粉 B.改用98%的硫酸 C.适当升高温度
II.以相同大小铜片和锌片为电极研究水果电池,得到的实验数据如下表所示:
| 实验编号 | 水果种类 | 电极间距离/cm | 电流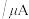 | 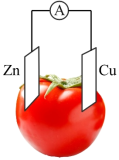 |
| 1 | 番茄 | 1 | 98.7 | |
| 2 | 番茄 | 2 | 72.5 | |
| 3 | 苹果 | 2 | 27.2 |
(4)该实验装置中,正极的材料是
(5)当有3.25gZn参与反应,转移的电子数目为
您最近半年使用:0次
解题方法
10 . 如图所示将锌、铜通过导线相连,置于硫酸溶液中。
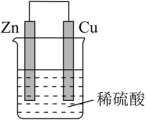
(1)该装置将___________ 能转化为___________ 能。
(2)Zn电极为___________ 极,发生___________ (填“氧化”或“还原”)反应,电极方程式为___________ 。
(3)外电路电流由___________ (填“锌”或“铜”,下同)电极经导线流向___________ 电极。
(4)标准状况下,若反应过程中溶解了6.5g锌,则生成的氢气的体积为___________ L。

(1)该装置将
(2)Zn电极为
(3)外电路电流由
(4)标准状况下,若反应过程中溶解了6.5g锌,则生成的氢气的体积为
您最近半年使用:0次



