名校
解题方法
1 . CH3OH、CO、CH4等都是重要的能源,也是重要的化工原料。
(1)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
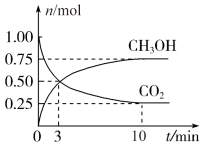
①从反应开始到平衡,CO2的平均反应速率v(CO2)=____ 。
②达到平衡时,H2的浓度为____ mol/L。
(2)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g) CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是____ 。
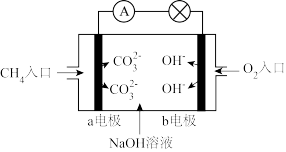
(3)某种甲烷燃料电池的工作原理如图所示氧气通入的一极为电源的____ 极,a电极反应式:____ ,b电极反应式:____ 。
(4)当电路中累计有2 mol电子通过时,消耗的甲烷体积为(在标准状况下)____ L。
(1)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
①从反应开始到平衡,CO2的平均反应速率v(CO2)=
②达到平衡时,H2的浓度为
(2)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g)
 CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是| A.反应中CO与CH3OH的物质的量之比为1:1 |
| B.混合气体的压强不随时间的变化而变化 |
| C.单位时间内每消耗1 mol CO,同时生成1 mol CH3OH |
| D.CH3OH的质量分数在混合气体中保持不变 |
(4)当电路中累计有2 mol电子通过时,消耗的甲烷体积为(在标准状况下)

您最近一年使用:0次
2022-05-12更新
|
436次组卷
|
3卷引用:福建省福州第八中学2021-2022学年高一下学期期末考试化学试题
2 .  的排放与燃烧化石燃料有很大的关系,所以对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
的排放与燃烧化石燃料有很大的关系,所以对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
Ⅰ.脱硝
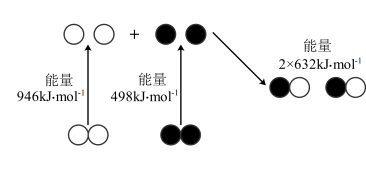
(1)汽车尾气中 生成过程中的能量变化如图所示。
生成过程中的能量变化如图所示。 和
和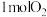 完全反应生成NO会吸收
完全反应生成NO会吸收___________  的能量。
的能量。
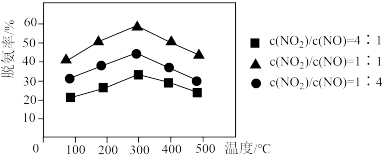
(2) 催化还原氮氧化物(SCR)技术是目前应用最广泛的脱硝技术,用Fe做催化剂时,在氨气足量的情况下,不同
催化还原氮氧化物(SCR)技术是目前应用最广泛的脱硝技术,用Fe做催化剂时,在氨气足量的情况下,不同 对应的脱氨率如图所示,当温度为
对应的脱氨率如图所示,当温度为___________ ℃,
___________ ,脱氮效果最佳。
Ⅱ.脱碳
(3)一定条件下 和
和 反应合成
反应合成 进行脱碳处理,其方程式为:
进行脱碳处理,其方程式为: 。在2L密闭容器中,该反应过程中的部分数据如下表:
。在2L密闭容器中,该反应过程中的部分数据如下表:
①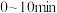 ,以
,以 的浓度变化表示反应的平均速率为
的浓度变化表示反应的平均速率为___________  。
。
②下列情况能说明该反应达到化学平衡状态的是___________ 。
A. 浓度之比为
浓度之比为 B.该密闭容器内压强保持不变
B.该密闭容器内压强保持不变
C.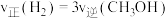 D.该密闭容器内混合气体的密度保持不变
D.该密闭容器内混合气体的密度保持不变
③平衡时, 的体积分数为
的体积分数为___________ (结果保留三位有效数字)。
Ⅲ.脱硫
(4)将 转化为重要的化工原料
转化为重要的化工原料 进行脱硫的原理示意图。
进行脱硫的原理示意图。
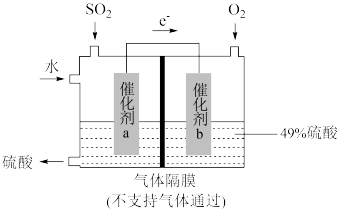
催化剂a表面的电极反应式为___________ ,若得到的硫酸质量分数仍为49%,则理论上参加反应的 与加入的
与加入的 的物质的量之比为
的物质的量之比为___________ 。
 的排放与燃烧化石燃料有很大的关系,所以对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
的排放与燃烧化石燃料有很大的关系,所以对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。Ⅰ.脱硝
(1)汽车尾气中
 生成过程中的能量变化如图所示。
生成过程中的能量变化如图所示。 和
和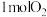 完全反应生成NO会吸收
完全反应生成NO会吸收 的能量。
的能量。
(2)
 催化还原氮氧化物(SCR)技术是目前应用最广泛的脱硝技术,用Fe做催化剂时,在氨气足量的情况下,不同
催化还原氮氧化物(SCR)技术是目前应用最广泛的脱硝技术,用Fe做催化剂时,在氨气足量的情况下,不同 对应的脱氨率如图所示,当温度为
对应的脱氨率如图所示,当温度为

Ⅱ.脱碳
(3)一定条件下
 和
和 反应合成
反应合成 进行脱碳处理,其方程式为:
进行脱碳处理,其方程式为: 。在2L密闭容器中,该反应过程中的部分数据如下表:
。在2L密闭容器中,该反应过程中的部分数据如下表:反应时间/ | 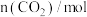 | 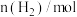 | 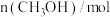 | 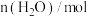 |
| 0 | 3 | 9 | 0 | 0 |
| 10 | 6 | |||
| 20 | 1.5 | |||
| 30 | 1.5 |
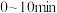 ,以
,以 的浓度变化表示反应的平均速率为
的浓度变化表示反应的平均速率为 。
。②下列情况能说明该反应达到化学平衡状态的是
A.
 浓度之比为
浓度之比为 B.该密闭容器内压强保持不变
B.该密闭容器内压强保持不变C.
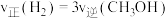 D.该密闭容器内混合气体的密度保持不变
D.该密闭容器内混合气体的密度保持不变③平衡时,
 的体积分数为
的体积分数为Ⅲ.脱硫
(4)将
 转化为重要的化工原料
转化为重要的化工原料 进行脱硫的原理示意图。
进行脱硫的原理示意图。
催化剂a表面的电极反应式为
 与加入的
与加入的 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
名校
解题方法
3 . SO2可形成酸雨,是大气污染物。利用如图装置既可以吸收工厂排放的SO2又可以制得硫酸溶液。下列说法正确的是


| A.a极为负极,发生还原反应 |
B.b极的电极反应式为 |
| C.电子的流动方向:a极→电解质溶液→b极 |
| D.从左下口流出的硫酸溶液的质量分数一定大于50% |
您最近一年使用:0次
2023-07-11更新
|
315次组卷
|
5卷引用:广东省清远市2022-2023学年高一下学期期末质量检测化学试题
名校
解题方法
4 . 某课题研究小组设计如图所示装置(电极材料均为Pt),该装置可将工业废水中的乙胺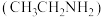 转化为无毒无害物质。下列分析错误的是
转化为无毒无害物质。下列分析错误的是
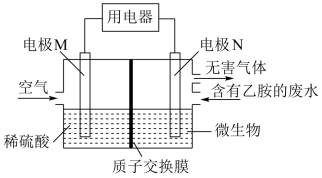
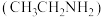 转化为无毒无害物质。下列分析错误的是
转化为无毒无害物质。下列分析错误的是 
| A.电极N为电池的负极 |
B.电池工作时, 由M极区通过交换膜移动到N极区 由M极区通过交换膜移动到N极区 |
C.电极N的电极反应式为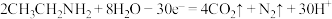 |
| D.当空气(含氧气20%)的进入量为7.5mol时,可以处理含乙胺(质量分数为9%)的废水0.2kg |
您最近一年使用:0次
解题方法
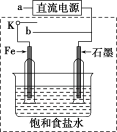
5 . 如图所示,某同学设计一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。

根据要求回答相关问题:
(1)通入氧气的电极为_______ (填“正极”或“负极”),负极的电极反应式为_______ 。
(2)铁电极为_______ (填“阳极”或“阴极”),石墨电极(C)的电极反应式为_______ 。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将_______ (填“增大”“减小”或“不变”)
(4)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为_______ (用 为阿伏加德罗常数的值表示)。
为阿伏加德罗常数的值表示)。
(5)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。
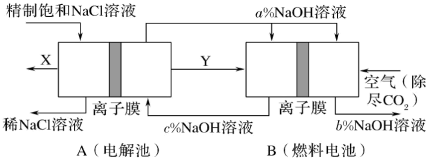
分析图可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为_______ 。

根据要求回答相关问题:
(1)通入氧气的电极为
(2)铁电极为
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将
(4)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为
 为阿伏加德罗常数的值表示)。
为阿伏加德罗常数的值表示)。(5)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。

分析图可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为
您最近一年使用:0次
6 . 电解工作原理的实际应用非常广泛。
(1)电解精炼银时,粗银作___________ ,阴极反应为___________ 。
(2)工业上为了处理含有Cr2O 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
(3)某同学设计了如图装置进行以下电化学实验。
①当开关K与a连接时,两极均有气泡产生,则阴极为___________ 电极。
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为___________ 。请写出此时Fe电极上的电极反应___________ 。
(4)1 L某溶液中含有的离子如下表:
用惰性电极电解该溶液,当电路中有3 mol e-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是___________(填字母)。
(1)电解精炼银时,粗银作
(2)工业上为了处理含有Cr2O
 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。| A.阳极反应:Fe-2e-=Fe2+ | B.阴极反应:2H++2e-=H2↑ |
| C.在电解过程中工业废水由酸性变为碱性 | D.可以将铁电极改为石墨电极 |

①当开关K与a连接时,两极均有气泡产生,则阴极为
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为
(4)1 L某溶液中含有的离子如下表:
| 离子 | Cu2+ | Al3+ | NO | Cl- |
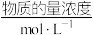 | 1 | 1 | a | 1 |
| A.电解后溶液呈酸性 | B.a=3 |
| C.阳极生成1.5 mol Cl2 | D.阴极析出的金属是铜与铝 |
您最近一年使用:0次
解题方法
7 . 某甲烷燃料电池的构造如图所示,a、b为电极,C、D为选择性离子交换膜,只允许一种离子通过。下列说法正确的是
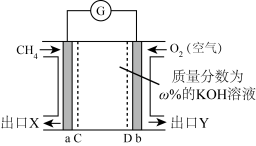

| A.b是电池负极 |
| B.电流由b沿导线流向a,再由a通过电解质溶液流回b |
| C.出口Y中KOH的质量分数小于ω% |
| D.a电极的电极反应式为:CH4−8e-+8OH-=CO2+6H2O |
您最近一年使用:0次
名校
解题方法
8 . 通过传感器可以监测空气中甲醛的含量。一种燃料电池型甲醛气体传感器的原理如图所示,下列说法错误的是
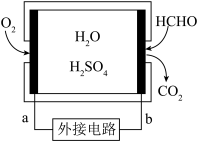
| A.a为电池的正极,发生还原反应 |
| B.b极的电极反应为HCHO+H2O-4e−=CO2+4H+ |
| C.传感器工作过程中,电解质溶液中H+向a极移动 |
| D.外电路中的电流方向为由b到a |
您最近一年使用:0次
2023-09-16更新
|
566次组卷
|
5卷引用:新疆维吾尔自治区喀什第二中学2022-2023学年高二上学期1月期末考试化学试题
新疆维吾尔自治区喀什第二中学2022-2023学年高二上学期1月期末考试化学试题(已下线)专题09 原电池-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)四川省泸县第一中学2023-2024学年高二上学期10月月考化学试题内蒙古自治区优质高中联考2023-2024学年高二上学期11月期中化学试题河南省唐河县鸿唐高级中学2023-2024学年高二上学期10月月考化学试题
9 . 氮氧化物 会参与形成雾霾,通过NOx传感器可监测NOx的含量,其工作原理示意图如下,下列说法不正确的是
会参与形成雾霾,通过NOx传感器可监测NOx的含量,其工作原理示意图如下,下列说法不正确的是

 会参与形成雾霾,通过NOx传感器可监测NOx的含量,其工作原理示意图如下,下列说法不正确的是
会参与形成雾霾,通过NOx传感器可监测NOx的含量,其工作原理示意图如下,下列说法不正确的是
| A.Pt电极发生还原反应 |
B.整个过程的总反应为: |
C.NiO电极的电极反应式为: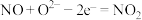 |
| D.装置工作时,电子流动的方向:NiO电极→固体电解质→Pt电极 |
您最近一年使用:0次
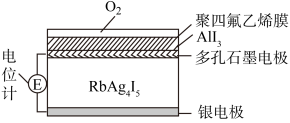
10 . 固体电解质是具有与强电解质水溶液相当的导电性的一类无机物,一种以 晶体为固体电解质的气体含量测定传感器如图所示,固体电解质内迁移的离子为
晶体为固体电解质的气体含量测定传感器如图所示,固体电解质内迁移的离子为 ,氧气流通过该传感器时,
,氧气流通过该传感器时, 可以透过聚四氟乙烯膜进入体系,通过电位计的变化可知
可以透过聚四氟乙烯膜进入体系,通过电位计的变化可知 的含量。下列说法正确的是
的含量。下列说法正确的是
 晶体为固体电解质的气体含量测定传感器如图所示,固体电解质内迁移的离子为
晶体为固体电解质的气体含量测定传感器如图所示,固体电解质内迁移的离子为 ,氧气流通过该传感器时,
,氧气流通过该传感器时, 可以透过聚四氟乙烯膜进入体系,通过电位计的变化可知
可以透过聚四氟乙烯膜进入体系,通过电位计的变化可知 的含量。下列说法正确的是
的含量。下列说法正确的是
| A.银电极为正极,多孔石墨电极为负极 |
B. 透过聚四氟乙烯膜后与 透过聚四氟乙烯膜后与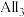 反应生成 反应生成 |
C.银电极的电极反应为: |
D.当传感器内迁移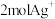 时,有标准状况下 时,有标准状况下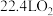 参与反应 参与反应 |
您最近一年使用:0次



