名校
1 . 铁及铁的化合物应用广泛,如氯化铁可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)氯化铁溶液腐蚀印刷电路铜板的离子方程式是_______ 。
(2)若将(1)中的反应设计成原电池,可用____ 作负极,____ 作正极,______ 作电解质溶液。
(3)负极反应式是___________ ,正极反应式是________________ 。
(1)氯化铁溶液腐蚀印刷电路铜板的离子方程式是
(2)若将(1)中的反应设计成原电池,可用
(3)负极反应式是
您最近一年使用:0次
2019-04-03更新
|
269次组卷
|
3卷引用:河南省林州市第一中学2019-2020学年高一3月线上考试化学试题
解题方法
2 . Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。
(1)该电池的负极材料是________ 。电池工作时,电子流向________ (填“正极”或“负极”)。
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是________ 。欲除去Cu2+,最好选用下列试剂中的________ (填代号)。
a.NaOH b.Zn c.Fe d.NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是________ 。若电解电路中通过2 mol电子,MnO2的理论产量为________ 。
(4)用间接电化学法除去NO的过程,如下图所示:
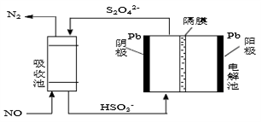
已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式:_____________ 。用离子方程式表示吸收池中除去NO的原理:____________________________________ 。
(1)该电池的负极材料是
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是
a.NaOH b.Zn c.Fe d.NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是
(4)用间接电化学法除去NO的过程,如下图所示:

已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式:
您最近一年使用:0次
2017-12-17更新
|
363次组卷
|
2卷引用:河南省洛阳名校2017-2018学年高二上学期第二次联考化学试题
3 . 已知电池反应Cu + 2FeCl3 == CuCl2 + 2FeCl2,则负极材料是________ ,电极反应式为________________________ ,正极材料是_______ ,电极反应式为________________________ ,电解质为_______________ 。
您最近一年使用:0次
4 . 我国每年产生的废旧铅蓄电池约330万吨。从含铅废料(PbSO4、PbO2、PbO等)中回收铅,实现铅的再生,意义重大。一种回收铅的工作流程如下:

(1)铅蓄电池放电时,PbO2作_______ 极。
(2)过程I,已知:PbSO4、PbCO3的溶解度(20℃)见图l;Na2SO4、Na2CO3的溶解度见图2。

①根据图l写出过程I的离子方程式:____ 。
②生产过程中的温度应保持在40℃,若温度降低,PbSO4的转化速率下降。根据图2,解释可能原因:
i.温度降低,反应速率降低;
ii.__________________________________________ (请你提出一种合理解释)。
(3)过程Ⅱ,发生反应2PbO2+H2C2O4=2PbO+H2O2+2CO2↑。实验中检测到有大量O2放出,推测PbO2氧化了H2O2,通过实验证实了这一推测。实验方案是__________________ 。(已知:PbO2为棕黑色固体;PbO为橙黄色固体)
(4)过程Ⅲ,将PbO粗品溶解在HCI和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液,生成Pb,如图3。阴极的电极反应式是_______________________ 。


(1)铅蓄电池放电时,PbO2作
(2)过程I,已知:PbSO4、PbCO3的溶解度(20℃)见图l;Na2SO4、Na2CO3的溶解度见图2。

①根据图l写出过程I的离子方程式:
②生产过程中的温度应保持在40℃,若温度降低,PbSO4的转化速率下降。根据图2,解释可能原因:
i.温度降低,反应速率降低;
ii.
(3)过程Ⅱ,发生反应2PbO2+H2C2O4=2PbO+H2O2+2CO2↑。实验中检测到有大量O2放出,推测PbO2氧化了H2O2,通过实验证实了这一推测。实验方案是
(4)过程Ⅲ,将PbO粗品溶解在HCI和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液,生成Pb,如图3。阴极的电极反应式是

您最近一年使用:0次
名校
解题方法
5 . 燃料电池是利用燃料(如CO、H2、CH4等)与氧气反应,将反应产生的化学能转变为电能的装置,通常用氢氧化钾作为电解质溶液。完成下列关于甲烷(CH4)燃料电池的填空:
(1)甲烷与氧气反应的化学方程式为:__________ 。
(2)已知燃料电池的总反应式为CH4+2O2+2KOH==K2CO3+3H2O,电池中有一极的电极反应为CH4+10OH--8e-== CO32-+7H2O,这个电极是燃料电池的_________ (填“正极”或“负极”),另一个电极上的电极反应式为:___________ 。
(3)随着电池不断放电,电解质溶液的碱性__________ (填“增大”、“减小”或“不变”)。
(1)甲烷与氧气反应的化学方程式为:
(2)已知燃料电池的总反应式为CH4+2O2+2KOH==K2CO3+3H2O,电池中有一极的电极反应为CH4+10OH--8e-== CO32-+7H2O,这个电极是燃料电池的
(3)随着电池不断放电,电解质溶液的碱性
您最近一年使用:0次
2017-06-29更新
|
216次组卷
|
2卷引用:河南省安阳市第三十六中学2016-2017学年高一5月月考化学试题
名校
6 . 如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液。回答下列问题:

银电极上发生_____ 反应(“氧化”或“还原”),电极反应式为__________ 。

银电极上发生
您最近一年使用:0次
2017-06-22更新
|
210次组卷
|
3卷引用:河南省周口中英文学校2020届高三10月月考化学试题
2014高三·全国·专题练习
名校
7 . 某课外小组分别用下图所示装置对原电池和电解原理进行实验探究.
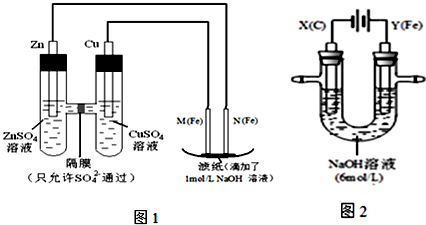
请回答:
I.用图1所示装置进行第一组实验.
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是______ (填字母序号).
A.铝 B.石墨 C.银 D.铂
(2)N极发生反应的电极反应式为_____________ .
(3)实验过程中,SO42-______ (填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有______________ .
II.用图2所示装置进行第二组实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色.
(4)电解过程中,X极区溶液的pH______ (填“增大”、“减小”或“不变”).
(5)电解过程中,Y极发生的电极反应为_____________ 和4OH- - 4e-= 2H2O + O2↑
(6)若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少______ g.
(7)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2 该电池正极发生的反应的电极反应式为__________ .

请回答:
I.用图1所示装置进行第一组实验.
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是
A.铝 B.石墨 C.银 D.铂
(2)N极发生反应的电极反应式为
(3)实验过程中,SO42-
II.用图2所示装置进行第二组实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色.
(4)电解过程中,X极区溶液的pH
(5)电解过程中,Y极发生的电极反应为
(6)若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少
(7)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2 该电池正极发生的反应的电极反应式为
您最近一年使用:0次
2017-06-17更新
|
606次组卷
|
7卷引用:河南省南阳市第一中学校2016-2017学年高二下学期第三次月考化学试题
河南省南阳市第一中学校2016-2017学年高二下学期第三次月考化学试题河南省南阳市第一中学2016-2017学年高二下学期第三次月考化学试题(已下线)2014届高考化学二轮专题复习 电化学练习卷(已下线)2014高考名师推荐化学电解规律及电化学计算北京市2017届高三高考押题卷化学试题2020届高考化学二轮复习大题精准训练 ——原电池、电解池填空题辽宁省沈阳市辽中区第一高级中学2020-2021学年高二下学期开学考试化学试题
名校
8 . (1)某种氢氧燃料电池是用固体金属化物陶瓷作电解质,两极上发生的电极反应分别为:A极:2H2+2O2--4e-=2H2O;B极:O2+4e-=2O2-
则A极是电池的________ 极;电子从该极________ (填“流入”或“流出”)。
(2)有人以化学反应:2Zn+O2+4H+=2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则原电池的负极材料是________ ,发生的电极反应为__________________ 。
(3)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察到锌片上有气泡,再平行插入一块铜片,可观察到铜片上________ (填“有”或“没有”)气泡产生,再用导线把锌片和铜片连接起来,组成一个原电池,正极的电极反应式为____________________ 。
则A极是电池的
(2)有人以化学反应:2Zn+O2+4H+=2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则原电池的负极材料是
(3)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察到锌片上有气泡,再平行插入一块铜片,可观察到铜片上
您最近一年使用:0次
13-14高一下·山东威海·期中
名校
解题方法
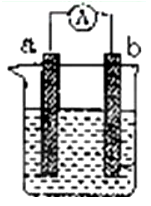
9 . 如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为:___________ 。
(2)当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该装置______ (填“能”或“不能”)
形成原电池,若不能,请说明理由;若能,请指出正、负极材料:__________ 。当反应中收集到标准状况下224mL气体时,消耗的电极质量为________ g。
(3)燃料电池工作原理是将燃料和氧化剂(如O2)反应产生的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,甲烷为燃料,采用氢氧化钠溶液为电解液;则甲烷应通入____ 极(填a或b,下同),电子从____ 极流出,电解质溶液中OH-向____ 极移动。
(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为:
(2)当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该装置
形成原电池,若不能,请说明理由;若能,请指出正、负极材料:
(3)燃料电池工作原理是将燃料和氧化剂(如O2)反应产生的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,甲烷为燃料,采用氢氧化钠溶液为电解液;则甲烷应通入
您最近一年使用:0次
解题方法
10 . 根据下列电化学装置,回答下列问题:
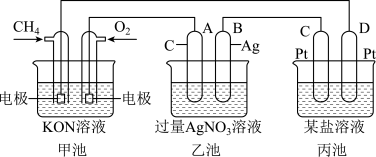
(1)图中甲、乙池的名称:甲池是__________ 装置,乙池是__________ 装置。(填“原电池”或“电解池”)
(2)A(石墨)电极的名称是____________ 。
(3)通入CH4一极的电极反应式为___________________________________ 。
(4)乙池中的电解方程式为___________________________________________ 。
(5)当乙池中B极的质量增加5.4 g时,甲池中理论上消耗O2_____ mL(标准状况下)。此时丙池某电极析出1.6 g某金属,则丙池溶液中的溶质可能是___________ (填序号)。
A.MgSO4 B.CuSO4 C.Na2SO4

(1)图中甲、乙池的名称:甲池是
(2)A(石墨)电极的名称是
(3)通入CH4一极的电极反应式为
(4)乙池中的电解方程式为
(5)当乙池中B极的质量增加5.4 g时,甲池中理论上消耗O2
A.MgSO4 B.CuSO4 C.Na2SO4
您最近一年使用:0次
2017-03-12更新
|
336次组卷
|
2卷引用:河南省郑州励德双语学校2020-2021学年高二上学期期中考试化学试题



