1 . 原电池是将化学能转化为电能的装置,某兴趣小组利用数据采集器和传感器等仪器对原电池进行实验探究。
I.能量变化探究
将上表的现象和结论补充完整
(1)_____________
(2)__________ 、__________
II.原电池电压影响因素的测定
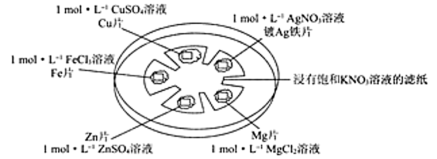
如图所示,在培养皿中进行微型实验,用浸有饱和KNO3溶液的滤纸充当盐桥,在滤纸间隔位置放置金属片,并滴三滴相应溶液,用电压传感器的两个探头分别与不同的金属表面接触形成闭合回路,测定电压。
(3)准确配制一定物质的量浓度的溶液时,操作X应在__________ (填字母)之间。
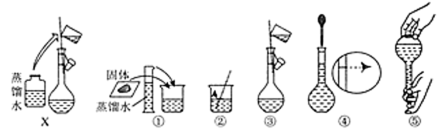
A.②③ B.③④ C.④⑤
(4)以上五种金属的活动性由活泼到不活泼的顺序为_________________ 。
(5)实验条件下,连接不同金属片时所得数据见下表,表中Y极代表__________ (填“正”或“负”)极,预测表中Ag和Zn相连接时,测得电压的数值a可能的范围为____________ ;Fe和Mg相连接时,Z极的电极反应式为__________ ,Y极的电极反应式为____________ 。
I.能量变化探究
| 实验操作 | 数据及图象 | 现象与结论 |
| 将60mL1mol/LCuSO4溶液置于100mL烧杯中,向其中加入1g镁粉 | 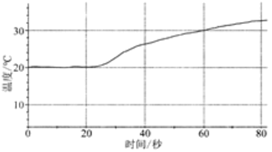 | (1)反应过程中,化学能直接转化为 能; |
| 将60mL1mol/LCuSO4溶液置于100mL烧杯中,平行插入铜片和镁片,与电流传感器形成闭合回路 | 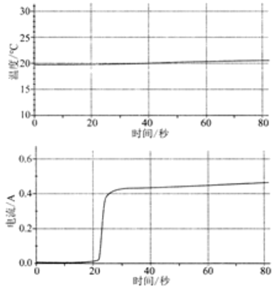 | (2)体系温度变化很小,原因是 ;反应过程中,镁片和铜片的质量变化分别为: ; |
(1)
(2)
II.原电池电压影响因素的测定
如图所示,在培养皿中进行微型实验,用浸有饱和KNO3溶液的滤纸充当盐桥,在滤纸间隔位置放置金属片,并滴三滴相应溶液,用电压传感器的两个探头分别与不同的金属表面接触形成闭合回路,测定电压。

(3)准确配制一定物质的量浓度的溶液时,操作X应在

A.②③ B.③④ C.④⑤
(4)以上五种金属的活动性由活泼到不活泼的顺序为
(5)实验条件下,连接不同金属片时所得数据见下表,表中Y极代表
| Y极 | Z极 | 测得电压/V |
| Ag | Fe | 1.009 |
| Ag | Zn | a |
| Ag | Mg | 2.114 |
| Fe | Zn | 0.473 |
| Fe | Mg | 1.111 |
| Zn | Mg | 0.636 |
您最近一年使用:0次
解题方法
2 . 随着社会的发展 ,环境问题越来越受到人们的关注。请回答下列相关问题。
I.汽车尾气中含有 CO、NO 等有害气体 ,某新型催化剂能促使 NO、CO 转化为 2 种无毒气体。T℃时,将 0.8 molNO 和 0. 8molCO 充入容积为 2L 的密闭容器中,模拟尾气转化,容器中 NO 物质的量随时间变化如图所示 。
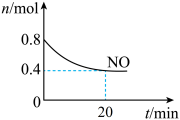
(1)将NO、CO转化为2种无毒气体的化学方程式是___________________ 。
(2)反应开始至20min,v (NO) =_________ mol/ (L• min) 。
(3)下列说法正确的是__________ 。
a.新型催化剂可以加快 NO、CO的转化
b.该反应进行到 20 min 时达到化学平衡状态
c.平衡时CO的浓度是 0.4 mol/ L
d.混合气体的总压强不随时间的变化而变化说明上述反应达到平衡状态
e.保持容器体积不变,充入 He 增大压强,反应速率加快
II我国最近在太阳能光电催化— 化学耦合分解硫化氢研究中获得新进展 ,相关装置如图所示。
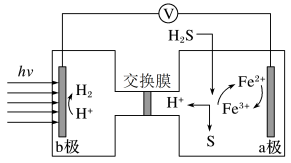
(1)负极为_________ 极(填“ a” 或“ b” ) 发生的电极反应式为______________ 。
(2)为使电池持续放电 ,交换膜需选用___________ 交换膜(填“阳离子” 或“阴离子”或“质子”)。
(3)分解硫化氢的离子方程式为_______________________ 。
I.汽车尾气中含有 CO、NO 等有害气体 ,某新型催化剂能促使 NO、CO 转化为 2 种无毒气体。T℃时,将 0.8 molNO 和 0. 8molCO 充入容积为 2L 的密闭容器中,模拟尾气转化,容器中 NO 物质的量随时间变化如图所示 。

(1)将NO、CO转化为2种无毒气体的化学方程式是
(2)反应开始至20min,v (NO) =
(3)下列说法正确的是
a.新型催化剂可以加快 NO、CO的转化
b.该反应进行到 20 min 时达到化学平衡状态
c.平衡时CO的浓度是 0.4 mol/ L
d.混合气体的总压强不随时间的变化而变化说明上述反应达到平衡状态
e.保持容器体积不变,充入 He 增大压强,反应速率加快
II我国最近在太阳能光电催化— 化学耦合分解硫化氢研究中获得新进展 ,相关装置如图所示。

(1)负极为
(2)为使电池持续放电 ,交换膜需选用
(3)分解硫化氢的离子方程式为
您最近一年使用:0次
2020-07-26更新
|
289次组卷
|
2卷引用:河南省驻马店市2019-2020学年高一下学期期末考试化学试题
名校
解题方法
3 . 某同学用如图所示做水果电池的实验,测得数据如下表所示:
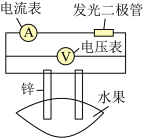
请回答以下问题:
(1)实验⑥中负极的电极反应式为_____________ 。
(2)实验①、⑤中电流方向相反的原因是_________ 。
(3)若在实验中发光二极管不亮,该同学用铜、锌作电极,用菠萝作介质,并将多个此电池串联起来,再接发光二极管,这样做________ (填“合理”或“不合理”)。

实验编号 | 电极材料 | 水果品种 | 电极间距/cm | 电压/mV | |
① | 锌 | 铜 | 菠萝 | 3 | 900 |
② | 锌 | 铜 | 苹果 | 3 | 650 |
③ | 锌 | 铜 | 柑橘 | 3 | 850 |
④ | 锌 | 铜 | 西红柿 | 3 | 750 |
⑤ | 锌 | 铜 | 菠萝 | 3 | 650 |
⑥ | 锌 | 铜 | 苹果 | 3 | 450 |
(1)实验⑥中负极的电极反应式为
(2)实验①、⑤中电流方向相反的原因是
(3)若在实验中发光二极管不亮,该同学用铜、锌作电极,用菠萝作介质,并将多个此电池串联起来,再接发光二极管,这样做
您最近一年使用:0次
名校
解题方法
4 . X、Y、Z、W、Q是原子序数依次增大的短周期主族元素,X与Y位于不同周期,X与W位于同一主族;原子最外层电子数之比N(Y):N(Q)=3:4;Z的原子序数等于Y、W、Q三种元素原子的最外层电子数之和。请回答下列问题:
(1)Y元素在周期表中的位置是______________ ;QX4的电子式为_____________ 。
(2)一种名为“PowerTrekk”的新型充电器是以化合物W2Q和X2Z为原料设计的,这两种化合物相遇会反应生成W2QZ3和气体X2,利用气体X2组成原电池提供能量。
①写出W2Q和X2Z反应的化学方程式:______________ 。
②以稀硫酸为电解质溶液,向两极分别通入气体X2和Z2可形成原电池,其中通入气体X2的一极是_______ (填“正极”或“负极”)。
③若外电路有3mol电子转移,则理论上需要W2Q的质量为_________ 。
(1)Y元素在周期表中的位置是
(2)一种名为“PowerTrekk”的新型充电器是以化合物W2Q和X2Z为原料设计的,这两种化合物相遇会反应生成W2QZ3和气体X2,利用气体X2组成原电池提供能量。
①写出W2Q和X2Z反应的化学方程式:
②以稀硫酸为电解质溶液,向两极分别通入气体X2和Z2可形成原电池,其中通入气体X2的一极是
③若外电路有3mol电子转移,则理论上需要W2Q的质量为
您最近一年使用:0次
2019-11-19更新
|
147次组卷
|
2卷引用:河南省南阳市一中2020届高三上期第五次月考化学试题
名校
5 . 《我在故宫修文物》这部纪录片里关于古代青铜器的修复引起了某研学小组的兴趣。“修旧如旧”是文物保护的主旨。
(1)查阅高中教材得知铜锈为Cu2(OH)2CO3,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值。参与形成铜绿的物质有Cu和_______ 。
(2)继续查阅中国知网,了解到铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。考古学家将铜锈分为无害锈和有害锈,结构如图所示:
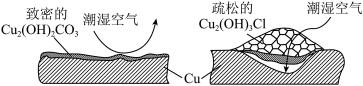
Cu2(OH)2CO3和Cu2(OH)3Cl分别属于无害锈和有害锈,请解释原因_____________ 。
(3)文献显示有害锈的形成过程中会产生CuCl(白色不溶于水的固体),请结合下图回答:
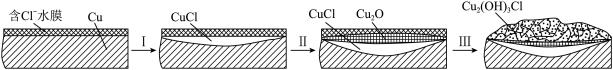
① 过程Ⅰ的正极反应物是___________ 。
② 过程Ⅰ负极的电极反应式是_____________ 。
(4)青铜器的修复有以下三种方法:
ⅰ.柠檬酸浸法:将腐蚀文物直接放在2%-3%的柠檬酸溶液中浸泡除锈;
ⅱ.碳酸钠法:将腐蚀文物置于含Na2CO3的缓冲溶液中浸泡,使CuCl转化为难溶的Cu2(OH)2CO3;
ⅲ.BTA保护法:
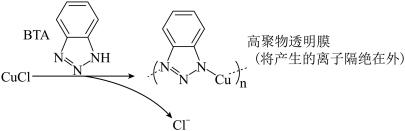
请回答下列问题:
①写出碳酸钠法的离子方程式___________________ 。
②三种方法中,BTA保护法应用最为普遍,分析其可能的优点有___________ 。
A.在青铜器表面形成一层致密的透明保护膜
B.替换出锈层中的Cl-,能够高效的除去有害锈
C.和酸浸法相比,不破坏无害锈,可以保护青铜器的艺术价值,做到“修旧如旧”
(1)查阅高中教材得知铜锈为Cu2(OH)2CO3,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值。参与形成铜绿的物质有Cu和
(2)继续查阅中国知网,了解到铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。考古学家将铜锈分为无害锈和有害锈,结构如图所示:

Cu2(OH)2CO3和Cu2(OH)3Cl分别属于无害锈和有害锈,请解释原因
(3)文献显示有害锈的形成过程中会产生CuCl(白色不溶于水的固体),请结合下图回答:

① 过程Ⅰ的正极反应物是
② 过程Ⅰ负极的电极反应式是
(4)青铜器的修复有以下三种方法:
ⅰ.柠檬酸浸法:将腐蚀文物直接放在2%-3%的柠檬酸溶液中浸泡除锈;
ⅱ.碳酸钠法:将腐蚀文物置于含Na2CO3的缓冲溶液中浸泡,使CuCl转化为难溶的Cu2(OH)2CO3;
ⅲ.BTA保护法:

请回答下列问题:
①写出碳酸钠法的离子方程式
②三种方法中,BTA保护法应用最为普遍,分析其可能的优点有
A.在青铜器表面形成一层致密的透明保护膜
B.替换出锈层中的Cl-,能够高效的除去有害锈
C.和酸浸法相比,不破坏无害锈,可以保护青铜器的艺术价值,做到“修旧如旧”
您最近一年使用:0次
2019-06-11更新
|
1879次组卷
|
7卷引用:中国人民大学附属中学2019届高三考前热身练习化学试题



