名校
1 . 有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6mol/L的H2SO4溶液中,乙同学将电极放入6mol/L的NaOH溶液中,如图所示。 移向
移向___________ (填“铝片”或“镁片”),写出甲中正极的电极反应式___________ 。
(2)乙中负极为___________ (填“铝片”或“镁片”),写出正极的电极反应式式:___________ 。
(3)铅蓄电池中,正极材料为PbO2,负极材料为Pb,电解液为硫酸,放电时其正极反应式为___________ 。
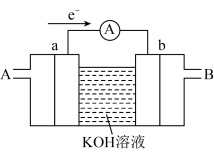
(4)如图为氢氧燃料电池的工作原理示意图,a、b均为惰性电极。___________ 口通入(填“A”或“B”)。电流由___________ 流向___________ (填“a”或“b”)。其总反应方程式为___________ ,在碱性条件下,负极反应式为___________ 。
(5)直接乙醇燃料电池( )具有很多优点。现有以下三种乙醇燃料电池。
)具有很多优点。现有以下三种乙醇燃料电池。___________ 。
②酸性乙醇燃料电池中,电极a上发生的电极反应式为___________ 。
③熔融碳酸盐乙醇燃料电池中,电极b上发生的电极反应式为___________ 。
(6)某同学设计如图的原电池,负极实验现象为___________ ,则正极的电极反应式为:___________ ,当导线中有3.01×1023个电子流过,溶液质量变化为___________ g。

 移向
移向(2)乙中负极为
(3)铅蓄电池中,正极材料为PbO2,负极材料为Pb,电解液为硫酸,放电时其正极反应式为
(4)如图为氢氧燃料电池的工作原理示意图,a、b均为惰性电极。
(5)直接乙醇燃料电池(
 )具有很多优点。现有以下三种乙醇燃料电池。
)具有很多优点。现有以下三种乙醇燃料电池。
②酸性乙醇燃料电池中,电极a上发生的电极反应式为
③熔融碳酸盐乙醇燃料电池中,电极b上发生的电极反应式为
(6)某同学设计如图的原电池,负极实验现象为

您最近一年使用:0次
2024-04-24更新
|
303次组卷
|
2卷引用:四川省凉山州宁南中学2023-2024学年高一下学期半期模拟考试化学试题
解题方法
2 . 如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
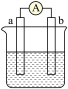
(1)当电极a为Zn,电极b为Cu,电解质溶液为CuSO4溶液时,正极的电极反应式为_______ 。若初始时两电极质量相等,当电路中有2mole-通过时,两极的质量差为_________ g。
(2)当电极a为Al,电极b为Mg,电解质溶液为NaOH溶液时,该电池的负极反应式为______ 。当反应中收集到标准状况下336mL气体时,消耗负极的物质的量为________ mol。

(1)当电极a为Zn,电极b为Cu,电解质溶液为CuSO4溶液时,正极的电极反应式为
(2)当电极a为Al,电极b为Mg,电解质溶液为NaOH溶液时,该电池的负极反应式为
您最近一年使用:0次
解题方法
3 . 水果电池是利用水果中的化学物质和金属片发生反应产生电能制作的一种电池。水果电池的发电原理:两种金属片的活泼性不一样,较活泼的金属能与水果中酸性物质的氢离子反应,从而形成原电池。水果电池的电流及电压大小与电极材料、电极间距、果酸浓度等有关。甲、乙两位同学一起做了水果电池的实验,测得数据如下:
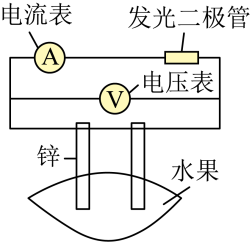
试根据上表中的实验数据回答下列问题:
(1)实验2中负极是___________ ,电极反应式为___________ 。
(2)实验1和5电流方向相反的原因是___________ 。
(3)由实验1~4可知影响水果电池的电压的因素是___________ 。
(4)通过实验2、6和实验1、5的比较可发现水果电池的电压还与___________ 有关。

| 实验编号 | 电极材料 | 水果品种 | 电极间距/cm | 电压/mV | |
| 1 | 锌 | 铜 | 菠萝 | 3 | 900 |
| 2 | 锌 | 铜 | 苹果 | 3 | 650 |
| 3 | 锌 | 铜 | 柑橘 | 3 | 850 |
| 4 | 锌 | 铜 | 西红柿 | 3 | 750 |
| 5 | 锌 | 铝 | 菠萝 | 3 | 650 |
| 6 | 锌 | 铝 | 苹果 | 3 | 450 |
(1)实验2中负极是
(2)实验1和5电流方向相反的原因是
(3)由实验1~4可知影响水果电池的电压的因素是
(4)通过实验2、6和实验1、5的比较可发现水果电池的电压还与
您最近一年使用:0次
名校
解题方法
4 . 丙烷作为奥运火炬的燃料,价格低廉,燃烧后只生成二氧化碳和水,不会对环境造成污染。丙烷燃烧产生的火焰呈亮黄色,比较醒目。
已知:①某些常见化学键的键能数据如下。
②
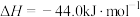 。
。
(1)写出表示丙烷燃烧热的热化学方程式:_______ ;该反应中反应物的总能量_______ (填“>”、“<”或“=”)的生成物的总能量。
(2)丙烷的爆炸极限窄,故其为比较理想的便携式燃料电池的燃料。以丙烷为燃料的固体氧化物(能传导 )燃料电池的结构示意图如图。该电池利用催化剂对正、负极气体选择催化性的差异而产生电势差进行工作。
)燃料电池的结构示意图如图。该电池利用催化剂对正、负极气体选择催化性的差异而产生电势差进行工作。
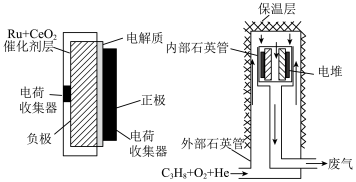
①电池工作时,丙烷在_______ (填“正”或“负”)极上发生_______ (填“氧化”或“还原”)反应,电极反应式为_______ 。
②电池工作时,丙烷会与氧气反应转化成合成气(成分为CO和 )而造成电能损失。若1mol丙烷先完全转化成合成气后再发生电极反应,则电能损失率为
)而造成电能损失。若1mol丙烷先完全转化成合成气后再发生电极反应,则电能损失率为_______ %,总反应消耗氧气的物质的量_______ (填“增大”、“减小”或“不变”)。
已知:①某些常见化学键的键能数据如下。
| 化学键 |  |  |  |  |  |
键能 | 803 | 463 | 348 | 413 | 497 |

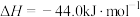 。
。(1)写出表示丙烷燃烧热的热化学方程式:
(2)丙烷的爆炸极限窄,故其为比较理想的便携式燃料电池的燃料。以丙烷为燃料的固体氧化物(能传导
 )燃料电池的结构示意图如图。该电池利用催化剂对正、负极气体选择催化性的差异而产生电势差进行工作。
)燃料电池的结构示意图如图。该电池利用催化剂对正、负极气体选择催化性的差异而产生电势差进行工作。
①电池工作时,丙烷在
②电池工作时,丙烷会与氧气反应转化成合成气(成分为CO和
 )而造成电能损失。若1mol丙烷先完全转化成合成气后再发生电极反应,则电能损失率为
)而造成电能损失。若1mol丙烷先完全转化成合成气后再发生电极反应,则电能损失率为
您最近一年使用:0次
2023-12-12更新
|
352次组卷
|
6卷引用:河南省创新发展联盟2023-2024学年高二上学期第四次联考化学试题
河南省创新发展联盟2023-2024学年高二上学期第四次联考化学试题陕西省西安市2023-2024学年高三上学期12月联考化学试卷河北省邢台市部分重点高中2023-2024学年高二上学期1月期末化学试题(已下线)专题07 原电池-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)吉林省白山市抚松县第一中学2023-2024学年高二上学期12月月考化学试题江苏省盐城市射阳中学2023-2024学年高二上学期1月期末化学试题
2023高三·全国·专题练习
解题方法
5 . 我国科学家研究Li-CO2电池,取得了重大科研成果。回答下列问题:
(1)Li-CO2电池中,Li为单质锂片,则该电池中的CO2在_______ (填“正”或“负”)极发生电化学反应。研究表明,该电池反应产物为碳酸锂和单质碳,且CO2电还原后与锂离子结合形成碳酸锂按以下4个步骤进行,写出步骤Ⅲ的离子方程式
Ⅰ.2CO2+2e-=C2O
Ⅱ.C2O =CO2+CO
=CO2+CO
Ⅲ._______
Ⅳ.CO +2Li+=Li2CO3
+2Li+=Li2CO3
(2)研究表明,在电解质水溶液中,CO2气体可被电化学还原。CO2在碱性介质中电还原为正丙醇(CH3CH2CH2OH)的电极反应方程式为_______ 。
(1)Li-CO2电池中,Li为单质锂片,则该电池中的CO2在
Ⅰ.2CO2+2e-=C2O

Ⅱ.C2O
 =CO2+CO
=CO2+CO
Ⅲ.
Ⅳ.CO
 +2Li+=Li2CO3
+2Li+=Li2CO3(2)研究表明,在电解质水溶液中,CO2气体可被电化学还原。CO2在碱性介质中电还原为正丙醇(CH3CH2CH2OH)的电极反应方程式为
您最近一年使用:0次
2023高三·全国·专题练习
6 . 为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
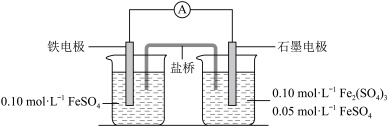
回答下列问题:
(1)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据表中数据,盐桥中应选择_____ 作为电解质。
(2)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入______ 电极溶液中。
(3)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02mol•L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=______ 。
(4)根据(2)、(3)实验结果,可知石墨电极的电极反应式为_____ ,铁电极的电极反应式为______ 。因此,验证了Fe2+氧化性小于______ 、还原性小于______ 。

回答下列问题:
(1)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据表中数据,盐桥中应选择
| 阳离子 | u∞×108/(m2•s-1•V-1) | 阴离子 | u∞×108/(m2•s-1•V-1) |
| Li+ | 4.07 | HCO | 4.61 |
| Na+ | 5.19 | NO | 7.40 |
| Ca2+ | 6.59 | Cl- | 7.91 |
| K+ | 7.62 | SO | 8.27 |
(3)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02mol•L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=
(4)根据(2)、(3)实验结果,可知石墨电极的电极反应式为
您最近一年使用:0次
解题方法
7 . 写出下列原电池装置中各部分的作用并分析其电极反应和离子移动方向.
原电池装置 | 各部分作用 | 电极反应 | 离子移动方向 |
|  : : : :稀硫酸: | 负极: | |
| 正极: | |||
|  : : : : 溶液: 溶液: 溶液: 溶液:盐桥: | 负极: | |
| 正极: | |||
| 石墨: : : : : 溶液: 溶液: | 负极: | |
| 正极: |
您最近一年使用:0次
解题方法
8 . 一种简单的原电池装置示意图如图所示。请据图回答下列问题。
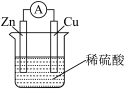
(1)锌是该电池的____ (填“正”或“负”)极。
(2)装置中锌的作用是____ ,稀硫酸的作用是____ 。
A.电极材料 B.电极反应物 C.电子导体 D.离子导体
(3)从化学的角度分析,该装置能产生电流的原因是____ 。

(1)锌是该电池的
(2)装置中锌的作用是
A.电极材料 B.电极反应物 C.电子导体 D.离子导体
(3)从化学的角度分析,该装置能产生电流的原因是
您最近一年使用:0次
23-24高一上·全国·假期作业
解题方法
9 . I.有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol·L-1的H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如图所示。
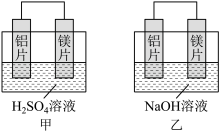
(1)写出甲中正极的电极反应式:_______
(2)乙中负极为_______ , 总反应的离子方程式:_______
(3)由此实验得出的下列结论中,正确的有_______
II.利用反应Cu+2FeCl3=CuCl2+2FeCl2设计成如图所示原电池,回答下列问题:
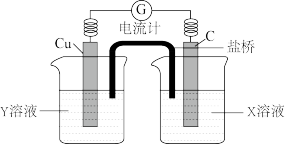
(4)写出电极反应式:正极_______ ;负极_______ 。
(5)图中X溶液是_______ ,Y溶液是_______ 。

(1)写出甲中正极的电极反应式:
(2)乙中负极为
(3)由此实验得出的下列结论中,正确的有_______
| A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质 |
| B.镁的金属性不一定比铝的金属性强 |
| C.该实验说明金属活动性顺序表已过时,没有实用价值了 |
| D.该实验说明化学研究对象复杂、反应受条件影响较大,因此应具体问题具体分析 |
II.利用反应Cu+2FeCl3=CuCl2+2FeCl2设计成如图所示原电池,回答下列问题:

(4)写出电极反应式:正极
(5)图中X溶液是
您最近一年使用:0次
解题方法
10 . Ⅰ.研原电池是化学对人类的一项重大贡献。
(1)如图是甲烷燃料电池原理示意图,回答下列问题:
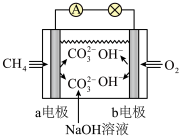
①电池的负极是_______ (填“a”或“b”)电极,该极的电极反应式为_______
②电池工作一段时间后电解质溶液的pH_______ (填 “增大”、“减小”或“不变”)。
(2)熔融盐燃料电池具有很高的发电效率,因而受到重视。可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650℃下工作的燃料电池。请完成有关的电池反应式:
负极反应式:2CO+2 —4e—=4CO2;
—4e—=4CO2;
正极反应式:_______ ,总电池反应式:_______
Ⅱ.“神舟九号”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。
(3)飞船在光照区运行时,太阳能电池帆板将太阳能转化为电能,除供给飞船使用外,多余部分用镉镍蓄电池储存起来。其工作原理为Cd+2NiO(OH)+2H2O Cd(OH)2 +2Ni(OH)2;当飞船运行到阴影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性
Cd(OH)2 +2Ni(OH)2;当飞船运行到阴影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性 _______ (填“增大”“减小”或“不变”)。
(4)紧急状况下,应急电池会自动启动,工作原理为Zn+Ag2O+H2O 2Ag+ Zn(OH)2,负极的电极反应式为
2Ag+ Zn(OH)2,负极的电极反应式为_______ 。
(1)如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是
②电池工作一段时间后电解质溶液的pH
(2)熔融盐燃料电池具有很高的发电效率,因而受到重视。可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650℃下工作的燃料电池。请完成有关的电池反应式:
负极反应式:2CO+2
 —4e—=4CO2;
—4e—=4CO2;正极反应式:
Ⅱ.“神舟九号”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。
(3)飞船在光照区运行时,太阳能电池帆板将太阳能转化为电能,除供给飞船使用外,多余部分用镉镍蓄电池储存起来。其工作原理为Cd+2NiO(OH)+2H2O
 Cd(OH)2 +2Ni(OH)2;当飞船运行到阴影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性
Cd(OH)2 +2Ni(OH)2;当飞船运行到阴影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性 (4)紧急状况下,应急电池会自动启动,工作原理为Zn+Ag2O+H2O
 2Ag+ Zn(OH)2,负极的电极反应式为
2Ag+ Zn(OH)2,负极的电极反应式为
您最近一年使用:0次






