名校
1 . 浓差电池是一种利用电解质溶液浓度差产生电势差而形成的电池,理论上当电解质溶液的浓度相等时停止放电。图1为浓差电池,图2为电渗析法制备磷酸二氢钠,用浓差电池为电源完成电渗析法制备磷酸二氢钠。下列说法正确的是
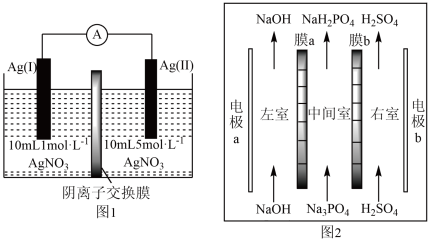
| A.电极Ag(II)的电极反应式为:Ag-e-=Ag+ |
| B.电渗析装置中膜a、b均为阳离子交换膜 |
| C.电渗析过程中左室中NaOH浓度增大,右室H2SO4的浓度减小 |
| D.电池从开始到停止放电,理论上可制备2.4gNaH2PO4 |
您最近一年使用:0次
2024-03-11更新
|
273次组卷
|
2卷引用:四川省成都外国语学校2023-2024学年高三上学期期末考试理科综合试题-高中化学
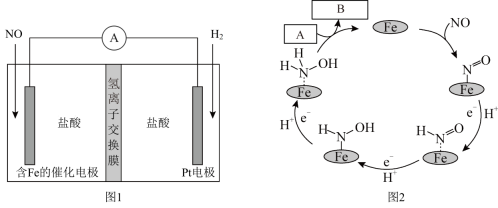
2 . 盐酸羟胺(化学式为NH3OHCl,其中N为 价)是一种常见的还原剂和显像剂,其化学性质类似NH4Cl。工业上主要采用如图1所示的方法制备,其电池装置中含Fe的催化电极的电极反应机理如图2所示。下列说法错误的是
价)是一种常见的还原剂和显像剂,其化学性质类似NH4Cl。工业上主要采用如图1所示的方法制备,其电池装置中含Fe的催化电极的电极反应机理如图2所示。下列说法错误的是
 价)是一种常见的还原剂和显像剂,其化学性质类似NH4Cl。工业上主要采用如图1所示的方法制备,其电池装置中含Fe的催化电极的电极反应机理如图2所示。下列说法错误的是
价)是一种常见的还原剂和显像剂,其化学性质类似NH4Cl。工业上主要采用如图1所示的方法制备,其电池装置中含Fe的催化电极的电极反应机理如图2所示。下列说法错误的是
| A.含Fe的催化电极为正极 |
| B.图2中,A为H+,B为NH3OH+ |
| C.电池工作时,每消耗2.24L NO(标准状况下),左室溶液质量增加3.0g |
| D.电池工作时,H+从右室穿过氢离子交换膜向左室迁移 |
您最近一年使用:0次
名校
解题方法
3 . 盐酸羟胺(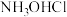 )是一种常见的还原剂和显像剂,其化学性质类似
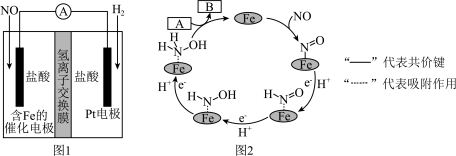
)是一种常见的还原剂和显像剂,其化学性质类似 。工业上主要采用图1所示的方法制备。电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
。工业上主要采用图1所示的方法制备。电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
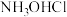 )是一种常见的还原剂和显像剂,其化学性质类似
)是一种常见的还原剂和显像剂,其化学性质类似 。工业上主要采用图1所示的方法制备。电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
。工业上主要采用图1所示的方法制备。电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
| A.电池工作时,Pt电极作正极 |
B.图2中,A为 和 和 ,B为 ,B为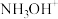 |
| C.电池工作时,每消耗2.24LNO(标准状况下),左室溶液质量增加3.3g |
D.Pt电极发生的电极方程式为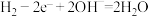 |
您最近一年使用:0次
名校
解题方法
4 . 乙炔制乙烯是煤化工路线的重要途径之一,如图是利用电化学装置制备 的工作原理示意图,下列说法正确的是
的工作原理示意图,下列说法正确的是
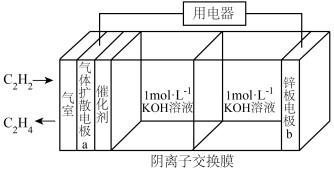
 的工作原理示意图,下列说法正确的是
的工作原理示意图,下列说法正确的是
| A.电极电势:a极<b极 |
| B.电子移动方向:电极b→用电器→电极a→KOH溶液→电极b |
C.电极a上的电极反应式为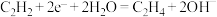 |
| D.放电一段时间后,正极室溶液pH不会发生变化 |
您最近一年使用:0次
2024-01-31更新
|
106次组卷
|
2卷引用:河南省南阳市桐柏县实验高中2024届高三上学期阶段检测化学试题(12月)
5 . 锌铜——稀硫酸原电池的装置如图所示,下列叙述错误的是
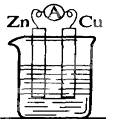

| A.电流从锌片经导线流向铜片 | B.锌是负极,其质量逐渐减小 |
| C.氢离子在铜表面被还原,产生气泡 | D.依据该实验现象可判断锌比铜活泼 |
您最近一年使用:0次
2018-07-04更新
|
114次组卷
|
2卷引用:【全国市级联考】湖北省襄阳市2017-2018学年高一下学期期末调研统一考试化学试题
2023高三上·全国·专题练习
6 . 膜技术原理在化工生产中有着广泛的应用。有人设想利用电化学原理制备少量硫酸和绿色硝化剂 ,装置图如下。下列说法不正确的是
,装置图如下。下列说法不正确的是
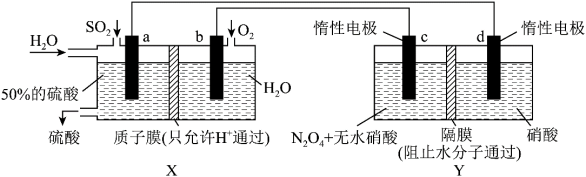
 ,装置图如下。下列说法不正确的是
,装置图如下。下列说法不正确的是
A. 是原电池 是原电池 |
B. 池能够生产 池能够生产 |
C.电路中电子流向为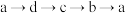 ,形成闭合回路 ,形成闭合回路 |
D. 、 、 中 中 均从左边迁移到右边 均从左边迁移到右边 |
您最近一年使用:0次
名校
解题方法
7 . 我国科学家设计可同时实现, 制备和海水淡化的新型电池,装置意图如图,下列说法
制备和海水淡化的新型电池,装置意图如图,下列说法不正确 的是
 制备和海水淡化的新型电池,装置意图如图,下列说法
制备和海水淡化的新型电池,装置意图如图,下列说法
| A.电极a是正极 |
B.电极b的反应式: |
C.每生成 ,有 ,有 发生迁移 发生迁移 |
| D.离子交换膜c、d分别是阴离子交换膜和阳离子交换膜 |
您最近一年使用:0次
2023-12-11更新
|
347次组卷
|
2卷引用: 北京市第五中学2023-2024学年高二上学期12月月考化学试题
名校
解题方法
8 . 环氧乙烷( )可用于生产乙二醇。电化学合成环氧乙烷(
)可用于生产乙二醇。电化学合成环氧乙烷( )的装置如图所示:
)的装置如图所示:

已知:
| A.Pt电极接电源正极 |
| B.制备1mol环氧乙烷,Ni电极区产生2molH2 |
| C.Pt电极区的反应方程式为:CH2=CH2+Br2+H2O→HOCH2CH2Br |
| D.电解完成后,将阳极区和阴极区溶液混合才可得到环氧乙烷 |
您最近一年使用:0次
名校
9 . 盐酸羟胺( )是一种常见的还原剂,工业上采用如图1所示方法利用NO制备盐酸羟胺,图2是用图1的电池处理含Cl-,
)是一种常见的还原剂,工业上采用如图1所示方法利用NO制备盐酸羟胺,图2是用图1的电池处理含Cl-, 的酸性废水的装置。下列说法正确的是
的酸性废水的装置。下列说法正确的是
 )是一种常见的还原剂,工业上采用如图1所示方法利用NO制备盐酸羟胺,图2是用图1的电池处理含Cl-,
)是一种常见的还原剂,工业上采用如图1所示方法利用NO制备盐酸羟胺,图2是用图1的电池处理含Cl-, 的酸性废水的装置。下列说法正确的是
的酸性废水的装置。下列说法正确的是
| A.图2电解池工作时a电极应与Pt电极相连 |
B.处理1mol ,电路中转移5mole- ,电路中转移5mole- |
| C.电池工作时,每消耗2.24 L(标准状况下)NO,左室溶液质量增加3.3g |
| D.电池工作一段时间后,正负极区溶液的pH均下降 |
您最近一年使用:0次
2024-02-01更新
|
336次组卷
|
2卷引用:江西省宜春市第一中学2023-2024学年高三上学期1月质量检测化学试题
名校
10 . 为探究原电池的形成条件和反应原理,某同学设计了如下实验并记录了现象:
① 向一定浓度的稀硫酸中插入锌片,看到有气泡生成;
② 向上述稀硫酸中插入铜片,没有看到有气泡生成;
③ 将锌片与铜片上端用导线连接,一起插入稀硫酸中,看到铜片上有气泡生成,且生成气泡的速率比实验①中快
④ 在锌片和铜片中间接上电流计,再将锌片和铜片插入稀硫酸中,发现电流计指针偏转。
下列关于以上实验设计及现象的分析,不正确 的是
① 向一定浓度的稀硫酸中插入锌片,看到有气泡生成;
② 向上述稀硫酸中插入铜片,没有看到有气泡生成;
③ 将锌片与铜片上端用导线连接,一起插入稀硫酸中,看到铜片上有气泡生成,且生成气泡的速率比实验①中快
④ 在锌片和铜片中间接上电流计,再将锌片和铜片插入稀硫酸中,发现电流计指针偏转。
下列关于以上实验设计及现象的分析,
| A.实验①、②说明锌能与稀硫酸反应产生氢气,而铜不能 |
| B.实验③说明发生原电池反应时会加快化学反应速率 |
| C.实验③说明在该条件下铜可以与稀硫酸反应生成氢气 |
| D.实验④说明该装置可形成原电池 |
您最近一年使用:0次



