名校
解题方法
1 . 碱性锌锰电池以氢氧化钾溶液为电解液,电池总反应方程式为Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s),下列说法正确的是
| A.Zn作负极,失去电子 |
| B.电池工作时,MnO2得电子被氧化 |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.理论上,锌的质量减小6.5g,通过外电路的电子为0.2mol |
您最近一年使用:0次
2020-08-04更新
|
530次组卷
|
2卷引用:山东省2019-2020学年高一下学期期末联考化学试题
解题方法
2 . 下列原电池在工作时,铜电极有电流流入的是
A.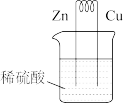 | B.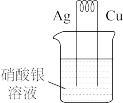 |
C.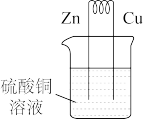 | D.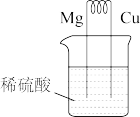 |
您最近一年使用:0次
名校
解题方法
3 . 如图装置,电流表G发生偏转,a极逐渐变粗,同时b极逐渐变细,c为电解质溶液, 则a、b、c可能是下列各组中的( )
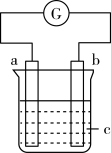

| A.a是Ag、b是Cu、c为Cu(NO3)2溶液 |
| B.a是Ag、b是Fe、c为AgNO3溶液 |
| C.a是Zn、b是Cu、c为稀H2SO4溶液 |
| D.a是Cu、b是Zn、c为稀H2SO4溶液 |
您最近一年使用:0次
2020-08-02更新
|
602次组卷
|
9卷引用:山东省实验中学2019-2020学年高一下学期4月线上考试化学试题
山东省实验中学2019-2020学年高一下学期4月线上考试化学试题福建省莆田第二十四中学2019-2020学年高一化学下学期期中测试卷甘肃省张掖市高台县第一中学2019-2020学年高一下学期期中考试化学试题甘肃省庆阳市第一中学2019-2020学年高一下学期期中考试化学试题黑龙江省齐齐哈尔三立高级中学有限公司2020-2021学年高二上学期开学考试化学试题安徽省六安市新安中学2020-2021学年高二下学期入学考试(普通班)化学试题河北省张家口宣化一中2020-2021学年高一下学期4月月考化学试题广东省茂名化州市第一中学2021-2022学年高一下学期期中考试化学试题江苏省盐城市东台创新高级中学2021-2022学年高一5月份月检测化学试题
4 . 我国科学家研制一种新型化学电池成功实现废气的处理和能源的利用,用该新型电池电解CuSO4溶液,装置如下(H2R和R都是有机物)。下列说法正确的是
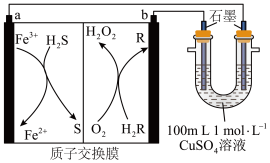

| A.b电极反应式为R+2H++2e-=H2R |
| B.电池工作时,负极区要保持呈酸性 |
| C.工作一段时间后,正极区的pH变大 |
| D.若消耗标准状况下112mLO2,则电解后的CuSO4溶液pH约为2 |
您最近一年使用:0次
2020-07-31更新
|
587次组卷
|
3卷引用:山东省烟台市2019-2020学年高二下学期期末考试化学试题
5 . 能源的开发和利用是当前科学研究的重要课题。
(1)原电池是将_____ 能转化为_____ 能的装置。
(2)下列不能用于设计成原电池的化学反应是_____ ,理由是_____ 。
A.2HCl+CaO=CaCl2+H2O
B.2CH3OH+3O2=2CO2+4H2O
C.4Fe(OH)2+2H2O+O2=4Fe(OH)3
D.2H2+O2=2H2O
(3)甲烷是天然气的主要成分。
①写出CH4燃烧的化学方程式_____ 。
②25℃,100kPa时生成或断裂1mol化学键所放出或吸收的能量称为键能。已知键能数据如下:
计算1mol甲烷完全燃烧放出的热量为_____ kJ。
(4)为提高能量转化效率,常将甲烷设计成燃料电池,装置示意图如图(其中A、B为石墨电极)。
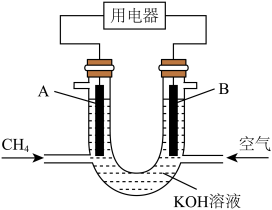
①B是该电池的_____ (填“正”或“负”)极。CH4在该装置中的作用是_____ ,KOH溶液的作用是_____ 。
②已知甲烷与氧气完全氧化时每生成1mol液态水释放能量约为400kJ,又知该甲烷燃料电池每发1kW·h电能生成216g水,则该电池的能量转化率为_____ (1kW·h=3.6×106J)。
(1)原电池是将
(2)下列不能用于设计成原电池的化学反应是
A.2HCl+CaO=CaCl2+H2O
B.2CH3OH+3O2=2CO2+4H2O
C.4Fe(OH)2+2H2O+O2=4Fe(OH)3
D.2H2+O2=2H2O
(3)甲烷是天然气的主要成分。
①写出CH4燃烧的化学方程式
②25℃,100kPa时生成或断裂1mol化学键所放出或吸收的能量称为键能。已知键能数据如下:
| 化学键 | C-H | O=O | C=O | O-H |
| 键能/kJ·mol-1 | 414 | 497 | 803 | 463 |
(4)为提高能量转化效率,常将甲烷设计成燃料电池,装置示意图如图(其中A、B为石墨电极)。

①B是该电池的
②已知甲烷与氧气完全氧化时每生成1mol液态水释放能量约为400kJ,又知该甲烷燃料电池每发1kW·h电能生成216g水,则该电池的能量转化率为
您最近一年使用:0次
2020-07-31更新
|
193次组卷
|
2卷引用:山东省烟台市2019-2020学年高一下学期期末考试化学试题
解题方法
6 . 铁镍蓄电池又称爱迪生电池,放电时的总反应为Fe+Ni2O3+3H2O = Fe(OH)2+Ni(OH)2。下列关于该电池的说法错误的是
| A.Fe为负极 | B.Ni2O3发生还原反应 |
| C.不能使用酸溶液作电解液 | D.该电池放电时化学能全部转换为电能 |
您最近一年使用:0次
解题方法
7 . 化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是( )
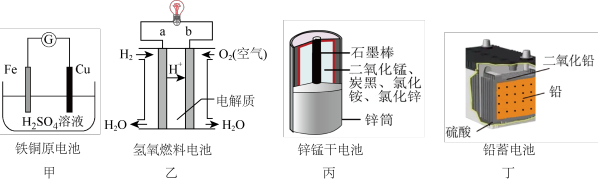

| A.甲:可用Zn电极代替Cu电极作正极 |
| B.乙:通入氧气的一极为正极 |
| C.丙:锌筒作负极,发生氧化反应,锌筒会变薄 |
| D.丁:原电池Pb+PbO2+2H2SO4=2PbSO4+2H2O中,PbO2发生还原反应作正极 |
您最近一年使用:0次
名校
解题方法
8 . 用特殊电极材料制作的新型二次电池,放电时发生如下图所示的电极反应,下列说法正确的是
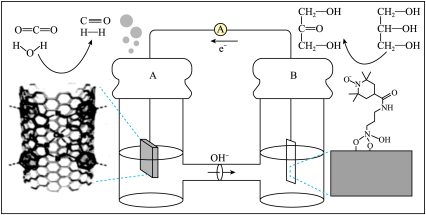

| A.A为原电池的负极,失去电子,发生氧化反应 |
| B.B上发生的电极反应为CH2OH(CHOH)CH2OH—2e-=CH2OHCOCH2OH+2H+ |
C.若通过交换膜的离子是HCO ,则B上发生的电极反应为CH2OH(CHOH)CH2OH—2e-+2HCO ,则B上发生的电极反应为CH2OH(CHOH)CH2OH—2e-+2HCO =CH2OHCOCH2OH+2H2O+2CO2 =CH2OHCOCH2OH+2H2O+2CO2 |
| D.若A处产生的CO和H2的物质的量之比为1:3,则B处消耗丙三醇的物质的量为4mol |
您最近一年使用:0次
2020-07-17更新
|
557次组卷
|
2卷引用:山东省日照市2020届高三6月校际联合考试化学试题
名校
9 . 某种浓差电池的装置如图所示,碱液室中加入电石渣浆液[主要成分为Ca(OH)2],酸液室通入CO2(以NaCl为支持电解质),产生电能的同时可生产纯碱等物质。下列叙述错误的是
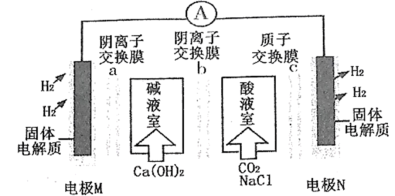

| A.电子由电极M经外电路流向电极N |
| B.在碱液室可以生成NaHCO3、Na2CO3 |
| C.放电一段时间后,酸液室溶液pH减小,碱液室pH增大 |
| D.Cl-通过阴离子交换膜b移向碱液室,H+通过质子交换膜c移向N极 |
您最近一年使用:0次
2020-07-16更新
|
315次组卷
|
2卷引用:山东省烟台市2019-2020学年高二下学期期中考试化学试题
10 . 反应Fe+Fe2(SO4)3=3FeSO4的能量变化趋势如图所示:
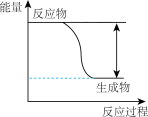
(1)该反应为_____ (填“吸热”或“放热”)反应。
(2)若要使该反应的反应速率加快,下列措施可行的是_____ (填字母)。
A.改铁片为铁粉 B.升高温度 C.减小压强 D.加入适量的Na2SO4固体
(3)若将上述反应设计成原电池,且铜为此原电池的某一电极材料,则铜为____ (填“正”或“负”)极。Fe电极上发生的电极反应为_____ ,溶液中的阳离子向______ (填“正”或“负”)极移动。

(1)该反应为
(2)若要使该反应的反应速率加快,下列措施可行的是
A.改铁片为铁粉 B.升高温度 C.减小压强 D.加入适量的Na2SO4固体
(3)若将上述反应设计成原电池,且铜为此原电池的某一电极材料,则铜为
您最近一年使用:0次



