解题方法
1 . 某化学兴趣小组的几位同学探究原电池原理的应用时,做了如图的实验:
(1)甲同学利用打磨过的铜片和铝片设计了如图的实验装置,并测量和绘制了原电池的电流(I)随时间(t)的变化曲线(极短时间电流反转),则图中t1时刻之后阶段,负极材料是___________ 。
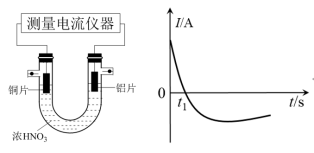
II.铜与浓硝酸反应探究
(2)乙同学将铜片直接放入浓硝酸中:
①实验现象为___________ ,溶液显绿色。
②待反应停止后,若铜有剩余,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,原因是___________ (用离子方程式表示)。
(3)电化学降解NO 的原理如图所示。
的原理如图所示。
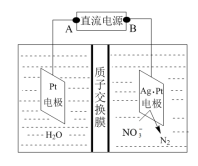
电源正极为___________ (填“A”或“B”),阳极的电极反应式为___________ 。若电解过程中转移了2mol电子,则膜两侧电极液的质量变化差(△m左-△m右)为___________ 。
(1)甲同学利用打磨过的铜片和铝片设计了如图的实验装置,并测量和绘制了原电池的电流(I)随时间(t)的变化曲线(极短时间电流反转),则图中t1时刻之后阶段,负极材料是

II.铜与浓硝酸反应探究
(2)乙同学将铜片直接放入浓硝酸中:
①实验现象为
②待反应停止后,若铜有剩余,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,原因是
(3)电化学降解NO
 的原理如图所示。
的原理如图所示。
电源正极为
您最近一年使用:0次
名校
2 . 根据要求,回答下列问题:
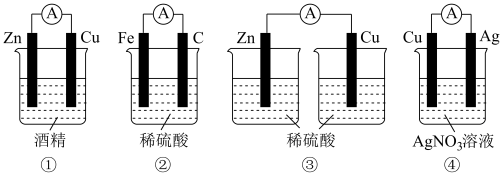
I.把化学能转化为电能的装置叫做原电池。_______ 。
(2)装置④中,正极材料是_______ ;负极的电极反应式为_______ ;电池工作时,总反应的离子方程式为_______ ;烧杯中 向
向_______ 电极移动(填“Cu”或“Ag”);导线中电子的流动方向为_______ (填“Cu到Ag”或“Ag到Cu”)。
II.某同学利用铁与盐酸的反应,探究影响反应速率的因素(实验所用铁的质量相等且铁块的形状相同,盐酸均过量),实验设计如下:
(1)若四组实验均以收集到448mL(标准状况)氢气为标准,则上述实验中还需要测定的数据是_______ 。
(2)实验1和2是探究_______ 对该反应速率的影响。实验_______ 和_______ 是探究温度对该反应速率的影响。
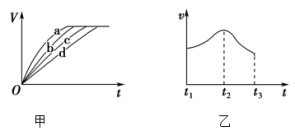
(3)不同时间t产生的氢气体积V如图甲所示,曲线c对应的实验编号是_______ 。每一组实验中产生氢气的速率v随时间t变化的曲线如图乙所示,其中t1~t2速率变化的主要原因是_______ 。______ 。
I.把化学能转化为电能的装置叫做原电池。
(2)装置④中,正极材料是
 向
向II.某同学利用铁与盐酸的反应,探究影响反应速率的因素(实验所用铁的质量相等且铁块的形状相同,盐酸均过量),实验设计如下:
| 实验编号 | 盐酸浓度/( ) ) | 铁的状态 | 温度/K |
| 1 | 2.00 | 块状 | 293 |
| 2 | 4.00 | 块状 | 293 |
| 3 | 4.00 | 粉末 | 293 |
| 4 | 4.00 | 块状 | 313 |
(2)实验1和2是探究
(3)不同时间t产生的氢气体积V如图甲所示,曲线c对应的实验编号是
您最近一年使用:0次
3 . 如图是氢氧燃料电池构造图。关于该电池说法不正确的是


| A.a极是负极 |
| B.电子由a通过灯泡流向b |
C.正极的电极反应是: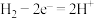 |
| D.氢氧燃料电池是环保电池 |
您最近一年使用:0次
解题方法
4 . 下列关于如图所示装置的叙述,错误的是
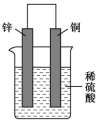

| A.锌失电子被氧化 | B.铜片表面有气泡产生 |
| C.电流从锌片经导线流向铜片 | D.电子从锌片经导线流向铜片 |
您最近一年使用:0次
解题方法
5 . 液体锌电池具有成本低、安全性强等特点,其工作原理如图所示(KOH凝胶中允许离子存在、生成或迁移)。下列说法正确的是
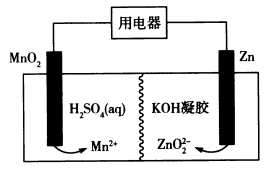

| A.电流由MnO2极经用电器流向Zn极 |
B.负极反应式为 |
| C.工作一段时间后,锌极区pH升高 |
| D.13.0 gZn参与反应,理论上电路中转移0.2 mol电子 |
您最近一年使用:0次
解题方法
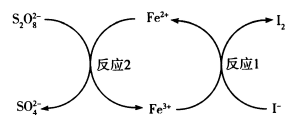
6 . 实验发现加入M能提高 和I-的反应速率,其原理如图所示,依次发生反应1、2,下列说法正确的是
和I-的反应速率,其原理如图所示,依次发生反应1、2,下列说法正确的是
 和I-的反应速率,其原理如图所示,依次发生反应1、2,下列说法正确的是
和I-的反应速率,其原理如图所示,依次发生反应1、2,下列说法正确的是
| A.M可能是Fe(OH)3 |
| B.Fe2+是该反应的催化剂 |
| C.反应1为2Fe3++2I-=2Fe2++I2 |
D.将反应2设计成原电池, 在负极反应 在负极反应 |
您最近一年使用:0次
名校
解题方法
7 . 写出下列原电池的电极反应式
①用金属Mg和Al做电极,HCl溶液做电解质溶液组成原电池,经测定Mg为负极,写出Al电极的电极反应式:_______ 。
②用金属Mg和Al做电极,NaOH溶液做电解质溶液组成原电池,经测定Mg为正极,写出Al电极的电极反应式:_______ 。
①用金属Mg和Al做电极,HCl溶液做电解质溶液组成原电池,经测定Mg为负极,写出Al电极的电极反应式:
②用金属Mg和Al做电极,NaOH溶液做电解质溶液组成原电池,经测定Mg为正极,写出Al电极的电极反应式:
您最近一年使用:0次
名校
8 . 原电池是化学对人类的一项重大贡献。某兴趣小组为研究原电池原理,设计了如图所示装置。
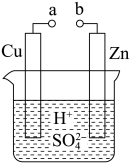
a和b用导线连接,Cu极为原电池___________ (填“正”或“负”)极,电极反应式为___________ ;锌片上的电极反应式为___________ ,溶液中 移向
移向___________ (填“Cu”或“Zn”)极。

a和b用导线连接,Cu极为原电池
 移向
移向
您最近一年使用:0次
2021-07-21更新
|
263次组卷
|
3卷引用:吉林省长春市第二十九中学2020-2021学年高一下学期期末考试化学试题
解题方法
9 . 铅蓄电池工作原理如下图所示,在电池工作时 ,电极发生反应,
,电极发生反应,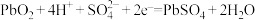 ,下列说法不正确的是
,下列说法不正确的是
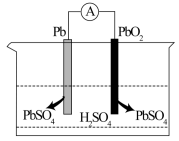
 ,电极发生反应,
,电极发生反应,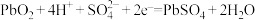 ,下列说法不正确的是
,下列说法不正确的是
A.该电极反应中 是氧化剂 是氧化剂 |
| B.铅蓄电池是二次电池 |
C.放电时,电子由 电极经 电极经 溶液回到Pb电极 溶液回到Pb电极 |
| D.该电池放电过程中,正、负极转移电子相等 |
您最近一年使用:0次
10 . 铜锌原电池如图所示,电解质溶液为硫酸铜。下列说法错误的是
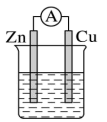

| A.锌电极将逐渐被腐蚀 |
| B.铜电极为正极,发生氧化反应 |
C.铜电极上的反应为: |
| D.电子从锌电极经过导线流向铜电极 |
您最近一年使用:0次
2021-07-20更新
|
306次组卷
|
3卷引用:福建省宁德市2020-2021学年高一下学期期末考试化学试题
福建省宁德市2020-2021学年高一下学期期末考试化学试题江苏省连云港市赣榆智贤中学2021-2022学年高二上学期第一次月考化学试题(已下线)第34练 原电池-2023年高考化学一轮复习小题多维练(全国通用)



