名校
解题方法
1 .  是大气污染物,造成酸雨的主要原因,用如图所示装置可以既吸收工厂排放的废气中的
是大气污染物,造成酸雨的主要原因,用如图所示装置可以既吸收工厂排放的废气中的 ,又可以生成一定量的硫酸,下列说法不正确的是( )
,又可以生成一定量的硫酸,下列说法不正确的是( )
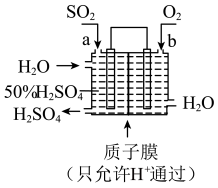
 是大气污染物,造成酸雨的主要原因,用如图所示装置可以既吸收工厂排放的废气中的
是大气污染物,造成酸雨的主要原因,用如图所示装置可以既吸收工厂排放的废气中的 ,又可以生成一定量的硫酸,下列说法不正确的是( )
,又可以生成一定量的硫酸,下列说法不正确的是( )
| A.a为负极,b为正极 |
| B.从左下口流出的硫酸的质量分数一定大于50% |
| C.生产过程中氢离子由左移向右 |
| D.负极反应式为SO2+2H2O-2e-=SO42—+4H+ |
您最近一年使用:0次
解题方法
2 . 某监测SO2含量的传感器工作原理如图所示(其中固体电解质允许O2-发生迁移)。下列说法正确的是( )


| A.传感器的内外电路中,电流均是由电子定向移动形成的 |
| B.传感器工作时,Pt电极上的电极反应式为:O2+4e-+2H2O=4OH- |
| C.传感器工作时,O2-向负极移动 |
| D.固体电解质可以用稀硫酸代替 |
您最近一年使用:0次
2020-11-24更新
|
366次组卷
|
2卷引用:浙江省温州十五校联合体2020-2021学年高二上学期期中联考化学试题
名校
3 . 按照要求回答下列问题。
(1)工业上,在强碱性条件下用电解法除去废水中的CN-,装置如图所示,依次发生的反应有:
i.CN--2e-+2OH-=CNO-+H2O
ii.2Cl--2e-=Cl2↑
iii.3Cl2+2CNO-+8OH-=N2+6Cl-+2 +4H2O
+4H2O

①除去1molCN-,外电路中至少需要转移________ mol电子。
②为了使电解池连续工作,需要不断补充_________ 。
(2)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示(电极材料为石墨)。

①图中a极要连接电源的________ (填“正”或“负”)极,C口流出的物质是________ 。
② 放电的电极反应式为
放电的电极反应式为__________ 。
(3)用零价铁(Fe)去除水体中的硝酸盐( )已成为环境修复研究的热点之一。Fe还原水体中的
)已成为环境修复研究的热点之一。Fe还原水体中的 的反应原理如图所示。
的反应原理如图所示。

①作负极的物质是________ 。
②正极的电极反应式是_____________ 。
(4)通过NOx传感器可监测NOx的含量,其工作原理示意图如图所示。

①Pt电极上发生的是________ 反应(填“氧化”或“还原”)。
②写出NiO电极的电极反应式:________________ 。
(1)工业上,在强碱性条件下用电解法除去废水中的CN-,装置如图所示,依次发生的反应有:
i.CN--2e-+2OH-=CNO-+H2O
ii.2Cl--2e-=Cl2↑
iii.3Cl2+2CNO-+8OH-=N2+6Cl-+2
 +4H2O
+4H2O
①除去1molCN-,外电路中至少需要转移
②为了使电解池连续工作,需要不断补充
(2)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示(电极材料为石墨)。

①图中a极要连接电源的
②
 放电的电极反应式为
放电的电极反应式为(3)用零价铁(Fe)去除水体中的硝酸盐(
 )已成为环境修复研究的热点之一。Fe还原水体中的
)已成为环境修复研究的热点之一。Fe还原水体中的 的反应原理如图所示。
的反应原理如图所示。
①作负极的物质是
②正极的电极反应式是
(4)通过NOx传感器可监测NOx的含量,其工作原理示意图如图所示。

①Pt电极上发生的是
②写出NiO电极的电极反应式:
您最近一年使用:0次
4 . 锂一氧化铜电池是一种新型绿色电池。它的比能量高、电压高、工作温度宽,使用寿命长,适合于大电流、重负载放电应用。回答下列问题:
(1)通过如下过程制备CuO:

①写出“氧化”时生成CuSO4的离子反应方程式:_______ 。
②“沉铜”时,将Na2CO3溶液加入CuSO4溶液中时,研究二者不同物质的量之比与产品纯度的关系(用铜元素的含量来表示产品的纯度),结果如图所示。

已知:Cu2(OH)2CO3中铜元素的含量为57.7%,二者比值为1:0.8时,产品中可能含有的杂质是____ [填“Cu(OH)2”或“CuCO3”]。
③“灼烧”时反应的化学方程式是______ 。
(2)锂-氧化铜电池以LiClO4有机溶液为电解质溶液,电池总反应为2Li+CuO=Li2O+Cu,其工作原理示意图如图。

①正极反应式为_______ 。
②每转移0.2 mol e-,理论上消耗Li的质量为_______ 。
(1)通过如下过程制备CuO:

①写出“氧化”时生成CuSO4的离子反应方程式:
②“沉铜”时,将Na2CO3溶液加入CuSO4溶液中时,研究二者不同物质的量之比与产品纯度的关系(用铜元素的含量来表示产品的纯度),结果如图所示。

已知:Cu2(OH)2CO3中铜元素的含量为57.7%,二者比值为1:0.8时,产品中可能含有的杂质是
③“灼烧”时反应的化学方程式是
(2)锂-氧化铜电池以LiClO4有机溶液为电解质溶液,电池总反应为2Li+CuO=Li2O+Cu,其工作原理示意图如图。

①正极反应式为
②每转移0.2 mol e-,理论上消耗Li的质量为
您最近一年使用:0次
名校
解题方法
5 . 通过NO传感器可监测NO的含量,其工作原理如图所示。下列说法错误的是
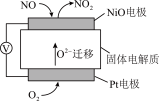

| A.Pt电极为该电池正极 |
| B.外电路中,电子从NiO电极流出 |
| C.Pt电极的电极反应为O2+ 4e-=2O2- |
| D.当有2.24 L NO参与反应时,转移了0.2 mol电子 |
您最近一年使用:0次
2020-12-24更新
|
286次组卷
|
5卷引用:重庆市第八中学校2020-2021学年高二上学期期中考试化学试题
解题方法
6 . 固体电解质可以通过离子迁移传递电荷,利用固体电解质RbAg4I5可以制成电化学气敏传感器,其中迁移的物种全是Ag+。下图是一种测定O2含量的气体传感器示意图,O2可以透过聚四氟乙烯薄膜,根据电池电动势变化可以测得O2的含量。在气体传感器工作过程中,下列有关说法正确的是
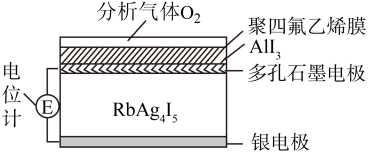

| A.银电极被消耗,RbAg4I5的量增多 |
| B.电位计读数越大,O2含量越高 |
| C.负极反应为Ag+I--e-= AgI |
| D.部分A1I3同体变为Al和AgI |
您最近一年使用:0次
2020-04-22更新
|
427次组卷
|
2卷引用:安徽省合肥市2020年高三第二次教学质量检测(全国I卷)理综化学试题
解题方法
7 . 2019年化学诺贝尔奖授予拓展锂离子电池应用的三位科学家。如图是某锂—空气充电电池的工作原理示意图,下列叙述正确的是


| A.电解质溶液可选用可溶性锂盐的水溶液 |
| B.电池放电时间越长,Li2O2含量越少 |
| C.电池工作时,正极可发生Li++O2-e- = LiO2 |
| D.充电时,b端应接负极 |
您最近一年使用:0次
名校
解题方法
8 . 电化学气敏传感器可用于监制环境中 NH3的含量,其工作原理示意图如图所示,下列说法不正确的是( )


| A.电池工作一段时间后pH将变大 |
| B.反应消耗的NH3与O2的物质的量之比为4:3 |
| C.负极的电极反应式为2NH36e6OHN26H2O |
| D.电流方向:电极b→导线→电极a→电解质溶液→电极b |
您最近一年使用:0次
2020-07-16更新
|
90次组卷
|
2卷引用:湖南省长沙市明德中学2019-2020学年高一下学期第八次阶段性检测化学试题
18-19高一下·江西南昌·阶段练习
名校
解题方法
9 . 电化学气敏传感器可用于监测环境中NH3 的含量,其工作原理(如图)与原电池的工作原理类似

(1)b为正极,发生_________ 反应(填“氧化”或“还原”);
(2)溶液中的OH-_________ 向极移动(填“a”或“b”);
(3)负极的电极反应式为__________

(1)b为正极,发生
(2)溶液中的OH-
(3)负极的电极反应式为
您最近一年使用:0次
名校
解题方法
10 . A、B、C、D、E是原子序数依次递增的五种常见元素。A、B元素组成的气态化合物M的水溶液呈碱性,C元素是地壳中含量最多的元素,D的单质在C的单质中燃烧后的产物可以使品红溶液褪色,E是金属元素。
(1)写出A、C两种元素组成的化合物A2C2的电子式_______ 。
(2)若将E金属投入盐酸中,生成了浅绿色溶液N。则N的酸性溶液与A2C2反应的离子方程式为______________________________________ 。
(3)R是B的氧化物,通常情况下呈红棕色。现有一试管R,欲使元素B全部转化为它的最高价氧化物对应的水化物,故进行如下实验操作:将盛有R的试管倒扣在水槽中,______ 。
(4)有人设想寻求合适的催化剂和电极材料,以A2、B2为电极反应物,以HCl—NH4Cl溶液为电解质溶液制造新型燃料电池,试写出该电池的正极反应式_____________ ,放电时,溶液中的H+移向_________ (填正极或负极)。
(1)写出A、C两种元素组成的化合物A2C2的电子式
(2)若将E金属投入盐酸中,生成了浅绿色溶液N。则N的酸性溶液与A2C2反应的离子方程式为
(3)R是B的氧化物,通常情况下呈红棕色。现有一试管R,欲使元素B全部转化为它的最高价氧化物对应的水化物,故进行如下实验操作:将盛有R的试管倒扣在水槽中,
(4)有人设想寻求合适的催化剂和电极材料,以A2、B2为电极反应物,以HCl—NH4Cl溶液为电解质溶液制造新型燃料电池,试写出该电池的正极反应式
您最近一年使用:0次



