解题方法
1 . 资料显示,水溶液中 与
与 发生互促水解生成蓝色沉淀
发生互促水解生成蓝色沉淀 。某小组同学设计实验探究水溶液中
。某小组同学设计实验探究水溶液中 与
与 反应的产物。
反应的产物。
实验记录如下:将 溶液逐滴加入盐酸酸化的
溶液逐滴加入盐酸酸化的 溶液中,溶液蓝色变浅,有白色沉淀生成。
溶液中,溶液蓝色变浅,有白色沉淀生成。
(1) 溶液用盐酸酸化的目的是
溶液用盐酸酸化的目的是___________ 。
(2)查阅资料得知,该白色沉淀是 。写出产生
。写出产生 的离子方程式:
的离子方程式:___________ 。
(3)甲同学认为:要证明 氧化了
氧化了 ,可检验溶液中含有
,可检验溶液中含有 。操作为:取少量上层清液于试管中,
。操作为:取少量上层清液于试管中,___________ (将操作和现象补充完整)。
(4)乙同学认为:溶液中存在 不一定是
不一定是 氧化的,体系中存在的
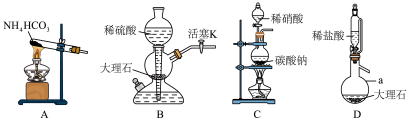
氧化的,体系中存在的 会干扰实验,于是设计了如下4个装置排除体系中的
会干扰实验,于是设计了如下4个装置排除体系中的 。其中合理的是
。其中合理的是___________ (填字母),仪器a的名称是___________ 。
(5)丙同学认为: 的还原性大
的还原性大 ,也可与盐酸酸化的
,也可与盐酸酸化的 溶液反应生成
溶液反应生成 沉淀,你认为是否合理,如果合理,简述你的实验方案,如果不合理,说明理由:
沉淀,你认为是否合理,如果合理,简述你的实验方案,如果不合理,说明理由:___________ 。
(6)称取沉淀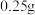 与过量氯化铁溶液反应,待样品完全溶解后,加水
与过量氯化铁溶液反应,待样品完全溶解后,加水 、邻菲啰啉溶液2滴,用
、邻菲啰啉溶液2滴,用 硫酸铈
硫酸铈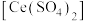 标准溶液滴定,滴定终点时消耗标准溶液
标准溶液滴定,滴定终点时消耗标准溶液 (已知:
(已知:
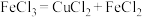 ,
, )。邻菲啰啉溶液的作用是
)。邻菲啰啉溶液的作用是___________ ,沉淀中 的质量分数为
的质量分数为___________ 。
 与
与 发生互促水解生成蓝色沉淀
发生互促水解生成蓝色沉淀 。某小组同学设计实验探究水溶液中
。某小组同学设计实验探究水溶液中 与
与 反应的产物。
反应的产物。实验记录如下:将
 溶液逐滴加入盐酸酸化的
溶液逐滴加入盐酸酸化的 溶液中,溶液蓝色变浅,有白色沉淀生成。
溶液中,溶液蓝色变浅,有白色沉淀生成。(1)
 溶液用盐酸酸化的目的是
溶液用盐酸酸化的目的是(2)查阅资料得知,该白色沉淀是
 。写出产生
。写出产生 的离子方程式:
的离子方程式:(3)甲同学认为:要证明
 氧化了
氧化了 ,可检验溶液中含有
,可检验溶液中含有 。操作为:取少量上层清液于试管中,
。操作为:取少量上层清液于试管中,(4)乙同学认为:溶液中存在
 不一定是
不一定是 氧化的,体系中存在的
氧化的,体系中存在的 会干扰实验,于是设计了如下4个装置排除体系中的
会干扰实验,于是设计了如下4个装置排除体系中的 。其中合理的是
。其中合理的是
(5)丙同学认为:
 的还原性大
的还原性大 ,也可与盐酸酸化的
,也可与盐酸酸化的 溶液反应生成
溶液反应生成 沉淀,你认为是否合理,如果合理,简述你的实验方案,如果不合理,说明理由:
沉淀,你认为是否合理,如果合理,简述你的实验方案,如果不合理,说明理由:(6)称取沉淀
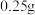 与过量氯化铁溶液反应,待样品完全溶解后,加水
与过量氯化铁溶液反应,待样品完全溶解后,加水 、邻菲啰啉溶液2滴,用
、邻菲啰啉溶液2滴,用 硫酸铈
硫酸铈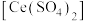 标准溶液滴定,滴定终点时消耗标准溶液
标准溶液滴定,滴定终点时消耗标准溶液 (已知:
(已知:
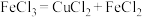 ,
, )。邻菲啰啉溶液的作用是
)。邻菲啰啉溶液的作用是 的质量分数为
的质量分数为
您最近半年使用:0次
名校
解题方法
2 . 通过传感器可以监测空气中甲醛的含量。一种燃料电池型甲醛气体传感器的原理如图所示,下列说法错误的是
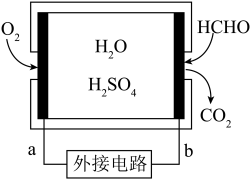

| A.a为电池的正极,发生还原反应 |
B.b极的电极反应为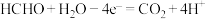 |
C.当电路中转移 电子时,传感器内参加反应的 电子时,传感器内参加反应的 为 为 |
| D.传感器工作过程中,电解质溶液中硫酸的浓度减小 |
您最近半年使用:0次
2023-08-15更新
|
155次组卷
|
2卷引用:辽宁省东港市第二中学2023-2024学年高二上学期开学考试化学试题
名校
解题方法
3 . 如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测。下列说法不正确的是
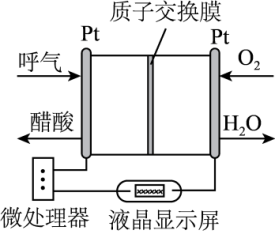

| A.H+在电池工作时向O2所在的铂电极移动 |
| B.电子由呼气的铂电极经电解质溶液流向O2所在的铂电极 |
| C.微处理器通过检测电流大小而计算出被测气体中酒精的含量 |
D.该电池的负极反应式为: |
您最近半年使用:0次
2023-05-18更新
|
348次组卷
|
7卷引用:辽宁省实验中学2020-2021学年高一下学期期中考试化学试题
名校
解题方法
4 . 回答下列问题:
(1)电池是一种将化学能直接转化为电能的装置,它的出现极大方便了人们的生活。如图为三种电池的示意图:
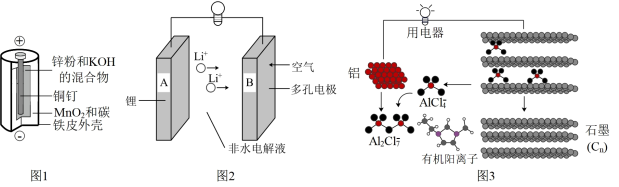
图1中碱性锌锰电池正极反应方程式是_____ 。
(2)锂-空气电池的理论能量密度高,是未来电动汽车续航里程的关键。锂-空气电池的反应原理可表示为:2Li+O2 Li2O2。探究H2O对放电的影响:向非水电解液中加入少量水,放电后检测A、B电极上的固体物质:A极产物:LiOH;B极产物:Li2O2、LiOH,B电极产生LiOH的电极反应方程式是2Li2O2+2H2O=4LiOH+O2↑或
Li2O2。探究H2O对放电的影响:向非水电解液中加入少量水,放电后检测A、B电极上的固体物质:A极产物:LiOH;B极产物:Li2O2、LiOH,B电极产生LiOH的电极反应方程式是2Li2O2+2H2O=4LiOH+O2↑或_____ 。
结论:H2O降低锂-空气电池放电、充电循环性能。
(3)铝离子电池高效耐用、超快充电、高安全性、可折叠、材料成本低等优势。已知图3的正极反应物为CnAlCl4,请写出负极的电极反应式:_____ 。
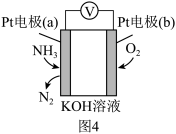
(4)图4所示装置为电化学气敏传感器,通过电压表示数可测量环境中NH3的含量。电极a上发生的电极反应为_____ 。
(1)电池是一种将化学能直接转化为电能的装置,它的出现极大方便了人们的生活。如图为三种电池的示意图:

图1中碱性锌锰电池正极反应方程式是
(2)锂-空气电池的理论能量密度高,是未来电动汽车续航里程的关键。锂-空气电池的反应原理可表示为:2Li+O2
 Li2O2。探究H2O对放电的影响:向非水电解液中加入少量水,放电后检测A、B电极上的固体物质:A极产物:LiOH;B极产物:Li2O2、LiOH,B电极产生LiOH的电极反应方程式是2Li2O2+2H2O=4LiOH+O2↑或
Li2O2。探究H2O对放电的影响:向非水电解液中加入少量水,放电后检测A、B电极上的固体物质:A极产物:LiOH;B极产物:Li2O2、LiOH,B电极产生LiOH的电极反应方程式是2Li2O2+2H2O=4LiOH+O2↑或结论:H2O降低锂-空气电池放电、充电循环性能。
(3)铝离子电池高效耐用、超快充电、高安全性、可折叠、材料成本低等优势。已知图3的正极反应物为CnAlCl4,请写出负极的电极反应式:
(4)图4所示装置为电化学气敏传感器,通过电压表示数可测量环境中NH3的含量。电极a上发生的电极反应为

您最近半年使用:0次
5 . 一种新型水锂充电电池采用复合膜包裹的金属锂和锰酸锂( )作电极材料,以
)作电极材料,以 水溶液作电解质,工作时电池的总反应为
水溶液作电解质,工作时电池的总反应为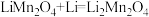 。下列有关该电池的说法
。下列有关该电池的说法错误 的是
 )作电极材料,以
)作电极材料,以 水溶液作电解质,工作时电池的总反应为
水溶液作电解质,工作时电池的总反应为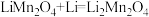 。下列有关该电池的说法
。下列有关该电池的说法
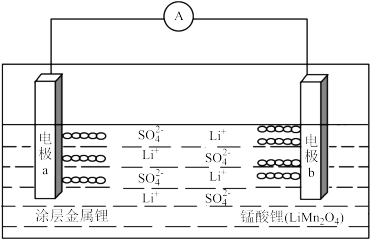
A.该电池放电时,溶液中的 向电极a移动 向电极a移动 |
B.该电池的负极反应式为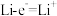 |
| C.电池充电时,阳极的锂元素质量分数减小 |
| D.去掉包裹金属锂的复合膜能使金属锂的利用率更高 |
您最近半年使用:0次
名校
解题方法
6 . 如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测,下列说法不正确 的是
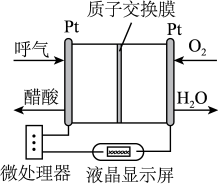

| A.左边的铂电极是负极 |
| B.O2所在的铂电极处发生还原反应 |
| C.该电池的负极反应式为:CH3CH2OH+3H2O—12e—=2CO2↑+12H+ |
| D.微处理器通过检测电流大小而计算出被测气体中酒精的含量 |
您最近半年使用:0次
2022-02-23更新
|
224次组卷
|
2卷引用:浙江省宁波市奉化区2021-2022学年高二上学期期末联考化学试题
名校
解题方法
7 . 电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质。下列说法错误的是
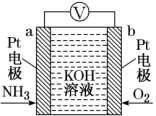

| A.溶液中K+向电极b移动 |
| B.负载通过0.6mol电子时,有4.48L (标况)NH3被氧化 |
| C.反应消耗的NH3与O2的物质的量之比为4:3 |
| D.正极的反应式为:O2+4e-+2H2O=4OH-,故电池工作一段时间后,电解质液溶液的pH升高 |
您最近半年使用:0次
名校
解题方法
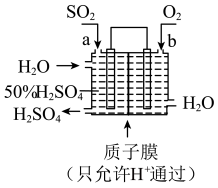
8 .  是大气污染物,造成酸雨的主要原因,用如图所示装置可以既吸收工厂排放的废气中的
是大气污染物,造成酸雨的主要原因,用如图所示装置可以既吸收工厂排放的废气中的 ,又可以生成一定量的硫酸,下列说法不正确的是( )
,又可以生成一定量的硫酸,下列说法不正确的是( )
 是大气污染物,造成酸雨的主要原因,用如图所示装置可以既吸收工厂排放的废气中的
是大气污染物,造成酸雨的主要原因,用如图所示装置可以既吸收工厂排放的废气中的 ,又可以生成一定量的硫酸,下列说法不正确的是( )
,又可以生成一定量的硫酸,下列说法不正确的是( )
| A.a为负极,b为正极 |
| B.从左下口流出的硫酸的质量分数一定大于50% |
| C.生产过程中氢离子由左移向右 |
| D.负极反应式为SO2+2H2O-2e-=SO42—+4H+ |
您最近半年使用:0次
9 . Li电池使用过程中会产生LiH,对电池的性能和安全性带来影响。可用D2O与LiH进行反应测定LiH含量,由产物中的 比例可推算
比例可推算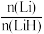 。
。
已知:(1)2LiH 2Li+H2 △H>0。下列说法正确的是
2Li+H2 △H>0。下列说法正确的是
 比例可推算
比例可推算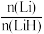 。
。已知:(1)2LiH
 2Li+H2 △H>0。下列说法正确的是
2Li+H2 △H>0。下列说法正确的是| A.H2O、D2O的化学性质基本相同,H、D、T可用于制造氢弹 |
| B.LiH与D2O反应的方程式是LiH+D2O=LiOH+D2 |
C. 比例小说明 比例小说明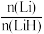 比例小 比例小 |
D.80℃下的 小于25℃下的 小于25℃下的 |
您最近半年使用:0次
10 . 碘、氮及其化合物在生产中应用广泛。
(1)在2HI(g)⇌H2(g)+ I2(g)反应中,三种分子化学键断裂时能量变化如图1所示。其他条件相同,1 mol HI在不同温度分解达平衡时,测得体系中I2的物质的量随温度变化的曲线如图2所示。已知:对于吸热反应,升高温度平衡向右移动。
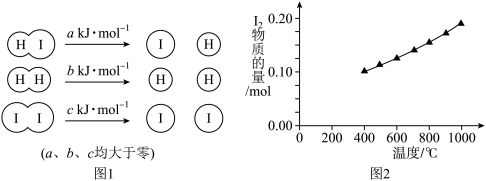
分析图1和图2,比较b+c_______ 2a(填“<”、“>”或“=”),理由是_______ 。
(2)碱性条件下3I2+6OH-=5I-+IO +3H2O,电解KI溶液制备KIO3的工作原理如下图所示。电解过程中观察到阳极液变蓝,一段时间后又逐渐变浅。
+3H2O,电解KI溶液制备KIO3的工作原理如下图所示。电解过程中观察到阳极液变蓝,一段时间后又逐渐变浅。

①b连接电源的_______ 极。
②简要说明制备KIO3的原理:_______ 。
(3)通过NOx,传感器可监测NOx的含量,其工作原理示意图如下:

①NiO电极上发生的是_______ 反应(填氧化或还原)。
②写出NiO电极的电极反应式:_______ 。
(1)在2HI(g)⇌H2(g)+ I2(g)反应中,三种分子化学键断裂时能量变化如图1所示。其他条件相同,1 mol HI在不同温度分解达平衡时,测得体系中I2的物质的量随温度变化的曲线如图2所示。已知:对于吸热反应,升高温度平衡向右移动。

分析图1和图2,比较b+c
(2)碱性条件下3I2+6OH-=5I-+IO
 +3H2O,电解KI溶液制备KIO3的工作原理如下图所示。电解过程中观察到阳极液变蓝,一段时间后又逐渐变浅。
+3H2O,电解KI溶液制备KIO3的工作原理如下图所示。电解过程中观察到阳极液变蓝,一段时间后又逐渐变浅。
①b连接电源的
②简要说明制备KIO3的原理:
(3)通过NOx,传感器可监测NOx的含量,其工作原理示意图如下:

①NiO电极上发生的是
②写出NiO电极的电极反应式:
您最近半年使用:0次



