解题方法
1 . 电能是现代社会应用最广泛的能源之一。
(1)如图所示装置中,Zn是_____ 极(填“正”或“负”)。
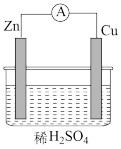
(2)如图所示装置可将______ (写化学方程式)反应释放的能量直接转变为电能;能证明产生电能的实验现象是_____ 。
(3)氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图所示。下列有关氢氧燃料电池的说法,正确的是______ 。

①电极b是正极
②外电路中电子由电极b通过导线流向电极a
③该电池的总反应:2H2+O2=2H2O
(1)如图所示装置中,Zn是

(2)如图所示装置可将
(3)氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图所示。下列有关氢氧燃料电池的说法,正确的是

①电极b是正极
②外电路中电子由电极b通过导线流向电极a
③该电池的总反应:2H2+O2=2H2O
您最近一年使用:0次
解题方法
2 . 根据原电池原理,人们研制出了性能各异的化学电池。
(1)下图装置中, 片作
片作_______ (填“正极”或“负极”), 片上发生反应的电极反应式为
片上发生反应的电极反应式为_______ ,能证明化学能转化为电能的实验现象是_______ 。

(2)下列反应中,通过原电池装置,可实现化学能直接转化为电能的是_______ (填字母)。
a.
b.
c.
(3)某氢氧燃料电池工作原理如图。下列说法正确的是_______ (填字母)。

a.氧气是正极反应物 b.总反应为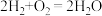 c.电池工作时,其中
c.电池工作时,其中 向
向 一极移动
一极移动
(1)下图装置中,
 片作
片作 片上发生反应的电极反应式为
片上发生反应的电极反应式为
(2)下列反应中,通过原电池装置,可实现化学能直接转化为电能的是
a.

b.

c.

(3)某氢氧燃料电池工作原理如图。下列说法正确的是

a.氧气是正极反应物 b.总反应为
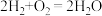 c.电池工作时,其中
c.电池工作时,其中 向
向 一极移动
一极移动
您最近一年使用:0次
解题方法
3 . 某研究小组探究原电池的原理并进行实验。
(1)下列反应中,可通过原电池装置实现化学能直接转化为电能的是(选填序号)_______ 。
① ②
②
③ ④
④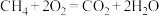
(2)甲同学用导线将电流表与 片、
片、 片相连接,插入盛有稀硫酸的烧杯中进行实验Ⅰ,如图1所示。
片相连接,插入盛有稀硫酸的烧杯中进行实验Ⅰ,如图1所示。

①能证明化学能转化为电能的实验现象是:电流表指针偏转、_______ 。
②从构成原电池的基本要素来看, 的作用是(选填序号,下同)
的作用是(选填序号,下同)_______ ,稀硫酸的作用是_______ 。
a.电极反应物 b.电极材料 c.离子导体 d.电子导体
(3)乙同学想利用反应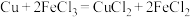 设计一个原电池,请在图2上标明所使用的用品
设计一个原电池,请在图2上标明所使用的用品_______ 。

(4)氢氧燃料电池是一种新型发电装置(如图3所示),下列叙述不正确 的是_______ 。
a.通氢气的一极是正极,发生氧化反应
b.电子由 电极经溶液流向
电极经溶液流向 电极
电极
c.总反应为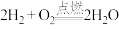

(1)下列反应中,可通过原电池装置实现化学能直接转化为电能的是(选填序号)
①
 ②
②
③
 ④
④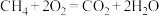
(2)甲同学用导线将电流表与
 片、
片、 片相连接,插入盛有稀硫酸的烧杯中进行实验Ⅰ,如图1所示。
片相连接,插入盛有稀硫酸的烧杯中进行实验Ⅰ,如图1所示。
①能证明化学能转化为电能的实验现象是:电流表指针偏转、
②从构成原电池的基本要素来看,
 的作用是(选填序号,下同)
的作用是(选填序号,下同)a.电极反应物 b.电极材料 c.离子导体 d.电子导体
(3)乙同学想利用反应
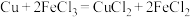 设计一个原电池,请在图2上标明所使用的用品
设计一个原电池,请在图2上标明所使用的用品
(4)氢氧燃料电池是一种新型发电装置(如图3所示),下列叙述
a.通氢气的一极是正极,发生氧化反应
b.电子由
 电极经溶液流向
电极经溶液流向 电极
电极c.总反应为
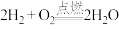

您最近一年使用:0次
解题方法
4 . 电池的发明是化学对人类的一项重大贡献。
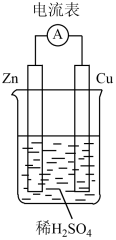
(1)下图所示装置中,Zn片作___________ (填“正极”或“负极”)。Cu片上发生反应的电极反应式为___________ ;能证明化学能转化为电能的实验现象是___________ 。
(2)氢氧燃料电池是一种高效、低污染的新型电池,在新能源汽车、航空航天、轨道交通等领域均有应用。某氢氧燃料电池的示意图如下。

下列说法正确的是___________ (填序号)。
①b电极是电池的负极
②该装置实现了将 反应释放的能量直接转化为电能
反应释放的能量直接转化为电能
③电池工作时,电池内部的 定向移动
定向移动
(1)下图所示装置中,Zn片作

(2)氢氧燃料电池是一种高效、低污染的新型电池,在新能源汽车、航空航天、轨道交通等领域均有应用。某氢氧燃料电池的示意图如下。

下列说法正确的是
①b电极是电池的负极
②该装置实现了将
 反应释放的能量直接转化为电能
反应释放的能量直接转化为电能③电池工作时,电池内部的
 定向移动
定向移动
您最近一年使用:0次
解题方法
5 . 实验室中,学生利用下图装置制作一个简单燃料电池。步骤如下:

①检验装置气密性后向U形管中注入适量的6 mol·L-1稀H2SO4溶液,至接近橡胶塞底部。
②接通学生电源K1,观察实验现象,当一端玻璃导管内的液柱接近溢出时,切断学生电源K1。
③将石英钟内的干电池取出,用导线与石英钟的正负极相连,接入装置中。接通学生电源K2,观察石英钟指针。
回答下列问题:
(1)接通学生电源K1,在右侧石墨棒表面观察到_______ 。
(2)观察到左侧的玻璃导管内的液柱先接近溢出,说明左侧石墨棒所连的是学生电源的_______ (填“正极”或“负极”),该石墨表面的电极方程式是_______ 。
(3)用导线与石英钟的正负极相连接入装置时,石英钟的正极应与_______ (填“左”或“右”)侧的石墨棒连接的导线相连。
(4)出现_______ 的现象,证明该燃料电池制作成功。燃料电池正极的电极方程式是_______ 。

①检验装置气密性后向U形管中注入适量的6 mol·L-1稀H2SO4溶液,至接近橡胶塞底部。
②接通学生电源K1,观察实验现象,当一端玻璃导管内的液柱接近溢出时,切断学生电源K1。
③将石英钟内的干电池取出,用导线与石英钟的正负极相连,接入装置中。接通学生电源K2,观察石英钟指针。
回答下列问题:
(1)接通学生电源K1,在右侧石墨棒表面观察到
(2)观察到左侧的玻璃导管内的液柱先接近溢出,说明左侧石墨棒所连的是学生电源的
(3)用导线与石英钟的正负极相连接入装置时,石英钟的正极应与
(4)出现
您最近一年使用:0次
解题方法
6 . 化学能在一定条件下可转化为电能。

(1)图A所示装置中,锌片是_______ (填“正极”或“负极”)。
(2)图A所示装置可将_______ (写化学方程式)释放的能量直接转化为电能,证明化学能转化为电能的实验现象是:铜片上有气泡产生、 _______ 。
(3)燃料电池已经开始应用于新能源汽车等领域,某氢氧燃料电池的原理如图B所示。下列说法正确的是_______ (填序号)。
①氧气是负极反应物
②总反应为2H2+O2=2H2O
③电池工作时,其中H+定向移动

(1)图A所示装置中,锌片是
(2)图A所示装置可将
(3)燃料电池已经开始应用于新能源汽车等领域,某氢氧燃料电池的原理如图B所示。下列说法正确的是
①氧气是负极反应物
②总反应为2H2+O2=2H2O
③电池工作时,其中H+定向移动
您最近一年使用:0次
名校
7 . 汽车让人们的生活越来越便捷。请回答以下问题:
(1)汽车尾气主要含有CO2、CO、SO2、NO等物质,是造成城市空气污染的主要因素之一,N2和O2反应生成NO的能量变化如图所示,则由该反应生成1mol NO时,应___________ (填“释放”或“吸收”)___________ kJ能量。
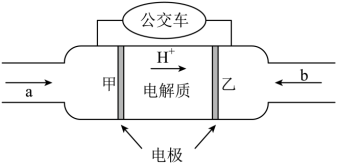
(3)近年来广州首批15辆氢燃料电池公交车已经投入运营,标志着广州公交进入氢能产业时代,如图是某种氢氧燃料电池的内部结构示意图,该电池工作时,氢气从___________ (填“a”或“b”)处通入,正极反应方程式为___________ ,标况下消耗11.2L空气,整个电路中转移的电子数约为___________ NA。___________ ,负极电极反应式为___________ 。
(1)汽车尾气主要含有CO2、CO、SO2、NO等物质,是造成城市空气污染的主要因素之一,N2和O2反应生成NO的能量变化如图所示,则由该反应生成1mol NO时,应




| A.NaN3属于离子化合物 |
| B.NaN3的分解反应属于吸热反应 |
| C.E1表示2mol NaN3固体的能量 |
| D.NaN3作为安全气囊的气体发生剂,具有产气快、产气量大等优点 |
(3)近年来广州首批15辆氢燃料电池公交车已经投入运营,标志着广州公交进入氢能产业时代,如图是某种氢氧燃料电池的内部结构示意图,该电池工作时,氢气从
您最近一年使用:0次
8 . 燃料电池是很有发展前途的新的动力电源,氢氧燃料电池因其绿色环保、能量转换率高而备受关注。通常氢氧燃料电池有酸式和碱式两种,试回答下列问题:
(1)在碱式介质中,负极反应的物质为_____ ,正极反应的物质为_____ 碱式电池的电极反应:负极:_____ ,正极:_____ 。电解质溶液pH的变化_____ (填“变大”,“变小”,“不变”)。
(2)氢氧燃料电池汽车作为上海世博园中的交通工具之,下列不正确的是_____。(单选)
(3)纯电动车采用了高效耐用的一种新型可充电电池,该电池的总反应式为:

①该电池放电时正极反应式为_____ 。
②放电时每转移3mol电子,正极有_____ mol 被还原。
被还原。
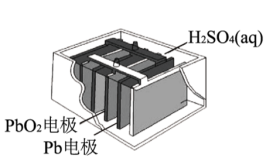
(4)铅蓄电池因其电压稳定、使用方便、安全可靠、价格低康,当前在燃油车上应用依然占主导地位,电池反应式为: ,下列有关说法正确的是_____。(双选)
,下列有关说法正确的是_____。(双选)

(1)在碱式介质中,负极反应的物质为
(2)氢氧燃料电池汽车作为上海世博园中的交通工具之,下列不正确的是_____。(单选)
| A.太阳光催化分解水制氯气比电解水气氢气更为科学 |
| B.氢氧燃料电池作为汽车动力更能保护环境 |
C.以稀 、KOH为介质的氢氧燃料电池的负极电极反应式相同 、KOH为介质的氢氧燃料电池的负极电极反应式相同 |
D.以稀 、KOH为介质的氢氧燃料电池的总反应式相同 、KOH为介质的氢氧燃料电池的总反应式相同 |

①该电池放电时正极反应式为
②放电时每转移3mol电子,正极有
 被还原。
被还原。(4)铅蓄电池因其电压稳定、使用方便、安全可靠、价格低康,当前在燃油车上应用依然占主导地位,电池反应式为:
 ,下列有关说法正确的是_____。(双选)
,下列有关说法正确的是_____。(双选)
A.Pb为电池的负极,发生氧化反应,电极方程式为: |
| B.铅蓄电池放电时,正、负电极质量均增大 |
C.铅蓄电池放电时, 定向移动去 定向移动去 极 极 |
| D.放电过程中,正极区附近pH减小 |
您最近一年使用:0次
解题方法
9 . 金属镍及其合金是工业上重要的材料。
(1)镍是有机物加氢的催化剂,写出丙烯与H2反应的化学方程式___________
(2)镍合金在苛刻的腐蚀环境中具有优良的耐腐蚀性能,钝化作用优于铁,推测镍合金耐腐蚀的原因是___________ ,C-276是一种大量降低含碳、硅量的镍合金,指出C-276耐腐蚀的另一原因___________ ,C-276在不同酸中的腐蚀速率如下:
下列说法不正确的是___________
A.同种酸浓度越大,腐蚀速率越快
B.阴离子对腐蚀速率有影响
C.Cf可能会促进金属腐蚀
D.c(H+)相同的硫酸腐蚀速率快于硝酸
(3)镍常用作燃料电池的电极兼催化剂,下图是氢氧燃料电池的结构图:
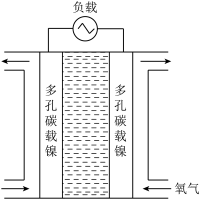
①选择多孔碳载镍电极的原因是___________
②降低电池内阻可以提高电池的工作效率,从而增大电池单位质量输出的电能。电池内阻和离子导体的导电性等因素有关。下表列出在298K时,无限稀释溶液中几种离子的无限稀释摩尔电导率
已知:镍与铁同族性质相似,电池工作时O2会与碳反应生成CO2。
通常燃料电池离子导体选择稀硫酸或氢氧化钾溶液,请说明选择稀硫酸做离子导体的优点1:___________ ,优点2:___________ 。
(1)镍是有机物加氢的催化剂,写出丙烯与H2反应的化学方程式
(2)镍合金在苛刻的腐蚀环境中具有优良的耐腐蚀性能,钝化作用优于铁,推测镍合金耐腐蚀的原因是
| 介质 | 10% HNO3 | 65% HNO3 | 10% H2SO4 | 10% HCl |
| 腐蚀速率mm/年 | 748 | 29527 | 906 | 9409 |
A.同种酸浓度越大,腐蚀速率越快
B.阴离子对腐蚀速率有影响
C.Cf可能会促进金属腐蚀
D.c(H+)相同的硫酸腐蚀速率快于硝酸
(3)镍常用作燃料电池的电极兼催化剂,下图是氢氧燃料电池的结构图:

①选择多孔碳载镍电极的原因是
②降低电池内阻可以提高电池的工作效率,从而增大电池单位质量输出的电能。电池内阻和离子导体的导电性等因素有关。下表列出在298K时,无限稀释溶液中几种离子的无限稀释摩尔电导率
| 离子种类 | H+ | OH- |  SO SO | Cl- |  CO CO | K+ | Na+ |
| 无限稀释摩尔电导率×104/(S·m2·mol) | 349.82 | 198.0 | 79.8 | 76.34 | 72 | 73.52 | 50.11 |
通常燃料电池离子导体选择稀硫酸或氢氧化钾溶液,请说明选择稀硫酸做离子导体的优点1:
您最近一年使用:0次
10 . 阅读下列短文并填空。
“绿色办奥”是北京冬奥会四大办奥理念之首,在“双碳”目标驱动下,全球首次服务体育赛事的大批量氢燃料客车在北京冬奥会上闪亮登场。
氢燃料大客车从车辆排放端实现了零污染、零排放。氢燃料电池是氢气和氧化剂通过特定装置发生反应将化学能转变为电能的化学电源。氢氧燃料电池在工作时,氧化剂和还原剂不接触即可在电池内部发生反应生成H2O,同时产生电能。
氢燃料客车还搭载了“U度”综合热管理技术。该技术可将氢燃料电池所产生的“废热”循环利用,为车内采暖、除霜、除雾提供能量。该车的极寒动力电池能让车辆实现零下30摄氏度极寒低温起动。
未来,氢燃料客车有望从“冬奥平台”出发,将应用场景拓展延伸至更多领域。
(1)氢燃料电池工作时负极通入的物质是_______ 。
(2)氢燃料电池工作时涉及的能量转化形式有_______ 。
a.电能转化为化学能 b.化学能转化为电能
c.化学能转化为热能 d.太阳能转化为电能
(3)氢燃料电池生成1molH2O时,通过线路的电子是_______ mol。
(4)下列关于氢燃料客车的说法,正确的是_______ 。
a.氢燃料客车环保,助力实现“双碳”目标
b.氢氧燃料电池工作时的总反应为2H2+O2=2H2O
c.氢燃料客车不能在极寒天气中使用
“绿色办奥”是北京冬奥会四大办奥理念之首,在“双碳”目标驱动下,全球首次服务体育赛事的大批量氢燃料客车在北京冬奥会上闪亮登场。
氢燃料大客车从车辆排放端实现了零污染、零排放。氢燃料电池是氢气和氧化剂通过特定装置发生反应将化学能转变为电能的化学电源。氢氧燃料电池在工作时,氧化剂和还原剂不接触即可在电池内部发生反应生成H2O,同时产生电能。
氢燃料客车还搭载了“U度”综合热管理技术。该技术可将氢燃料电池所产生的“废热”循环利用,为车内采暖、除霜、除雾提供能量。该车的极寒动力电池能让车辆实现零下30摄氏度极寒低温起动。
未来,氢燃料客车有望从“冬奥平台”出发,将应用场景拓展延伸至更多领域。
(1)氢燃料电池工作时负极通入的物质是
(2)氢燃料电池工作时涉及的能量转化形式有
a.电能转化为化学能 b.化学能转化为电能
c.化学能转化为热能 d.太阳能转化为电能
(3)氢燃料电池生成1molH2O时,通过线路的电子是
(4)下列关于氢燃料客车的说法,正确的是
a.氢燃料客车环保,助力实现“双碳”目标
b.氢氧燃料电池工作时的总反应为2H2+O2=2H2O
c.氢燃料客车不能在极寒天气中使用
您最近一年使用:0次



