名校
解题方法
1 . 应用电化学原理,回答下列问题。
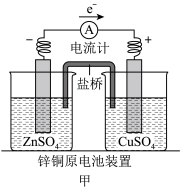
(1)甲中电流计指针偏移时,盐桥(装有含琼胶的KCl饱和溶液)中离子移动的方向是_______ 。
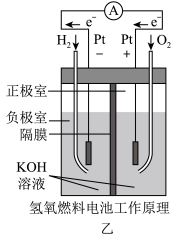
(2)乙中正极反应式为___________ ;若将H2换成CH4,则负极反应式为___________ 。
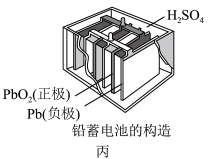
(3)丙中铅蓄电池放电一段时间后,进行充电时,要将外接电源的负极与铅蓄电池___________ 极相连接。充电时该电极反应式___________ 。
(4)若用铅蓄电池作为电源电解硝酸银溶液500mL,电路中转移0.2mol电子,则溶液中氢离子浓度为___________ (忽略溶液体积变化)。
(5)氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可利用电解原理,将氨转化为高纯氢气,其装置如图所示。

①电解过程中OH-的移动方向为___________ (填“从左往右”或“从右往左”);
②阳极的电极反应式为___________ 。
(1)甲中电流计指针偏移时,盐桥(装有含琼胶的KCl饱和溶液)中离子移动的方向是

(2)乙中正极反应式为

(3)丙中铅蓄电池放电一段时间后,进行充电时,要将外接电源的负极与铅蓄电池

(4)若用铅蓄电池作为电源电解硝酸银溶液500mL,电路中转移0.2mol电子,则溶液中氢离子浓度为
(5)氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可利用电解原理,将氨转化为高纯氢气,其装置如图所示。

①电解过程中OH-的移动方向为
②阳极的电极反应式为
您最近一年使用:0次
名校
解题方法
2 . 降低能耗是氯碱工业发展的重要方向。
(1)我国利用氯碱厂生产的 作燃料,将氢燃料电站应用于氯碱工业,其示意图如下。
作燃料,将氢燃料电站应用于氯碱工业,其示意图如下。
① 极为
极为_____ (填“正”或“负”)极。
②乙装置中电解饱和 溶液的化学方程式为
溶液的化学方程式为_____ 。
③下列说法正确的是_____ 。
A.甲装置可以实现化学能向电能转化
B.甲装置中 透过阳离子交换膜向
透过阳离子交换膜向 极移动
极移动
C.乙装置中 极一侧流出的是淡盐水
极一侧流出的是淡盐水
④结合化学用语解释 极区产生
极区产生 的原因:
的原因:_____ 。
⑤实际生产中,阳离子交换膜的损伤会造成 迁移至阳极区,从而在电解池阳极能检测到
迁移至阳极区,从而在电解池阳极能检测到 ,产生
,产生 的电极反应式为
的电极反应式为_____ 。下列生产措施有利于提高 产量、降低阳极
产量、降低阳极 含量的是
含量的是_____ 。
A.定期检查并更换阳离子交换膜
B.向阳极区加入适量盐酸
C.使用 浓度高的精制饱和食盐水为原料
浓度高的精制饱和食盐水为原料
(2)降低氯碱工业能耗的另一种技术是“氧阴极技术”。通过向阴极区通入 ,避免水电离的
,避免水电离的 直接得电子生成
直接得电子生成 ,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为
,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为_____ 。
(1)我国利用氯碱厂生产的
 作燃料,将氢燃料电站应用于氯碱工业,其示意图如下。
作燃料,将氢燃料电站应用于氯碱工业,其示意图如下。
①
 极为
极为②乙装置中电解饱和
 溶液的化学方程式为
溶液的化学方程式为③下列说法正确的是
A.甲装置可以实现化学能向电能转化
B.甲装置中
 透过阳离子交换膜向
透过阳离子交换膜向 极移动
极移动C.乙装置中
 极一侧流出的是淡盐水
极一侧流出的是淡盐水④结合化学用语解释
 极区产生
极区产生 的原因:
的原因:⑤实际生产中,阳离子交换膜的损伤会造成
 迁移至阳极区,从而在电解池阳极能检测到
迁移至阳极区,从而在电解池阳极能检测到 ,产生
,产生 的电极反应式为
的电极反应式为 产量、降低阳极
产量、降低阳极 含量的是
含量的是A.定期检查并更换阳离子交换膜
B.向阳极区加入适量盐酸
C.使用
 浓度高的精制饱和食盐水为原料
浓度高的精制饱和食盐水为原料(2)降低氯碱工业能耗的另一种技术是“氧阴极技术”。通过向阴极区通入
 ,避免水电离的
,避免水电离的 直接得电子生成
直接得电子生成 ,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为
,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为
您最近一年使用:0次
2023-10-01更新
|
50次组卷
|
3卷引用:北京市北京医学院附属中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
3 . 降低能耗是氯碱工业发展的重要方向。
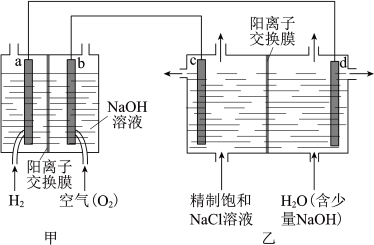
(1)我国利用氯碱厂生产的H2作燃料,将氢燃料电站应用于氯碱工业,其示意图如图。
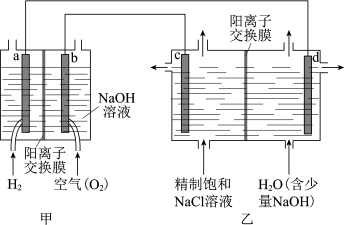
①a极为_______ (填“正”或“负”)极。
②乙装置中电解饱和NaCl溶液的化学方程式为。_______ 。
③下列说法正确的是_______ 。
A.甲装置可以实现化学能向电能转化
B.甲装置中Na+透过阳离子交换膜向a极移动
C.乙装置中c极一侧流出的是淡盐水
④实际生产中,阳离子交换膜的损伤会造成OH- 迁移至阳极区,从而在电解池阳极能检测到O2,产生O2的电极反应式为_______ 。下列生产措施有利于提高Cl2产量、降低阳极O2含量的是_______ 。
A.定期检查并更换阳离子交换膜
B.向阳极区加入适量盐酸
C.使用Cl-浓度高的精制饱和食盐水为原料
(2)降低氯碱工业能耗的另一种技术是“氧阴极技术”。通过向阴极区通入O2,避免水电离的H+直接得电子生成H2,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为_______ 。
(1)我国利用氯碱厂生产的H2作燃料,将氢燃料电站应用于氯碱工业,其示意图如图。

①a极为
②乙装置中电解饱和NaCl溶液的化学方程式为。
③下列说法正确的是
A.甲装置可以实现化学能向电能转化
B.甲装置中Na+透过阳离子交换膜向a极移动
C.乙装置中c极一侧流出的是淡盐水
④实际生产中,阳离子交换膜的损伤会造成OH- 迁移至阳极区,从而在电解池阳极能检测到O2,产生O2的电极反应式为
A.定期检查并更换阳离子交换膜
B.向阳极区加入适量盐酸
C.使用Cl-浓度高的精制饱和食盐水为原料
(2)降低氯碱工业能耗的另一种技术是“氧阴极技术”。通过向阴极区通入O2,避免水电离的H+直接得电子生成H2,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为
您最近一年使用:0次
2022-04-12更新
|
208次组卷
|
9卷引用:北京市西城区2020-2021学年高二上学期期末考试化学试题
北京市西城区2020-2021学年高二上学期期末考试化学试题北京师范大学第二附属中学未来科技城学校2021-2022学年高二上学期期中考试化学试题北京三中2021-2022学年高二上学期期中考试化学试题江西省南昌市第二中学2020-2021学年高二上学期期末考试化学试题江西省临川一中暨临川一中实验学校2021-2022学年高二上学期期末考试化学试题吉林省长春市清蒲中学2021-2022学年高二上学期期末考试化学试题吉林省长春市清蒲中学2021-2022学年高二上学期期末考试化学试题吉林省永吉县第四中学2022-2023学年高二上学期期末考试化学试题天津市武清区杨村第一中学2023-2024学年高三上学期第三次质量检测化学试题
名校
4 . (1)海水资源的利用具有广阔前景。海水中主要离子的含量如下:
电渗析法淡化海水示意图如图所示,其中阴(阳) 离子交换膜仅允许阴(阳)离子通过。

①电解氯化钠溶液的离子方程式_____ 。
②电解过程中阴极区碱性明显增强,用平衡移动原理 解释原因_____ 。 在阴极附近产生少量白色沉淀,其成分有_________ 和CaCO3。
③淡水的出口为_________ (填“a”、“b”或“c”);a 出口物质为_____ (填化学式)。
④若用下面燃料电池为电源电解 100mL1mol•L-1氯化钠溶液,当电池消耗0.00025 molO2时,常温下,所得溶液的 pH 为__________ (忽略反应前后溶液体积变化)
(2)如图Ⅰ是氢氧燃料电池(电解质为 KOH 溶液)的结构示意图,

①Ⅰ中通入O2的一端为电池的_____ 极。 通入H2的一端的电极反应式_________
②若在Ⅱ中实现锌片上镀铜,则 b 的电极材料是_____ ,N 溶液为_____ 溶液。
③若在Ⅱ中实现 Cu+H2SO4= CuSO4+H2↑,则a 极的反应式是_____ ,N 溶液为 _____ 溶液。
(3)工业上用 Na2SO3溶液吸收 SO2,过程中往往得到 Na2SO3和 NaHSO3的混合溶液,溶液 pH 随 n( ):n(
):n( ) 变化关系如下表:
) 变化关系如下表:
当吸收液的 pH 降至约为 6 时,送至电解槽再生。再生示意图如下,结合图示回答:

① 在阳极放电的电极反应式是
在阳极放电的电极反应式是_____ 。
②当阴极室中溶液 pH升至 8 以上时,吸收液再生并循环利用。简述再生原理:_____ 。
| 成分 | 含量/(mg/L) | 成分 | 含量/(mg/L) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 |  | 142 |
 | 2560 | Br- | 64 |
| Mg2+ | 1272 |
电渗析法淡化海水示意图如图所示,其中阴(阳) 离子交换膜仅允许阴(阳)离子通过。

①电解氯化钠溶液的离子方程式
②电解过程中阴极区碱性明显增强,用平衡移动原理 解释原因
③淡水的出口为
④若用下面燃料电池为电源电解 100mL1mol•L-1氯化钠溶液,当电池消耗0.00025 molO2时,常温下,所得溶液的 pH 为
(2)如图Ⅰ是氢氧燃料电池(电解质为 KOH 溶液)的结构示意图,

①Ⅰ中通入O2的一端为电池的
②若在Ⅱ中实现锌片上镀铜,则 b 的电极材料是
③若在Ⅱ中实现 Cu+H2SO4= CuSO4+H2↑,则a 极的反应式是
(3)工业上用 Na2SO3溶液吸收 SO2,过程中往往得到 Na2SO3和 NaHSO3的混合溶液,溶液 pH 随 n(
 ):n(
):n( ) 变化关系如下表:
) 变化关系如下表:n( ): n( ): n( ) ) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
当吸收液的 pH 降至约为 6 时,送至电解槽再生。再生示意图如下,结合图示回答:

①
 在阳极放电的电极反应式是
在阳极放电的电极反应式是②当阴极室中溶液 pH升至 8 以上时,吸收液再生并循环利用。简述再生原理:
您最近一年使用:0次



