9-10高二下·河北·阶段练习
名校
解题方法
1 . 下面有关电化学的图示,完全正确的是
A.Cu-Zn原电池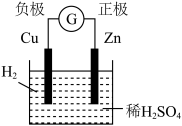 | B.粗铜的精炼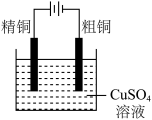 |
C.铁片镀锌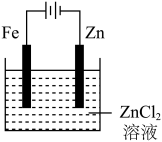 | D.验证NaCl溶液(含酚酞)电解产物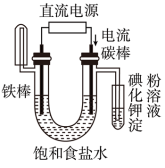 |
您最近一年使用:0次
2022-12-21更新
|
662次组卷
|
59卷引用:山东省德州市2017-2018学年高二上学期期末考试化学试题
山东省德州市2017-2018学年高二上学期期末考试化学试题2014-2015湖南省娄底市湘中名校高二上学期期末化学(理)试卷2015-2016学年黑龙江东部地区高二上学期期末联考化学试卷2016-2017学年山东省寿光中学高二上10月月考化学卷2016-2017黑龙江牡丹江第一高级中学高二上期末化学卷内蒙古包头市铁路一中2016-2017学年高二下学期期末考试化学试题山东省寿光现代中学2017-2018学年高二上学期开学考试化学试题河南省安阳市2016-2017学年高二上学期期末考试化学试题青海省西宁市第四高级中学2017-2018学年高二上学期期末考试化学试题云南省腾冲市第八中学2017-2018学年高二下学期期末考试化学试题山东省泰安第四中学2018-2019学年高二上学期12月月考化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二上学期期末考试化学试题黑龙江省大庆市第十中学2019-2020学年高二上学期期末考试化学试题陕西省咸阳市2019—2020学年高二上学期期末考试化学试题湖南广益实验中学2019-2020学年高二上学期期末考试化学试题江西省上饶市2018-2019学年高二下学期期末教学质量测试化学试题山东省泰安市宁阳一中2020-2021学年高二上学期10月学习质量检测化学试题 山东省泰安市宁阳县宁阳一中2020-2021学年高二上学期第一阶段考试化学试题内蒙古北京八中乌兰察布分校2020-2021学年高二上学期期末考试化学试题陕西省安康市六校联考2021-2022学年高二上学期期末考试化学试题四川省凉山州2021-2022学年高二上学期期末考试化学试题陕西省西安市西航一中2021-2022学年高二上学期期末考试化学试题广东省兴宁市下堡中学2021-2022学年高二上学期期末质量检测化学试题宁夏石嘴山三中2015~2016学年度高二上学期期末化学试卷【解析版】(已下线)2009—2010学年存瑞中学第二学期第二阶段考试高二化学试题2015届上海市虹口区高三上学期期末考试化学试卷2014-2015学年福建省晋江市季延中学高二下学期期中考试化学试卷2015-2016学年河北省成安一中高二上学期1月月考化学试卷2015-2016学年广西钦州港经济开发区中学高一上学期期末化学试卷河北省承德市第一中学2017-2018学年高二上学期第一次月考化学试题安徽省蚌埠市第二中学2017-2018学年高二上学期期中考试化学试题四川省什邡中学2017-2018学年高二春秋招班第三次月考化学试题河南省郑州市第一中学2018-2019学年高二上学期入学测试化学试题高二人教版选修4 第四章 第三节 电解池【全国百强校】福建省莆田市第一中学2018-2019学年高二上学期期中考试化学试题【校级联考】江西省吉安市几所重点中学2018-2019学年高二上学期联考化学试题【全国百强校】江西省临川第一中学2018-2019学年高二上学期12月月考化学试题【全国百强校】黑龙江省大庆市第一中学2018-2019学年高二下学期第三次阶段考试化学试题重庆市第三十中学2018-2019学年高二上学期第三次月考化学试题广东省深圳科学高中2019-2020学年高二上学期开学考试化学试题浙江省宁波市余姚中学2019-2020学年高二上学期期中考试化学试题四川省新津中学2019-2020学年高二下学期4月月考(入学)化学试题黑龙江省哈尔滨师范大学青冈实验中学校2019-2020学年高二上学期开学考试(8月)化学试题(已下线)【浙江新东方】43(已下线)【浙江新东方】绍兴qw124安徽省六安市舒城县舒州中学2020-2021学年高二上学期12月月考化学试题安徽省淮北市树人高级中学2020-2021学年高二下学期第一次阶段考试化学试题江苏省吴江汾湖高级中学2020-2021学年高二下学期阶段性教学质量检测化学试题内蒙古集宁新世纪中学2020-2021学年高二下学期质量检测月考化学试题安徽省泗县第一中学2021-2022学年高二上学期第二次月考化学试题河北省邢台市第一中学2021-2022学年高二上学期第三次月考化学试题(已下线)第29讲 第四章《化学反应与电能》单元测试(基础巩固)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)辽宁省锦州市黑山县黑山中学2021-2022学年高二上学期12月月考化学试题福建省宁德第一中学2020-2021学年高二上学期第一次月考化学试题2015届江西省吉安市白鹭洲中学高三上学期期中化学试卷2017届宁夏石嘴山三中高三上期中化学试卷【全国百强校】上海市复旦大学附属中学2019—2020学年高三上学期期中考试化学试题宁夏银川市宁夏大学附属中学2021届高三上学期第一次月考化学试题(已下线)专题突破卷07 化学反应与能量?-2024年高考化学一轮复习考点通关卷(新教材新高考)
名校
解题方法
2 . 某同学利用下图所示装置探究金属的腐蚀与防护条件。下列不合理的是
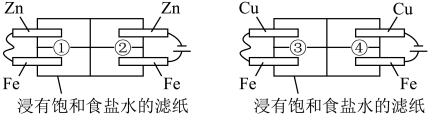

A.①区 电极的电极反应式为 电极的电极反应式为 , , 电极附近滴加 电极附近滴加 溶液未出现蓝色, 溶液未出现蓝色, 被保护 被保护 |
B.②区 电极的电极反应式为 电极的电极反应式为 , , 电极附近滴加 电极附近滴加 溶液出现蓝色, 溶液出现蓝色, 被腐蚀 被腐蚀 |
C.③区 电极上产生气泡, 电极上产生气泡, 电极附近滴加 电极附近滴加 溶液后出现蓝色, 溶液后出现蓝色, 被腐蚀 被腐蚀 |
D.④区 电极附近滴加酚酞后变成红色, 电极附近滴加酚酞后变成红色, 电极附近滴加 电极附近滴加 溶液出现蓝色, 溶液出现蓝色, 被腐蚀 被腐蚀 |
您最近一年使用:0次
2022-12-09更新
|
507次组卷
|
2卷引用:山东省青岛第二中学2020-2021学年高二上学期期末化学试题
解题方法
3 . 一种新型可充电钠离子电池的工作原理如图所示。下列说法正确的是
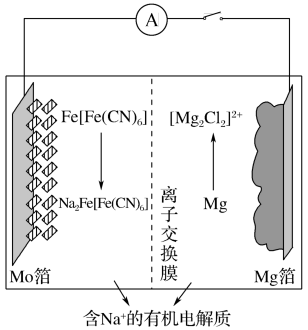

| A.放电时,Mo箔为正极 |
B.充电时, 通过交换膜从右室移向左室 通过交换膜从右室移向左室 |
C.放电时,外电路中通过0.1mol电子时,左室中生成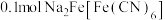 |
D.充电时,阴极反应为 |
您最近一年使用:0次
2022-11-17更新
|
234次组卷
|
2卷引用:山东省菏泽市2022-2023学年高二上学期期末考试(线上)化学试题
名校
4 . 酸性锌锰干电池是一种常用的一次电池,其结构如图所示。该电池在放电过程产生MnOOH和Zn(NH3)2Cl2。回答下列问题:
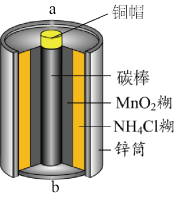
(1)该电池的正极为____ (填“a”或“b”)极,该电池总反应的化学方程式为____ 。
(2)如图为电解100mL2.0mol·L-1CuSO4溶液的装置,该装置的电源为上述酸性锌锰干电池。
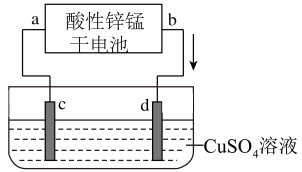
①电解一段时间后,石墨电极d出现的现象为____ ;石墨电极c上的电极反应式为____ 。
②当上述电池消耗3.25gZn时,电解后溶液中c(H+)为_____ (忽略电解前后溶液体积变化)。欲将电解后的溶液恢复至原溶液,应加入的试剂是____ ,其质量为____ g。

(1)该电池的正极为
(2)如图为电解100mL2.0mol·L-1CuSO4溶液的装置,该装置的电源为上述酸性锌锰干电池。

①电解一段时间后,石墨电极d出现的现象为
②当上述电池消耗3.25gZn时,电解后溶液中c(H+)为
您最近一年使用:0次
2022-09-06更新
|
163次组卷
|
4卷引用:山东省菏泽市鄄城县第一中学2022-2023学年高二上学期期末考试化学试题
解题方法
5 . 某油脂厂废弃的镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收镍制备硫酸镍晶体(NiS4·7H2O)。
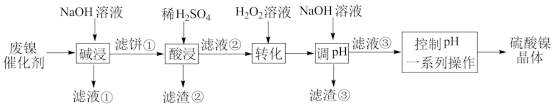
已知某些金属离子开始沉淀和沉淀完全的pH如下:
回答下列问题:
(1)提高“碱浸”速率的有效措施有_______ (任写一种即可);“滤液②”中含有的金属离子有_______ 。
(2)写出“转化”中发生反应的离子方程式_______ 。
(3)若“转化”后溶液中Ni2+浓度为1mol·L-1,则“调pH”应控制的范围为___ 。
(4)获得硫酸镍晶体时,需经过控制pH、_____ 、_____ 过滤等“一系列操作”。
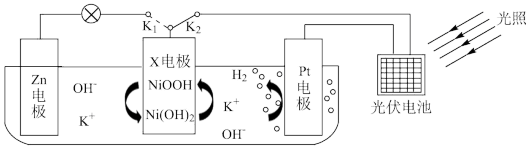
(5)硫酸镍可用来制备新型镍电池电极材料NiOOH,我国科研团队利用该电极材料设计了一种新型能量存储-转化装置(如图)。闭合K2、断开K1时,制氢并储能;断开K2、闭合K1时,供电。供电时,X电极反应式为_______ 。

已知某些金属离子开始沉淀和沉淀完全的pH如下:
| 金属离子 | Ni2+ | A13+ | Fe3+ | Fe2+ |
| 开始沉淀时(c=0.01mol·L-1)的pH | 7.2 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时(c=1.0×10-5mol·L-1)的pH | 8.7 | 4.7 | 3.2 | 9.0 |
(1)提高“碱浸”速率的有效措施有
(2)写出“转化”中发生反应的离子方程式
(3)若“转化”后溶液中Ni2+浓度为1mol·L-1,则“调pH”应控制的范围为
(4)获得硫酸镍晶体时,需经过控制pH、
(5)硫酸镍可用来制备新型镍电池电极材料NiOOH,我国科研团队利用该电极材料设计了一种新型能量存储-转化装置(如图)。闭合K2、断开K1时,制氢并储能;断开K2、闭合K1时,供电。供电时,X电极反应式为

您最近一年使用:0次
解题方法
6 . 催化还原二氧化碳是解决温室效应及能源问题的重要手段之一,中国科学家设计出如图装置实现 的转化,电池总反应为:
的转化,电池总反应为: 。下列说法正确的是
。下列说法正确的是
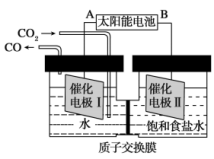
 的转化,电池总反应为:
的转化,电池总反应为: 。下列说法正确的是
。下列说法正确的是
| A.太阳能电池的正极为A极 |
| B.该装置工作时,质子通过交换膜由电极II移向电极I |
C.催化电极I的电极反应: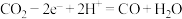 |
D.该装置不仅还原 ,还产生了具有经济附加值的次氯酸盐 ,还产生了具有经济附加值的次氯酸盐 |
您最近一年使用:0次
解题方法
7 . 燃料电池是一种连续的将燃料和氧化剂的化学能直接转化为电能的化学装置,氢气,氨、甲醇等气体或液体均可做燃料电池的燃料,具有广阔的发展前景。
(1)一种将燃料电池与电解池相组合的新工艺,可将高耗能的氯碱工业节能超过 。在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极均为惰性电极。所用的离子交换膜都只允许阳离子通过。
。在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极均为惰性电极。所用的离子交换膜都只允许阳离子通过。
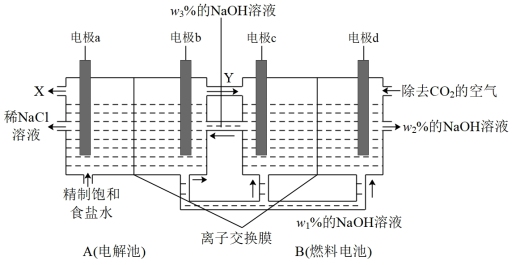
①X是___________ 。
②电池工作时电极a连接___________ (填“电极b”、“电极c”或“电极d”);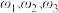 由大到小的顺序为
由大到小的顺序为___________ 。
③电极c的电极方程式为___________ 。
(2)甲烷碱性燃料电池提供电能,用电解法处理酸性含铬废水(主要含有 )时,铁板作阴、阳极,处理过程中发生反应:
)时,铁板作阴、阳极,处理过程中发生反应: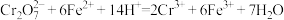 ,最后
,最后 以
以 形式除去。阳极电极反应式为
形式除去。阳极电极反应式为______ ,电解过程中废水的
_______ (填“变大”、“不变”或“变小”),当消耗甲烷 (标准状况)时最多有
(标准状况)时最多有______ g的 被还原。
被还原。
(1)一种将燃料电池与电解池相组合的新工艺,可将高耗能的氯碱工业节能超过
 。在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极均为惰性电极。所用的离子交换膜都只允许阳离子通过。
。在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极均为惰性电极。所用的离子交换膜都只允许阳离子通过。
①X是
②电池工作时电极a连接
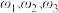 由大到小的顺序为
由大到小的顺序为③电极c的电极方程式为
(2)甲烷碱性燃料电池提供电能,用电解法处理酸性含铬废水(主要含有
 )时,铁板作阴、阳极,处理过程中发生反应:
)时,铁板作阴、阳极,处理过程中发生反应: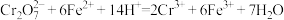 ,最后
,最后 以
以 形式除去。阳极电极反应式为
形式除去。阳极电极反应式为
 (标准状况)时最多有
(标准状况)时最多有 被还原。
被还原。
您最近一年使用:0次
8 . 锌离子电池成本低廉、安全性好,其原理如图,放电时电池总反应为:Zn+2MnO2=ZnMn2O4。下列说法错误的是
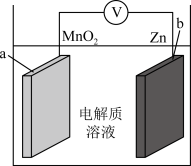

| A.放电时Zn2+由b极区向a极区迁移 |
| B.充电时b极发生还原反应 |
| C.放电时电路中转移1mol电子,a极理论增重65g |
| D.充电时a极反应为ZnMn2O4-2e-=Zn2++2MnO2 |
您最近一年使用:0次
9 . 电解原理在化学工业中有广泛应用。
(1)电解食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如图所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:
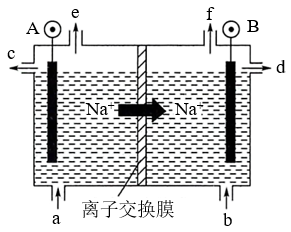
①电解饱和食盐水的总反应的离子方程式是___________ 。
②精制饱和食盐水在b口加入的物质为___________ (写化学式)
(2)全钒液流电池是一种新型的绿色环保储能系统,工作原理如图:
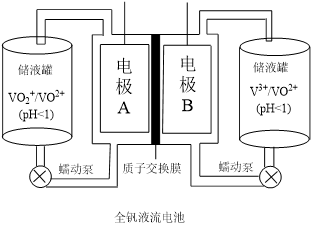
①全钒液流电池放电时V2+发生氧化反应,该电池放电时总反应式是___________ 。
②当完成储能时,阴极溶液的颜色是___________
(3)将PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示。
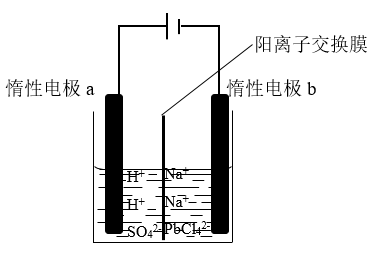
①写出电解时阴极的电极反应式___________
②电解过程中通过阳离子交换膜的离子主要为___________
③电解过程中,Na2PbCl4电解液浓度不断减小,为了恢复其浓度,应该向___________ 极室(填“阴”或者“阳”)加入___________ (填化学式)。
(1)电解食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如图所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:

①电解饱和食盐水的总反应的离子方程式是
②精制饱和食盐水在b口加入的物质为
(2)全钒液流电池是一种新型的绿色环保储能系统,工作原理如图:
| 离子种类 | VO | VO2+ | V3+ | V2+ |
| 颜色 | 黄色 | 蓝色 | 绿色 | 紫色 |

①全钒液流电池放电时V2+发生氧化反应,该电池放电时总反应式是
②当完成储能时,阴极溶液的颜色是
(3)将PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示。

①写出电解时阴极的电极反应式
②电解过程中通过阳离子交换膜的离子主要为
③电解过程中,Na2PbCl4电解液浓度不断减小,为了恢复其浓度,应该向
您最近一年使用:0次
2021-11-10更新
|
1575次组卷
|
8卷引用:山东省嘉祥县第一中学2022-2023学年高二上学期期末考试化学试题
山东省嘉祥县第一中学2022-2023学年高二上学期期末考试化学试题山东省实验中学2021-2022学年高二上学期期中化学试题山东省枣庄滕州市第一中学2022-2023学年高二上学期10月月考化学试题山东省新泰市第一中学2022-2023学年高二上学期期中考试化学试题(已下线)4.3.1 电解原理-2021-2022学年高二化学课后培优练(人教版选修4)第四章化学反应与电能福建省厦门集美中学2022-2023学年高二上学期第一次月考(10月)化学试题(已下线)专题突破卷07 化学反应与能量?-2024年高考化学一轮复习考点通关卷(新教材新高考)
名校
10 . 在如图串联装置中,通电片刻即发现乙装置左侧电极表面出现红色固体,则下列说法不正确的是


| A.标准状况下当甲中产生4.48L气体时,丙中Cu电极质量增加21.6g |
| B.电解过程中丙中溶液酸碱性无变化 |
| C.向甲中加入适量的盐酸,可使溶液恢复到电解前的状态 |
D.乙中左侧电极反应式: |
您最近一年使用:0次
2021-10-23更新
|
615次组卷
|
6卷引用:山东省枣庄一中分校2021-2022学年高二上学期期末考试化学试题
山东省枣庄一中分校2021-2022学年高二上学期期末考试化学试题安徽省六安第一中学2021-2022学年高二上学期期末考试化学试题福建省莆田市擢英中学2021-2022学年高二上学期第一次月考化学试卷黑龙江省大庆市东风中学2022-2023学年高二10月月考化学试题(已下线)专题31 多池串联的模型-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)专题09 串联电解池(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)



