名校
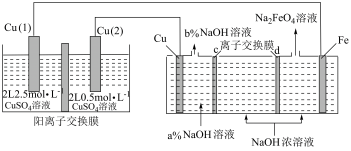
1 . 利用浓差电池制备高铁电池的重要材料 ,反应原理如图所示。下列说法错误的是
,反应原理如图所示。下列说法错误的是
 ,反应原理如图所示。下列说法错误的是
,反应原理如图所示。下列说法错误的是
A. |
B.c为阳离子交换膜,当Cu电极产生1mol气体时,有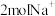 通过阳离子交换膜 通过阳离子交换膜 |
C.浓差电池放电过程中, 电极上的电极反应为 电极上的电极反应为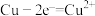 |
D.Fe电极的电极反应为: |
您最近一年使用:0次
2023-08-02更新
|
208次组卷
|
2卷引用:河北省邢台市襄都区等5地2022-2023学年高二上学期12月月考化学试题
解题方法
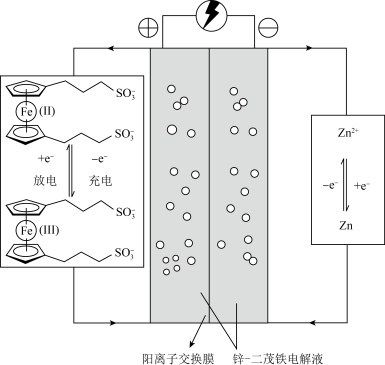
2 . 刘天骠教授团队开发出一种能应用于pH中性水系液流电池的双极性储能材料:锌-二茂铁【 】。工作原理如下图,箭头代表液体的流动方向。下列说法不正确的是
】。工作原理如下图,箭头代表液体的流动方向。下列说法不正确的是

 】。工作原理如下图,箭头代表液体的流动方向。下列说法不正确的是
】。工作原理如下图,箭头代表液体的流动方向。下列说法不正确的是

| A.双极性储能材料指既能做正极区的电解液又做负极区电解液 |
B.充电时,每生成1mol ,溶解32.5g锌 ,溶解32.5g锌 |
C.放电时的总反应为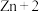 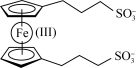  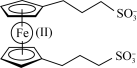 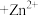 |
D.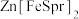 易溶于水是由于磺酸基能和水分子形成氢键 易溶于水是由于磺酸基能和水分子形成氢键 |
您最近一年使用:0次
名校
解题方法
3 . 下列说法正确的是
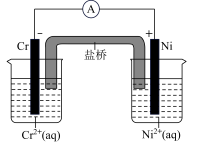

| A.铅蓄电池放电时的负极和充电时的阳极均发生还原反应 |
| B.钢铁水闸可用外加电流的阴极保护法防止其腐蚀 |
| C.从电解精炼铜的阳极泥中回收锌、金、银等金属 |
D.如图所示,可判断发生反应为 |
您最近一年使用:0次
2023-07-23更新
|
215次组卷
|
3卷引用:江苏省扬州市高邮市2022-2023学年高二上学期10月月考化学试题
解题方法
4 . 氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺节能超过30%。在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子交换膜都只允许阳离子通过。

(1)图中X、Y分别是_______ 、__________ 填化学式);X可用于制取84消毒液,请写出离子方程式________ 。
(2)燃料电池B中的负极反应式为:______ ,判断正极附近溶液的pH将______ (选择“增大”、“减小”、“不变”填空)。
(3)标准状况下,当A池中生成22.4L氢气时,电路中转移的电子数为__________ 。
(4)如图所示装置,用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。写出阳极上产生ClO2的电极反应式:________ 。


(1)图中X、Y分别是
(2)燃料电池B中的负极反应式为:
(3)标准状况下,当A池中生成22.4L氢气时,电路中转移的电子数为
(4)如图所示装置,用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。写出阳极上产生ClO2的电极反应式:

您最近一年使用:0次
名校
解题方法
5 . 电化学在生产、生活和科学研究中应用十分广泛,认识和研究化学能与电能相互转化的原理和规律具有重要意义。
(1)有机物的电化学合成是一种环境友好的化学合成方法,图1和图2中的电极相连时可实现电化学原理制取对氨基苯甲酸。
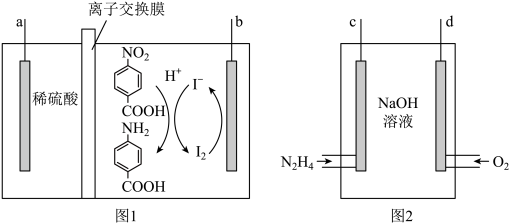
①图2为液态肼 燃料电池,c电极与
燃料电池,c电极与_______ (填“a”或“b”)相连,c电极发生的电极反应式为________ 。
②图1、图2相连时a电极为___________ (填“正”“负”“阴”或“阳”)极。生成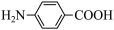 的离子方程式为
的离子方程式为___________ 。
③通过离子交换膜的离子是___________ (填离子符号);当电路中转移 电子时消耗标准状况下
电子时消耗标准状况下 体积
体积___________ ,电解池左室质量变化___________ g。
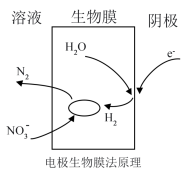
(2)氮氧化物和 排放易造成酸雨及水体污染,电极生物膜法能有效去除水体中的
排放易造成酸雨及水体污染,电极生物膜法能有效去除水体中的 ,进行生物的反硝化反应。其可能反应机理如图所示。用必要的化学用语及文字来描述此过程为
,进行生物的反硝化反应。其可能反应机理如图所示。用必要的化学用语及文字来描述此过程为___________ 。
(1)有机物的电化学合成是一种环境友好的化学合成方法,图1和图2中的电极相连时可实现电化学原理制取对氨基苯甲酸。

①图2为液态肼
 燃料电池,c电极与
燃料电池,c电极与②图1、图2相连时a电极为
 的离子方程式为
的离子方程式为③通过离子交换膜的离子是
 电子时消耗标准状况下
电子时消耗标准状况下 体积
体积(2)氮氧化物和
 排放易造成酸雨及水体污染,电极生物膜法能有效去除水体中的
排放易造成酸雨及水体污染,电极生物膜法能有效去除水体中的 ,进行生物的反硝化反应。其可能反应机理如图所示。用必要的化学用语及文字来描述此过程为
,进行生物的反硝化反应。其可能反应机理如图所示。用必要的化学用语及文字来描述此过程为
您最近一年使用:0次
2023-07-17更新
|
251次组卷
|
2卷引用:江苏省徐州市铜山区2022-2023学年高二上学期11月期中考试(选择考)化学试题
解题方法
6 . 电化学给人类的生活和工业生产带来极大的方便。回答下列问题:
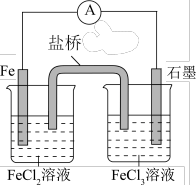
(1)如上图所示的电池,Fe作_______ 极(填“正”或“负”)。盐桥由琼脂和饱和KCl溶液构成,盐桥中的 往
往_______ (填“Fe”或“石墨”)电极移动。
(2)高铁电池是一种新型可充电电池,总反应为: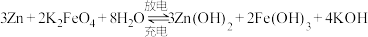 。
。
①放电时,负极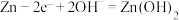 ,则正极电极反应为
,则正极电极反应为_______ 。
②充电时,阴极附近溶液的碱性_______ (填“增强”、“减弱”或“不变”)。
(3)甲烷燃料电池工作的示意图如下,其中A为铜电极,B为铁电极,C、D均为石墨电极。工作一段时间后,甲池中消耗甲烷0.05mol。

①乙池溶液的质量_______ (填“增大”、“减少”或“不变”)。
②丙池中C电极析出的气体在标准状况下的体积为_______ L。

(1)如上图所示的电池,Fe作
 往
往(2)高铁电池是一种新型可充电电池,总反应为:
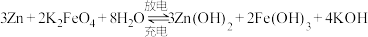 。
。①放电时,负极
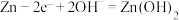 ,则正极电极反应为
,则正极电极反应为②充电时,阴极附近溶液的碱性
(3)甲烷燃料电池工作的示意图如下,其中A为铜电极,B为铁电极,C、D均为石墨电极。工作一段时间后,甲池中消耗甲烷0.05mol。

①乙池溶液的质量
②丙池中C电极析出的气体在标准状况下的体积为
您最近一年使用:0次
2023-07-16更新
|
212次组卷
|
2卷引用:福建省宁德市区域性学业质量检测2022-2023学年高二上学期2月期末考试化学试题
名校
7 . 我国科学家设计了一种高效电解水制氢的系统,实现了在催化剂作用下析氢和析氧反应分离。该系统的工作原理如图所示,其中电极均为惰性电极,电解液中含 。下列关于该装置工作时的说法正确的是
。下列关于该装置工作时的说法正确的是
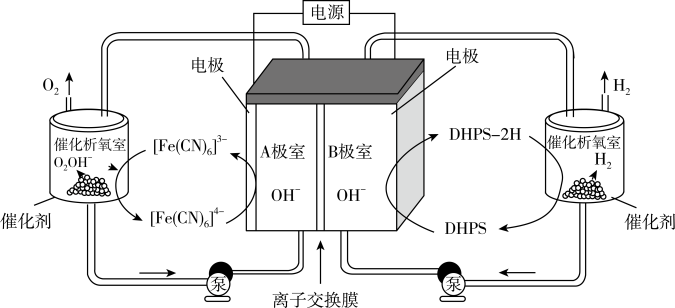
 。下列关于该装置工作时的说法正确的是
。下列关于该装置工作时的说法正确的是
| A.A电极与外电路的正极相连 |
| B.该装置中离子交换膜为质子交换膜 |
C.催化析氢室的反应为: |
D.理论上,该过程中溶液中 的浓度会不断减小 的浓度会不断减小 |
您最近一年使用:0次
名校
8 .  可采用“电解法”制备,装置如图所示。下列说法正确的是
可采用“电解法”制备,装置如图所示。下列说法正确的是
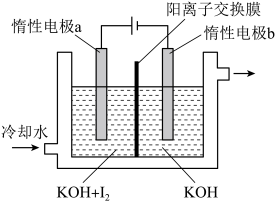
 可采用“电解法”制备,装置如图所示。下列说法正确的是
可采用“电解法”制备,装置如图所示。下列说法正确的是
A.惰性电极 有 有 生成 生成 |
| B.阳离子交换膜可以换成质子交换膜 |
C.电解过程中 通过由右往左通过阳离子交换膜 通过由右往左通过阳离子交换膜 |
D.电解时阳极的电极反应式: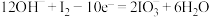 |
您最近一年使用:0次
名校
9 . 下列装置的线路接通后,经过一段时间,溶质质量增加的是
A.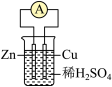 | B.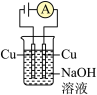 | C.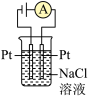 | D.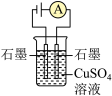 |
您最近一年使用:0次
解题方法
10 . 某课外小组设计如图1所示装置为电源对粗铜(含有Cu,少量Fe、Zn、Ag、Au等)进行精炼。
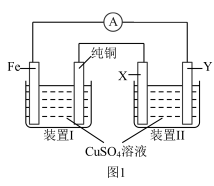
(1)装置Ⅰ中Fe电极上发生反应的电极反应式为___________ 。
(2)当反应一段时间后,经测量发现,Fe电极质量减少0.80 g,纯铜电极质量增重0.96 g,则实际经过电流表的电子的物质的量为___________ mol,装置Ⅰ的能量转化率为___________ 。(已知:装置Ⅰ中 足量)
足量)
(3)有同学提议,为避免副反应的发生,应将装置Ⅰ改为如图2所示装置,则溶液Z中溶质的化学式为___________ ,阴离子交换膜的作用为___________ (任写一条)。
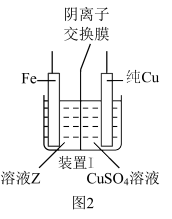
(4)装置Ⅱ中X电极材料的名称为___________ ,Y电极上的电极反应式为___________ ,一段时间后,装置Ⅱ溶液中阳离子主要为 和
和___________ 。

(1)装置Ⅰ中Fe电极上发生反应的电极反应式为
(2)当反应一段时间后,经测量发现,Fe电极质量减少0.80 g,纯铜电极质量增重0.96 g,则实际经过电流表的电子的物质的量为
 足量)
足量)(3)有同学提议,为避免副反应的发生,应将装置Ⅰ改为如图2所示装置,则溶液Z中溶质的化学式为

(4)装置Ⅱ中X电极材料的名称为
 和
和
您最近一年使用:0次



