解题方法
1 . 微生物燃料电池不仅可以获得高效能源,还能合成电子工业清洗剂四甲基氢氧化铵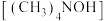 ,采用微生物燃料电池电渗析法合成
,采用微生物燃料电池电渗析法合成 的工作原理如图所示,下列说法正确的是
的工作原理如图所示,下列说法正确的是
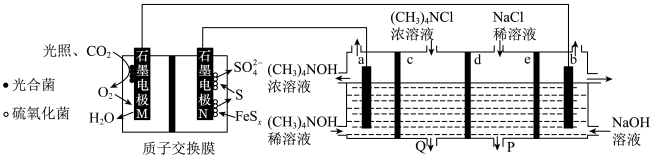
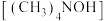 ,采用微生物燃料电池电渗析法合成
,采用微生物燃料电池电渗析法合成 的工作原理如图所示,下列说法正确的是
的工作原理如图所示,下列说法正确的是
| A.d为阴离子交换膜 |
B.电极M为正极,该电极上发生的电极反应为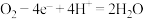 |
| C.电流方向为电极M→电极b→电极a→电极N |
D.制备1 mol  时,电极b处产生11.2 L(标准状况下)气体 时,电极b处产生11.2 L(标准状况下)气体 |
您最近一年使用:0次
解题方法
2 . 新型的高比能量锌-碘溴液流电池工作原理示意图如下。图中贮液器可储存电解质溶液,提高电池的容量,下列叙述正确的是
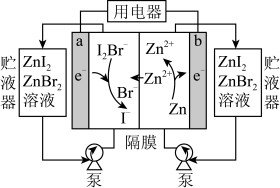

| A.放电时,a作电池的负极 |
B.放电时,a极区溶液中每增加 ,b电极将减少 ,b电极将减少 |
C.充电时,a电极反应为 |
| D.充电时,b电极接外电源正极 |
您最近一年使用:0次
名校
解题方法
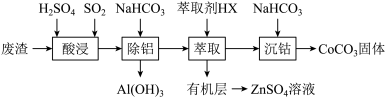
3 . 过渡金属催化的反应已成为重要的合成工具,贵金属成本高,会对环境造成不利影响,因此研究成本低廉的含锰、铁、钴、镍、铜等催化剂成为热点。以下是以含钴废渣(主要成分CoO、 ,还含有
,还含有 、ZnO等杂质)为原料制备
、ZnO等杂质)为原料制备 的一种工艺流程:
的一种工艺流程:
已知: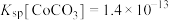 ,
,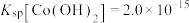
回答下列问题:
(1)“酸浸”时通入 的目的是
的目的是_______ 。
(2)“除铝”步骤中,铝离子发生的离子反应方程式_____________________ 。
(3)“萃取”过程可表示为, (水层)
(水层) (有机层)
(有机层)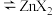 (有机层)
(有机层) (水层),从有机层获取
(水层),从有机层获取 ,下列试剂最好选择_______。
,下列试剂最好选择_______。
(4)“沉钴”的离子方程式是_____________________ 。“沉钴”步骤选择 ,而不选择
,而不选择 是为了避免有
是为了避免有 的生成,向溶液加入
的生成,向溶液加入 溶液,当溶液的pH达到8时,就会同时有
溶液,当溶液的pH达到8时,就会同时有 生成,计算当溶液的pH为8时,此时溶液中的
生成,计算当溶液的pH为8时,此时溶液中的 浓度
浓度______ mol/L。
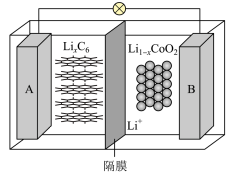
(5) 与纯碱反应可以制备重要的电极材料钴酸锂(
与纯碱反应可以制备重要的电极材料钴酸锂( )。一种充电电池的装置如图所示,充放电过程中,存在
)。一种充电电池的装置如图所示,充放电过程中,存在 与
与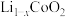 之间的转化,放电过程中
之间的转化,放电过程中 从A电极向B电极迁移,写出该电池放电时的正极反应:
从A电极向B电极迁移,写出该电池放电时的正极反应:_______ ,若用该电池为外接电源,惰性电极电解饱和氯化钠溶液,则电解饱和氯化钠溶液的离子方程式为___________ 。当通过隔膜的离子数目为 时,电解池阴极收集到的气体体积在标准状况下为
时,电解池阴极收集到的气体体积在标准状况下为_______ L。
 ,还含有
,还含有 、ZnO等杂质)为原料制备
、ZnO等杂质)为原料制备 的一种工艺流程:
的一种工艺流程:
已知:
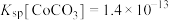 ,
,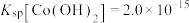
回答下列问题:
(1)“酸浸”时通入
 的目的是
的目的是(2)“除铝”步骤中,铝离子发生的离子反应方程式
(3)“萃取”过程可表示为,
 (水层)
(水层) (有机层)
(有机层)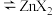 (有机层)
(有机层) (水层),从有机层获取
(水层),从有机层获取 ,下列试剂最好选择_______。
,下列试剂最好选择_______。| A.稀硫酸 | B.NaOH溶液 | C.HX | D.水 |
 ,而不选择
,而不选择 是为了避免有
是为了避免有 的生成,向溶液加入
的生成,向溶液加入 溶液,当溶液的pH达到8时,就会同时有
溶液,当溶液的pH达到8时,就会同时有 生成,计算当溶液的pH为8时,此时溶液中的
生成,计算当溶液的pH为8时,此时溶液中的 浓度
浓度(5)
 与纯碱反应可以制备重要的电极材料钴酸锂(
与纯碱反应可以制备重要的电极材料钴酸锂( )。一种充电电池的装置如图所示,充放电过程中,存在
)。一种充电电池的装置如图所示,充放电过程中,存在 与
与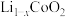 之间的转化,放电过程中
之间的转化,放电过程中 从A电极向B电极迁移,写出该电池放电时的正极反应:
从A电极向B电极迁移,写出该电池放电时的正极反应: 时,电解池阴极收集到的气体体积在标准状况下为
时,电解池阴极收集到的气体体积在标准状况下为
您最近一年使用:0次
名校
4 . 如图是一个化学过程的示意图。已知甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O请回答:
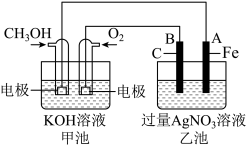
(1)甲池是_______ (填“原电池”或“电解池”),通入O2的电极作为_______ 极,该电极反应式为_______ 。
(2)乙池是_______ (填“原电池”或“电解池”),B电极名称为_______ 极,电极反应式为_______ 。
(3)甲池中溶液的pH_______ (填“增大”、“减小”或“不变”);乙池中溶液的pH_______ (填“增大”、“减小”或“不变”)。
(4)当乙池中A(Fe)极的质量增加5.40g时,电路中转移电子的物质的量是_______ mol,甲池中理论上消耗O2_______ mL(标准状况下)。

(1)甲池是
(2)乙池是
(3)甲池中溶液的pH
(4)当乙池中A(Fe)极的质量增加5.40g时,电路中转移电子的物质的量是
您最近一年使用:0次
5 . 锂离子电池具有比能量大、用途广等特点。如图为一种锂离子电池的结构示意图,电池反应式为LixC6+Li1-xCoO2 C6+LiCoO2(x<1)。下列说法正确的是
C6+LiCoO2(x<1)。下列说法正确的是

 C6+LiCoO2(x<1)。下列说法正确的是
C6+LiCoO2(x<1)。下列说法正确的是
| A.充电时,a电极发生Li+脱嵌,放电时发生Li+嵌入 |
| B.放电时电解质中Li+数目减少 |
C.放电时若转移0.02mol电子, 电极将增重0.14g 电极将增重0.14g |
| D.充电时a极接外电源的负极 |
您最近一年使用:0次
名校
解题方法
6 . 全固态锂电池以比容量高、安全、轻便等优势成为电动汽车的理想电池。近期,研究者以硅和石墨为基体,分别负载 Li 和 S 作为电池电极,以 Li3PS4为固体电解质进行充放电实验,发现该 Li-S电池具有高离子电导率。该电池的装置如图所示,下列说法正确的是
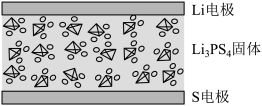

| A.Li 和 S无需基体负载,也能正常放电产生电流 |
| B.充电时,阴极电极反应式为:S+2e-+ 2Li+=Li2S |
| C.放电时,Li+从Li电极经 Li3PS4固体电解质迁移到 S 电极 |
| D.用该电池电解饱和食盐水时,若生成 22.4LH2,则需要消耗 14 g Li |
您最近一年使用:0次
2023-04-24更新
|
213次组卷
|
2卷引用:河南省洛阳市新安县第一高级中学2022-2023学年高三上学期12月线上考试(实验班)化学试题
名校
解题方法
7 . 基于硫化学的金属硫电池有望替代当前锂离子电池技术,满足人类社会快速增长的能源需求,该电池的结构及原理如图所示。

下列有关叙述正确的是

下列有关叙述正确的是
A.该电池可采用含 的水溶液或有机物为电解质溶液 的水溶液或有机物为电解质溶液 |
| B.放电时,电子的移动方向:电极a→电极b→隔膜→电极a |
C.充电时,阳极区可能发生的反应有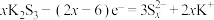 |
D.充电时。电路中转移 时,阴极质量减重78g 时,阴极质量减重78g |
您最近一年使用:0次
2023-04-07更新
|
1024次组卷
|
14卷引用:山东省济南市2022-2023学年高三上学期期中考试化学试题
山东省济南市2022-2023学年高三上学期期中考试化学试题(已下线)化学反应与电能——课时2化学电源湖南省长沙市雅礼中学2022-2023学年高三下学期4月份第八次月考化学试题湖南省长沙市雅礼中学2022-2023学年高三下学期4月份第八次月考化学试题(已下线)仿真卷06-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)山西省吕梁市孝义市2022-2023学年高二下学期期中考试化学试题河南省安阳市新乡鹤壁2022-2023学年高二下学期5月份联考化学试题四川省成都市树德中学2022-2023学年高二下学期5月月考化学试题湖北省武汉市武昌区2022-2023学年高二下学期期末质量检测化学试题河北省昌黎第一中学2022-2023学年高二下学期期末考试化学试题山东省青岛第一中学2023-2024学年高二上学期10月月考化学试题内蒙古自治区鄂尔多斯市第一中学2023-2024学年高三上学期12月阶段性测试理科综合试题(已下线)题型03 新型化学电池-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)黑龙江省大庆实验中学实验二部2023-2024学年高二上学期期末考试化学试题
名校
解题方法
8 . Ⅰ.当今社会的主题之一:发展经济,节能减排。而燃料电池因其无污染,且原料来源广可再生被人们青睐,广泛应用于生产、生活、科学研究中,现有如下图所示装置,所有电极均为Pt,请按要求回答下列问题:

(1)写出a极的电极反应_______ 。
(2)当b极消耗标准状况下的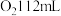 时,若乙中硫酸铜溶液的体积是200mL,假若电解前后溶液体积保持不变,此时乙池中的
时,若乙中硫酸铜溶液的体积是200mL,假若电解前后溶液体积保持不变,此时乙池中的
_______ 。
(3)若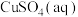 足够,电解一段时间后,要恢复到原来的状态,则可加入_______。(填序号)
足够,电解一段时间后,要恢复到原来的状态,则可加入_______。(填序号)
(4)现用丙装置电解硫酸钾溶液制取氢气、氧气、硫酸和氢氧化钾,其中M、N为离子交换膜,只允许某些离子通过,M为_______ 离子交换膜(填“阴”或“阳”)。
Ⅱ.下图为青铜器在潮湿环境中发生的电化学腐蚀的示意图。
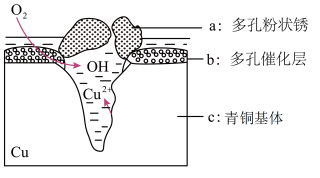
(5)环境中的 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔铜锈
扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔铜锈 ,其离子方程式为
,其离子方程式为_______ 。
(6)若生成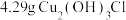 ,则理论上耗氧体积为
,则理论上耗氧体积为_______ L(标准状况)。

(1)写出a极的电极反应
(2)当b极消耗标准状况下的
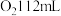 时,若乙中硫酸铜溶液的体积是200mL,假若电解前后溶液体积保持不变,此时乙池中的
时,若乙中硫酸铜溶液的体积是200mL,假若电解前后溶液体积保持不变,此时乙池中的
(3)若
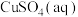 足够,电解一段时间后,要恢复到原来的状态,则可加入_______。(填序号)
足够,电解一段时间后,要恢复到原来的状态,则可加入_______。(填序号)A. | B. | C. | D. |
Ⅱ.下图为青铜器在潮湿环境中发生的电化学腐蚀的示意图。

(5)环境中的
 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔铜锈
扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔铜锈 ,其离子方程式为
,其离子方程式为(6)若生成
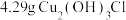 ,则理论上耗氧体积为
,则理论上耗氧体积为
您最近一年使用:0次
2023-03-18更新
|
98次组卷
|
3卷引用:四川省乐山市沫若中学2021-2022学年高二下学期第二次月考化学试题
名校
解题方法
9 . 有机物电极材料具有来源丰富、可降解等优点,一种负极材料为固态聚酰亚胺-水系二次电池的结构如图所示。下列说法正确的是
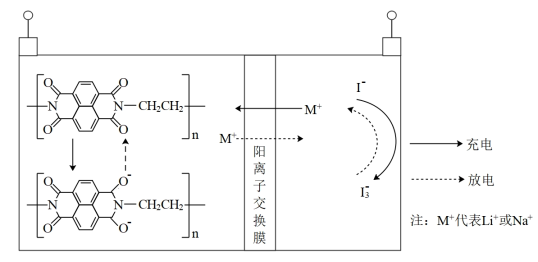

| A.充电时有机电极发生了氧化反应 |
B.将 由 由 换成 换成 ,电池的比能量会下降 ,电池的比能量会下降 |
C.充电时每转移 ,右室离子数目减少 ,右室离子数目减少 |
D.放电时负极电极反应为: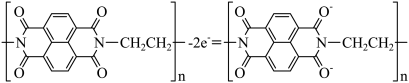 |
您最近一年使用:0次
名校
解题方法
10 . 2019年诺贝尔化学奖授予锂离子电池的发明者, 是锂离子电池的正极材料。用含锂废渣(主要元素的含量:As 5.40%、
是锂离子电池的正极材料。用含锂废渣(主要元素的含量:As 5.40%、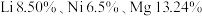 )制备
)制备 ,并用其制备
,并用其制备 。部分工艺流程如图(该流程可能造成水体砷污染):
。部分工艺流程如图(该流程可能造成水体砷污染):
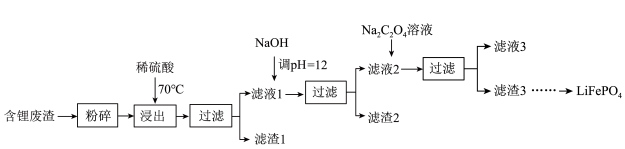
已知:室温下测得滤液1、滤液2中部分离子的浓度如下表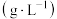 :
:
Ⅰ.制备
(1)处理废渣时粉碎的作用是____________________________________ 。
(2)滤渣2的主要成分(填化学式)_________________ ,滤液3可回收的物质是___________ 。
(3)下列有关说法正确的是__________ 。
A. 中铁元素的化合价为+2价 B.流程中可以直接循环利用的物质为稀硫酸
中铁元素的化合价为+2价 B.流程中可以直接循环利用的物质为稀硫酸
C.室温下 的
的 等于
等于 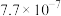
(4)将 和
和 置于高温下反应,生成
置于高温下反应,生成 和一种温室气体,该反应的化学方程式是
和一种温室气体,该反应的化学方程式是__________________ 。
II、如图是一个电化学过程的示意图。请回答下列问题:
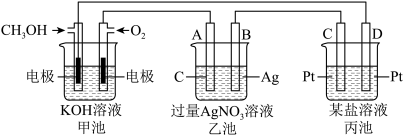
(5)写出通入CH3OH的电极的电极反应式____________ 。
(6)乙池中反应的化学方程式___________ 。
 是锂离子电池的正极材料。用含锂废渣(主要元素的含量:As 5.40%、
是锂离子电池的正极材料。用含锂废渣(主要元素的含量:As 5.40%、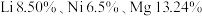 )制备
)制备 ,并用其制备
,并用其制备 。部分工艺流程如图(该流程可能造成水体砷污染):
。部分工艺流程如图(该流程可能造成水体砷污染):
已知:室温下测得滤液1、滤液2中部分离子的浓度如下表
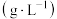 :
: |  |  | |
| 滤液1 | 22.72 | 20.68 | 60.18 |
| 滤液2 | 21.94 | 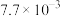 | 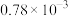 |
Ⅰ.制备

(1)处理废渣时粉碎的作用是
(2)滤渣2的主要成分(填化学式)
(3)下列有关说法正确的是
A.
 中铁元素的化合价为+2价 B.流程中可以直接循环利用的物质为稀硫酸
中铁元素的化合价为+2价 B.流程中可以直接循环利用的物质为稀硫酸C.室温下
 的
的 等于
等于 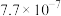
(4)将
 和
和 置于高温下反应,生成
置于高温下反应,生成 和一种温室气体,该反应的化学方程式是
和一种温室气体,该反应的化学方程式是II、如图是一个电化学过程的示意图。请回答下列问题:

(5)写出通入CH3OH的电极的电极反应式
(6)乙池中反应的化学方程式
您最近一年使用:0次



