名校
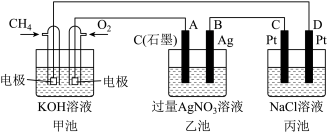
1 . 下图是一个化学过程的示意图,请回答下列问题:___________ 装置,乙池是___________ 装置。
(2)通入O2的电极的电极反应式为___________ ,通入CH4的电极的电极反应式为___________ 。
(3)乙池中反应的化学方程式为___________ 。
(4)一段时间后,当丙中共产生112ml(标准状况)气体时,均匀搅拌丙池,所得溶液在室温时的pH=___________ (已知NaCl溶液足量,电解后溶液体积为500ml),若要使丙池恢复电解前的状态,应向丙池通入___________ (填化学式)
(5)在A、B、C、D各电极上析出生成物的物质的量之比为___________ 。
(2)通入O2的电极的电极反应式为
(3)乙池中反应的化学方程式为
(4)一段时间后,当丙中共产生112ml(标准状况)气体时,均匀搅拌丙池,所得溶液在室温时的pH=
(5)在A、B、C、D各电极上析出生成物的物质的量之比为
您最近一年使用:0次
2024-02-10更新
|
119次组卷
|
2卷引用:宁夏青铜峡市宁朔中学2023-2024学年高二上学期期末考试化学试题
名校
解题方法
2 . 电池的发明和应用是化学家们对人类社会的重要贡献之一、每一次化学电池技术的突破,都带来了电子设备革命性的发展。最近,我国在甲烷燃料电池的相关技术上获得了新突破,原理如下图所示:

(1)通甲烷燃料一极的电极反应式为_______ 。
(2)以石墨做电极电解Na2SO4溶液,如图2所示,电解开始后先出现红色的一极的电极反应式为_______ 。
(3)随着电池使用范围的日益扩大,废旧电池潜在的污染已引起社会各界的广泛关注。工业上为了处理含有 的酸性工业废水,用绿矾(FeSO4·7H2O)把废水中的六价铬离子还原成三价铬离子,再加入过量的石灰水,使铬离子转变为Cr(OH)3沉淀。
的酸性工业废水,用绿矾(FeSO4·7H2O)把废水中的六价铬离子还原成三价铬离子,再加入过量的石灰水,使铬离子转变为Cr(OH)3沉淀。
①氧化还原过程的离子方程式为_______ 。
②常温下,Cr(OH)3的溶度积Ksp=1×10-32 mol4·L-4,溶液的pH至少为_______ ,才能使Cr3+沉淀完全(溶液中离子浓度小于10-5 mol/L时,可视为完全沉淀)。
(4)人工肾脏可采用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图。
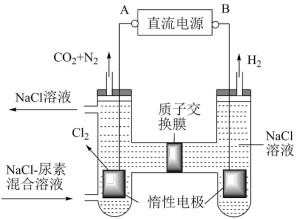
①电源的正极为_______ (填“A”或“B”)。
②电解结束后,阴极室溶液的pH与电解前相比将_______ (填“增大”、“减小”、“不变”);若收集到H2 2.24L(标准状况),则通过质子交换膜的H+数目为_______ (忽略气体的溶解)。

(1)通甲烷燃料一极的电极反应式为
(2)以石墨做电极电解Na2SO4溶液,如图2所示,电解开始后先出现红色的一极的电极反应式为
(3)随着电池使用范围的日益扩大,废旧电池潜在的污染已引起社会各界的广泛关注。工业上为了处理含有
 的酸性工业废水,用绿矾(FeSO4·7H2O)把废水中的六价铬离子还原成三价铬离子,再加入过量的石灰水,使铬离子转变为Cr(OH)3沉淀。
的酸性工业废水,用绿矾(FeSO4·7H2O)把废水中的六价铬离子还原成三价铬离子,再加入过量的石灰水,使铬离子转变为Cr(OH)3沉淀。①氧化还原过程的离子方程式为
②常温下,Cr(OH)3的溶度积Ksp=1×10-32 mol4·L-4,溶液的pH至少为
(4)人工肾脏可采用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图。

①电源的正极为
②电解结束后,阴极室溶液的pH与电解前相比将
您最近一年使用:0次
名校
3 . 全钒氧化还原液流电池是一种新型绿色的二次电池,其放电时的工作原理为 。用铅蓄电池对其进行充电时,与铅电板相连的一极生成的物质是
。用铅蓄电池对其进行充电时,与铅电板相连的一极生成的物质是
 。用铅蓄电池对其进行充电时,与铅电板相连的一极生成的物质是
。用铅蓄电池对其进行充电时,与铅电板相连的一极生成的物质是A. | B.V2+ | C.VO2+ | D.V3+ |
您最近一年使用:0次
名校
4 . 利用光伏电池与膜电解法制备Ce(SO4)2溶液的装置如图所示,下列说法不正确的是
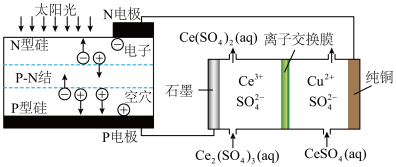

| A.该光伏电池的P电极为正极 |
| B.电解池中纯铜为阴极,其电极反应式为Cu2+ +2e- =Cu |
C.该离子交换膜为阴离子交换膜,  由左池向右池迁移 由左池向右池迁移 |
| D.电路中有0.1mol电子通过时,阳极室生成33.2g Ce(SO4)2 |
您最近一年使用:0次
名校
解题方法
5 . 将图1所示的装置中盐桥换成铜导线与两石墨棒连接得到图2所示装置,并将NaCl溶液换为HCl溶液,发现电流表指针仍然有偏转,下列说法正确的是
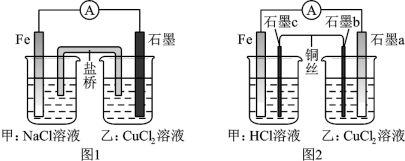
A.图2中乙装置总反应的离子方程式: |
| B.两图都是将化学能转变成电能的装置 |
| C.图1盐桥中的阳离子移向甲装置 |
| D.图2中电子流向为Fe→电流计→石墨a→石墨b→石墨c→Fe |
您最近一年使用:0次
2023-03-31更新
|
421次组卷
|
3卷引用:宁夏石嘴山市第三中学2022-2023学年高二下学期第一次月考化学(理)试题
名校
解题方法
6 . 按照要求回答下列问题。
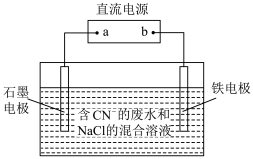
(1)工业上,在强碱性条件下用电解法除去废水中的 ,装置如图所示,依次发生的反应有:
,装置如图所示,依次发生的反应有:
i.
ii.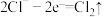
iii.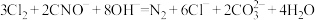
①a为电源_______ 极。
②通电过程中溶液pH不断_______ (填“增大”“减小”或“不变”)。
③除去1mol ,外电路中至少需要转移
,外电路中至少需要转移_______ mol电子。
④为了使电解池连续工作,需要不断补充_______ 。
(2)用NaOH溶液吸收烟气中的 ,将所得的
,将所得的 溶液进行电解,可循环再生NaOH,同时得到
溶液进行电解,可循环再生NaOH,同时得到 ,其原理如图所示(电极材料为石墨)。
,其原理如图所示(电极材料为石墨)。
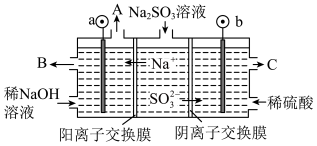
① C口流出的物质是_______ 。
② 放电的电极反应式为
放电的电极反应式为_______ 。
③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因:_______ 。
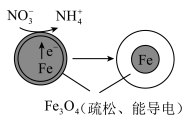
(3)用零价铁(Fe)去除水体中的硝酸盐( )已成为环境修复研究的热点之一、Fe还原水体中的
)已成为环境修复研究的热点之一、Fe还原水体中的 的反应原理如图所示。正极的电极反应式是
的反应原理如图所示。正极的电极反应式是_______ 。
(1)工业上,在强碱性条件下用电解法除去废水中的
 ,装置如图所示,依次发生的反应有:
,装置如图所示,依次发生的反应有:
i.

ii.
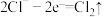
iii.
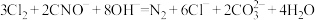
①a为电源
②通电过程中溶液pH不断
③除去1mol
 ,外电路中至少需要转移
,外电路中至少需要转移④为了使电解池连续工作,需要不断补充
(2)用NaOH溶液吸收烟气中的
 ,将所得的
,将所得的 溶液进行电解,可循环再生NaOH,同时得到
溶液进行电解,可循环再生NaOH,同时得到 ,其原理如图所示(电极材料为石墨)。
,其原理如图所示(电极材料为石墨)。
① C口流出的物质是
②
 放电的电极反应式为
放电的电极反应式为③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因:
(3)用零价铁(Fe)去除水体中的硝酸盐(
 )已成为环境修复研究的热点之一、Fe还原水体中的
)已成为环境修复研究的热点之一、Fe还原水体中的 的反应原理如图所示。正极的电极反应式是
的反应原理如图所示。正极的电极反应式是
您最近一年使用:0次
名校
7 . 高铁酸钠 (Na2FeO4)是一种新型绿色水处理剂。工业上可用电解浓 溶液制备
溶液制备 ,其工作原理如图所示,两端隔室中离子不能进入中间隔室。下列说法错误的是
,其工作原理如图所示,两端隔室中离子不能进入中间隔室。下列说法错误的是

 溶液制备
溶液制备 ,其工作原理如图所示,两端隔室中离子不能进入中间隔室。下列说法错误的是
,其工作原理如图所示,两端隔室中离子不能进入中间隔室。下列说法错误的是
A.阳极反应式: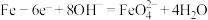 |
| B.甲溶液可循环利用 |
| C.离子交换膜a是阳离子交换膜 |
D.当电路中通过 电子时, 电子时, 电极会有 电极会有 生成 生成 |
您最近一年使用:0次
名校
解题方法
8 . 现以CO、O2、熔熔盐Z(Na2CO3)组成的燃料电池,采用电解法制备N2O5,装置如图所示,其中Y为CO2,下列说法正确的是
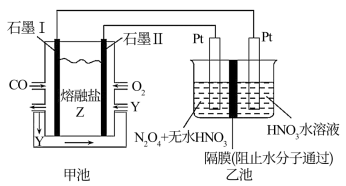

| A.甲池石墨I是原电池的正极,发生氧化反应 |
B.甲池石墨II发生的电极反应:O2 +4e- +2CO2 = 2CO |
| C.乙池中左端Pt极电极反应式:N2O4-2e-+H2O=N2O5+2H+ |
| D.若甲池消耗氧气 2.24L(标准状况),则乙池中产生氢气0.1mol |
您最近一年使用:0次
2023-02-06更新
|
140次组卷
|
2卷引用:宁夏石嘴山市平罗中学2022-2023学年高二下学期3月月考化学试题
解题方法
9 . 某课外活动小组用如图所示装置进行实验,试回答下列问题:
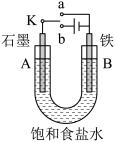
(1)若开始时开关K与a连接,则B极的电极反应式为_______ 。
(2)若开始时开关K与b极连接,此装置为______ (原电池或电解池)总反应的离子方程式为_______ 。
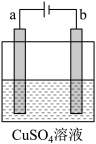
(3)如图所示用惰性电极电解100 mL 0.5 mol·L 硫酸铜溶液,a电极上的电极反应式为
硫酸铜溶液,a电极上的电极反应式为_______ ,若a电极产生56 mL(标准状况)气体,则所得溶液的
_______ (不考虑溶液体积变化)。

(1)若开始时开关K与a连接,则B极的电极反应式为
(2)若开始时开关K与b极连接,此装置为
(3)如图所示用惰性电极电解100 mL 0.5 mol·L
 硫酸铜溶液,a电极上的电极反应式为
硫酸铜溶液,a电极上的电极反应式为

您最近一年使用:0次
名校
10 . 某新型可充电电池,能长时间保持稳定的放电电压,该电池的总反应 。
。
(1)放电时负极反应为___________ ;
(2)充电时Fe(OH)3发生___________ 反应;
(3)放电时电子由___________ 极流向___________ 极;
(4)放电时1 mol K2FeO4发生反应,转移电子数是___________ 。
 。
。(1)放电时负极反应为
(2)充电时Fe(OH)3发生
(3)放电时电子由
(4)放电时1 mol K2FeO4发生反应,转移电子数是
您最近一年使用:0次



