1 . I.化学电源在生产生活中有着广泛的应用,请回答下列问题。
(1)根据构成原电池的本质判断,下列化学反应方程式正确且能够设计原电池的是_______
(2)为了探究化学反应中的能量变化,某同学设计了如下两个实验(如图)。有关实验现象,下列说法正确的是:_______

II.以氨气替代氢气研发氨燃料电池是当前科研的一个热点。
(3)氨燃料电池使用的电解质溶液是2mol/L的KOH溶液,电池反应为:4NH3 + 3O2 = 2N2 + 6H2O,该电池负极的电极反应为:_______
(4)以上述氨燃料电池接下图A.B两极(C、D、E、F都是惰性电极)。电源接通后,F极附近溶液呈红色,请回答:甲池中电极C名称为:_______ ,乙池中发生的离子反应方程式为:_______ ,丙装置是验证外加电流法对钢铁设备的保护(电解液为盐酸酸化的氯化钠溶液),钢铁应该接在_______ 处(填G或H)。为证明铁被保护,可先取少量的电解后的溶液于试管中,向溶液中加入_______ 溶液观察颜色变化。

(1)根据构成原电池的本质判断,下列化学反应方程式正确且能够设计原电池的是_______
| A.KOH + HCl =KCl + H2O | B.Cu + FeCl3 = FeCl2 + CuCl2 |
| C.Na2O + H2O = 2NaOH | D.Fe+ H2SO4=FeSO4 +H2↑ |

| A.图I中温度计的示数高于图II的示数 |
| B.图I和图II中温度计的示数相等,且均高于室温 |
| C.图I和图II中的气泡均产生于锌棒表面 |
| D.图II中产生气体的速率比I慢 |
II.以氨气替代氢气研发氨燃料电池是当前科研的一个热点。
(3)氨燃料电池使用的电解质溶液是2mol/L的KOH溶液,电池反应为:4NH3 + 3O2 = 2N2 + 6H2O,该电池负极的电极反应为:
(4)以上述氨燃料电池接下图A.B两极(C、D、E、F都是惰性电极)。电源接通后,F极附近溶液呈红色,请回答:甲池中电极C名称为:

您最近一年使用:0次
2022-09-13更新
|
371次组卷
|
2卷引用:广东省广州市番禺区2021-2022学年高二上学期期末考试化学试题
解题方法
2 . 水系钠离子电池有成本低、寿命长、环保等诸多优势,未来有望代替锂离子电池和铅酸电池。一种水系钠离子电池放电和充电的工作原理示意图如图所示。下列说法错误的是


| A.放电时,光可以促进电子转移 |
| B.放电时,工作一段时间,M电极区Na+浓度减小 |
| C.充电时,M极发生还原反应 |
D.充电时,阳极的电极反应式为3I--2e-= |
您最近一年使用:0次
名校
解题方法
3 . 高纯镓是制备第三代半导体的重要原料,其化学性质与铝相似。下图为工业精炼镓的装置示意图。下列说法不正确的是

A.阴极的电极反应为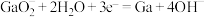 |
B.电解过程中,阳极室中 的物质的量减小 的物质的量减小 |
C.电路中每转移 电子,理论上粗镓熔融液减少 电子,理论上粗镓熔融液减少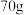 |
D.电解后粗镓中的 以离子形式进入 以离子形式进入 溶液中 溶液中 |
您最近一年使用:0次
2024-03-01更新
|
680次组卷
|
5卷引用:广东省广州市第二中学2023-2024学年高三上学期期末化学试卷
广东省广州市第二中学2023-2024学年高三上学期期末化学试卷(已下线)通关练09 重温“两池”原理及应用-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)吉林省长春市东北师范大学附属中学2024届高三下学期第五次模拟考试化学试题河南省漯河市高级中学2023-2024学年高三下学期5月月考化学试题黑龙江省哈尔滨工业大学附属中学校2024届高三下学期五模化学试题
解题方法
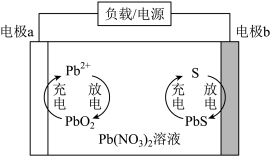
4 . 一种由我国科学家研发的水系 电池的结构及工作原理如图所示,其中电极
电池的结构及工作原理如图所示,其中电极 为碳电极,电极
为碳电极,电极 为掺有硫单质的碳电极。下列说法不正确的是
为掺有硫单质的碳电极。下列说法不正确的是
 电池的结构及工作原理如图所示,其中电极
电池的结构及工作原理如图所示,其中电极 为碳电极,电极
为碳电极,电极 为掺有硫单质的碳电极。下列说法不正确的是
为掺有硫单质的碳电极。下列说法不正确的是
A.放电时,电极 为负极 为负极 |
B.充电时,电极 发生反应: 发生反应: |
C.放电时,电极 附近溶液的 附近溶液的 逐渐减小 逐渐减小 |
D.充电时,每转移 电子,阴极质量理论上减少 电子,阴极质量理论上减少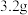 |
您最近一年使用:0次
解题方法
5 . 我国将在2030年前实现碳达峰、2060年前实现碳中和。 的资源化利用能有效减少
的资源化利用能有效减少 排放,某研究小组利用工业废气中的
排放,某研究小组利用工业废气中的 在催化剂的作用下合成甲醇,发生反应:
在催化剂的作用下合成甲醇,发生反应:
已知:Ⅰ.
Ⅱ.
(1)根据以上化学反应方程式,计算反应热
_______ 。
(2)下列有关合成甲醇的说法中正确的是_______(填标号)。
(3)反应温度和催化剂组成与反应物 的转化率和产物甲醇的选择性高度相关。改变温度和催化剂组成,控制其他条件相同进行四组实验,得到的实验数据如下表所示:
的转化率和产物甲醇的选择性高度相关。改变温度和催化剂组成,控制其他条件相同进行四组实验,得到的实验数据如下表所示:
注:“甲醇选择性”是指生成甲醇的二氧化碳占所有参与反应的二氧化碳的百分比。
结合表中数据可知,用 生产甲醇的最优条件为
生产甲醇的最优条件为_______ (填实验编号)。
(4)下图为一定温度下, 时,氢气的转化率
时,氢气的转化率 与投料比
与投料比
 的关系图像,请在图中画出相同温度下,压强为
的关系图像,请在图中画出相同温度下,压强为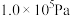 时对应的变化曲线。
时对应的变化曲线。_________

(5)某研究小组采用甲醇燃料电池,以石墨为电极材料进行电解饱和NaCl溶液的实验,装置如图所示:

①甲醇燃料电池工作时,甲醇应由_______ (填“a”或“b”)口通入。该燃料电池的正极反应式为_______ 。
②电解一段时间后,c1、c2电极上均有气体产生,其中c2电极上得到的是_______ ,电解NaCl溶液的离子方程式为_______ 。
 的资源化利用能有效减少
的资源化利用能有效减少 排放,某研究小组利用工业废气中的
排放,某研究小组利用工业废气中的 在催化剂的作用下合成甲醇,发生反应:
在催化剂的作用下合成甲醇,发生反应:
已知:Ⅰ.

Ⅱ.

(1)根据以上化学反应方程式,计算反应热

(2)下列有关合成甲醇的说法中正确的是_______(填标号)。
| A.增大氢气的浓度,有利于提高甲醇的产率 |
| B.选择合适的催化剂,有利于平衡正向移动 |
| C.低温有利于平衡正向移动,因此实际生产中温度越低越好 |
| D.高压有利于平衡正向移动,因此实际生产中压强越高越好 |
 的转化率和产物甲醇的选择性高度相关。改变温度和催化剂组成,控制其他条件相同进行四组实验,得到的实验数据如下表所示:
的转化率和产物甲醇的选择性高度相关。改变温度和催化剂组成,控制其他条件相同进行四组实验,得到的实验数据如下表所示:| 实验编号 | 温度/℃ | 催化剂组成 |  转化率/% 转化率/% | 甲醇选择性/% |
| 甲 | 250 | 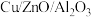 | 12.3 | 42.3 |
| 乙 | 250 | 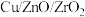 | 30.3 | 87.2 |
| 丙 | 300 | 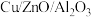 | 15.3 | 38.5 |
| 丁 | 300 | 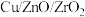 | 30.5 | 60.2 |
结合表中数据可知,用
 生产甲醇的最优条件为
生产甲醇的最优条件为(4)下图为一定温度下,
 时,氢气的转化率
时,氢气的转化率 与投料比
与投料比
 的关系图像,请在图中画出相同温度下,压强为
的关系图像,请在图中画出相同温度下,压强为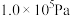 时对应的变化曲线。
时对应的变化曲线。
(5)某研究小组采用甲醇燃料电池,以石墨为电极材料进行电解饱和NaCl溶液的实验,装置如图所示:

①甲醇燃料电池工作时,甲醇应由
②电解一段时间后,c1、c2电极上均有气体产生,其中c2电极上得到的是
您最近一年使用:0次
名校
6 . 电解 溶液的装置如图所示,a、b均为惰性电极。下列说法不正确的是
溶液的装置如图所示,a、b均为惰性电极。下列说法不正确的是

 溶液的装置如图所示,a、b均为惰性电极。下列说法不正确的是
溶液的装置如图所示,a、b均为惰性电极。下列说法不正确的是
A.a极上发生的反应为: |
B. 移向b极 移向b极 |
C.转移2 mol  ,理论上阳极产生11.2 L气体(标准状况下) ,理论上阳极产生11.2 L气体(标准状况下) |
D.电解总反应: |
您最近一年使用:0次
解题方法
7 . 工业上 加氢制
加氢制 ,为
,为 的减排与再利用提供了一种新策略,该过程中存在如下反应:
的减排与再利用提供了一种新策略,该过程中存在如下反应:
反应Ⅰ:
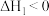
反应Ⅱ:

回答下列问题:
(1)已知: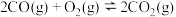

则反应

_______ (用含 、
、 、
、 的代数式表示)。
的代数式表示)。
(2)关于反应Ⅰ,下列说法正确的有_______(填标号)。
(3)向恒压密闭装置中充入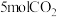 和
和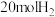 ,在不同温度下同时发生反应Ⅰ和Ⅱ,达平衡时,测得
,在不同温度下同时发生反应Ⅰ和Ⅱ,达平衡时,测得 和
和 的物质的量
的物质的量 随温度
随温度 变化关系如图所示。
变化关系如图所示。

①曲线 对应物质为
对应物质为_______ (填化学式)。
② 达平衡时,
达平衡时, 的总转化率为
的总转化率为_______  。
。
③结合图像分析,达平衡时装置中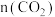 随温度升高的变化趋势为
随温度升高的变化趋势为_______ (填标号)。
A.减小 B.增大 C.先减小后增大 D.先增大后减小
④工业制备 通常控制温度在
通常控制温度在 ℃之间的原因是
℃之间的原因是_______ 。
(4)采用下图装置能实现 电化学法制
电化学法制 ,同时获得副产物
,同时获得副产物 。
。

①铜电极的电极反应式为_______ 。
②每制得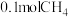 ,理论上
,理论上 电极生成
电极生成_______ 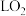 (折算为标准状况)。
(折算为标准状况)。
 加氢制
加氢制 ,为
,为 的减排与再利用提供了一种新策略,该过程中存在如下反应:
的减排与再利用提供了一种新策略,该过程中存在如下反应:反应Ⅰ:

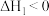
反应Ⅱ:


回答下列问题:
(1)已知:
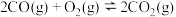

则反应


 、
、 、
、 的代数式表示)。
的代数式表示)。(2)关于反应Ⅰ,下列说法正确的有_______(填标号)。
| A.反应物的键能之和高于生成物的键能之和 |
| B.低温条件有利于该反应自发进行 |
| C.混合气体的平均摩尔质量不再改变,说明反应已达平衡 |
D.恒容条件下,充入更多的 能提高单位体积活化分子的百分数 能提高单位体积活化分子的百分数 |
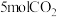 和
和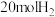 ,在不同温度下同时发生反应Ⅰ和Ⅱ,达平衡时,测得
,在不同温度下同时发生反应Ⅰ和Ⅱ,达平衡时,测得 和
和 的物质的量
的物质的量 随温度
随温度 变化关系如图所示。
变化关系如图所示。
①曲线
 对应物质为
对应物质为②
 达平衡时,
达平衡时, 的总转化率为
的总转化率为 。
。③结合图像分析,达平衡时装置中
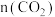 随温度升高的变化趋势为
随温度升高的变化趋势为A.减小 B.增大 C.先减小后增大 D.先增大后减小
④工业制备
 通常控制温度在
通常控制温度在 ℃之间的原因是
℃之间的原因是(4)采用下图装置能实现
 电化学法制
电化学法制 ,同时获得副产物
,同时获得副产物 。
。
①铜电极的电极反应式为
②每制得
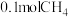 ,理论上
,理论上 电极生成
电极生成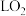 (折算为标准状况)。
(折算为标准状况)。
您最近一年使用:0次
解题方法
8 . 近期,我国科学家提出了一种双极膜硝酸盐还原工艺,原理如图。双极膜中间层中的 解离为
解离为 和
和 ,在外加直流电场作用下分别向两极迁移。下列说法不正确的是
,在外加直流电场作用下分别向两极迁移。下列说法不正确的是

 解离为
解离为 和
和 ,在外加直流电场作用下分别向两极迁移。下列说法不正确的是
,在外加直流电场作用下分别向两极迁移。下列说法不正确的是
A.m是 |
| B.b接电源正极 |
C.产生的 与 与 的物质的量之比为4:5 的物质的量之比为4:5 |
D.左室电极反应为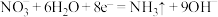 |
您最近一年使用:0次
解题方法
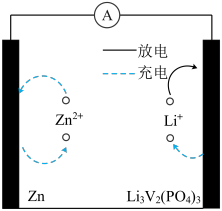
9 . 可充电水系Zn-LVP电池用锌和 作两极,电池工作示意图如图所示,下列有关该电池的说法正确的是
作两极,电池工作示意图如图所示,下列有关该电池的说法正确的是
 作两极,电池工作示意图如图所示,下列有关该电池的说法正确的是
作两极,电池工作示意图如图所示,下列有关该电池的说法正确的是
| A.放电时,当电路中转移1 mol电子时,正极材料增重7g |
B.放电时, 作正极,发生氧化反应 作正极,发生氧化反应 |
C.充电时,电子从 电极经电解液流向锌电极 电极经电解液流向锌电极 |
D.充电时,电池总反应为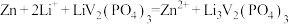 |
您最近一年使用:0次
名校
解题方法
10 . 一种微生物电解生产甲烷的装置如图所示。下列有关说法正确的是
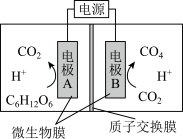

A.电极 应与电源的负极相连 应与电源的负极相连 |
B.电极 上的反应式为: 上的反应式为: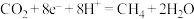 |
| C.提高温度一定能提高电解反应的速率 |
D.电解时 通过质子交换膜移向电极 通过质子交换膜移向电极 |
您最近一年使用:0次
2023-12-14更新
|
280次组卷
|
3卷引用:广东省江门市新会第一中学2023-2024学年高二上学期期末考试化学试题



