1 . 近年碳中和理念成为热门,通过“ →合成气→高附加值产品”的工艺路线,可有效实现
→合成气→高附加值产品”的工艺路线,可有效实现 的资源化利用。请回答下列问题:
的资源化利用。请回答下列问题:
(1) 加复制合成气(CO、
加复制合成气(CO、 )时发生下列反应:
)时发生下列反应:
已知:①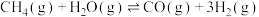

②

则

___________ 
(2) 经催化加氢可合成烯烃:
经催化加氢可合成烯烃: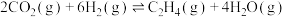
 。在0.1MPa时,按
。在0.1MPa时,按 投料,如下图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
投料,如下图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
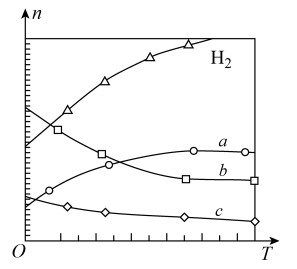
①在一个恒温恒容的密闭容器中,该可逆反应达到平衡的标志是___________ (填字母)
A.容器内各物质的浓度不随时间变化 B.
C.容器内压强不随时间变化 D.混合气体的密度不再改变
②该反应的
___________ 0(填“>”或“<”)。
③曲线b表示的物质为___________ (用化学式表示)。
(3)由 与
与 反应合成甲醇:
反应合成甲醇: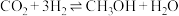
 。某温度下,将1mol
。某温度下,将1mol 和3mol
和3mol 充入体积不变的2L密闭容器中,初始总压为8MPa,发生上述反应,测得不同时刻反应后与反应前的压强关系如下表:
充入体积不变的2L密闭容器中,初始总压为8MPa,发生上述反应,测得不同时刻反应后与反应前的压强关系如下表:
该条件下的分压平衡常数为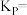
___________  (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
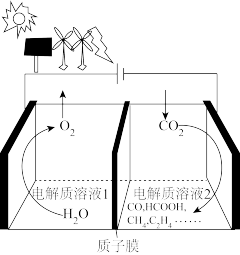
(4)电催化 制备燃料可实现资源综合利用。如图所示装置工作时,阳极的电极反应式为
制备燃料可实现资源综合利用。如图所示装置工作时,阳极的电极反应式为___________ 。
 →合成气→高附加值产品”的工艺路线,可有效实现
→合成气→高附加值产品”的工艺路线,可有效实现 的资源化利用。请回答下列问题:
的资源化利用。请回答下列问题:(1)
 加复制合成气(CO、
加复制合成气(CO、 )时发生下列反应:
)时发生下列反应:已知:①
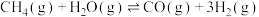

②


则



(2)
 经催化加氢可合成烯烃:
经催化加氢可合成烯烃: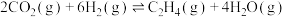
 。在0.1MPa时,按
。在0.1MPa时,按 投料,如下图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
投料,如下图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
①在一个恒温恒容的密闭容器中,该可逆反应达到平衡的标志是
A.容器内各物质的浓度不随时间变化 B.

C.容器内压强不随时间变化 D.混合气体的密度不再改变
②该反应的

③曲线b表示的物质为
(3)由
 与
与 反应合成甲醇:
反应合成甲醇: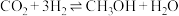
 。某温度下,将1mol
。某温度下,将1mol 和3mol
和3mol 充入体积不变的2L密闭容器中,初始总压为8MPa,发生上述反应,测得不同时刻反应后与反应前的压强关系如下表:
充入体积不变的2L密闭容器中,初始总压为8MPa,发生上述反应,测得不同时刻反应后与反应前的压强关系如下表:| 时间/h | 1 | 2 | 3 | 4 | 5 |
 | 0.92 | 0.85 | 0.79 | 0.75 | 0.75 |
该条件下的分压平衡常数为
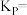
 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。(4)电催化
 制备燃料可实现资源综合利用。如图所示装置工作时,阳极的电极反应式为
制备燃料可实现资源综合利用。如图所示装置工作时,阳极的电极反应式为
您最近一年使用:0次
名校
解题方法
2 . 以Cl2、NaOH、CO(NH2)2(尿素)和SO2为原料可制备N2H4∙H2O(水合肼)和无水Na2SO3,其主要实验流程如下:

已知 ①Cl2+2OH-=ClO-+Cl-+H2O是放热反应。
②N2H4∙H2O沸点约118℃,具有强还原性,能与NaClO剧烈反应生成N2。
(1)如图表示用石墨作电极,在一定条件下电解饱和食盐水制取Cl2时,阳极上产生也会产生少量的ClO2的电极反应式:___________ ;电解一段时间,当阴极产生标准状况下气体112mL时,停止电解,则通过阳离子交换膜的阳离子物质的量为___________ mol。

(2)步骤Ⅰ制备NaClO溶液时,若温度超过40℃,Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式为___________ ;实验中控制温度除用冰水浴外,还需采取的措施是___________ 。
(3)步骤Ⅱ合成N2H4∙H2O的装置如图所示。NaClO碱性溶液与尿素水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应。实验中通过滴液漏斗滴加的溶液是___________ ;使用冷凝管的目的是___________ 。

(4)步骤Ⅳ用步骤Ⅲ得到的副产品Na2CO3制备无水Na2SO3,欲测定亚硫酸钠产品的纯度设计如下实验方案,并进行实验。某同学设计的下列滴定方式中,合理的是___________ (夹持部分略去)(填字母序号)


已知 ①Cl2+2OH-=ClO-+Cl-+H2O是放热反应。
②N2H4∙H2O沸点约118℃,具有强还原性,能与NaClO剧烈反应生成N2。
(1)如图表示用石墨作电极,在一定条件下电解饱和食盐水制取Cl2时,阳极上产生也会产生少量的ClO2的电极反应式:

(2)步骤Ⅰ制备NaClO溶液时,若温度超过40℃,Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式为
(3)步骤Ⅱ合成N2H4∙H2O的装置如图所示。NaClO碱性溶液与尿素水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应。实验中通过滴液漏斗滴加的溶液是

(4)步骤Ⅳ用步骤Ⅲ得到的副产品Na2CO3制备无水Na2SO3,欲测定亚硫酸钠产品的纯度设计如下实验方案,并进行实验。某同学设计的下列滴定方式中,合理的是

您最近一年使用:0次
解题方法
3 . 我国科学家以 与辛胺为原料实现了甲酸盐和辛腈的高选择性合成,该装置如图所示。下列表达正确的是
与辛胺为原料实现了甲酸盐和辛腈的高选择性合成,该装置如图所示。下列表达正确的是
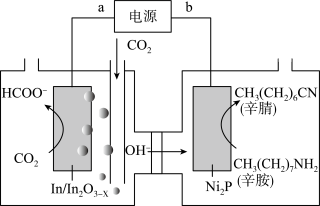
 与辛胺为原料实现了甲酸盐和辛腈的高选择性合成,该装置如图所示。下列表达正确的是
与辛胺为原料实现了甲酸盐和辛腈的高选择性合成,该装置如图所示。下列表达正确的是
| A.电源a为正极、b为负极 |
B.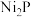 电极上辛胺失去电子 电极上辛胺失去电子 |
C.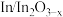 电极上发生了氧化反应 电极上发生了氧化反应 |
D.电极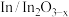 上的反应为 上的反应为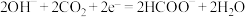 |
您最近一年使用:0次
4 . 2019年12月4日“全球碳计划”发布报告说,全球 排放量增速趋缓。人们还需要更有力的政策来逐步淘汰化石燃料的使用。
排放量增速趋缓。人们还需要更有力的政策来逐步淘汰化石燃料的使用。 的综合利用是解决温室问题的有效途径。
的综合利用是解决温室问题的有效途径。
(1)以 与
与 为原料可以合成尿素[CO(NH2)2],涉及的化学反应如下:
为原料可以合成尿素[CO(NH2)2],涉及的化学反应如下:
反应Ⅰ: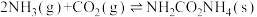
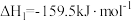 ;
;
反应Ⅱ: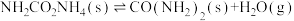
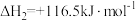 ;
;
反应Ⅲ:
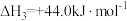 。
。
则反应Ⅳ: 与
与 合成尿素同时生成液态水的热化学方程式为
合成尿素同时生成液态水的热化学方程式为___________ 。
(2)利用工业废气中的 可以制取甲醇和水蒸气,其反应原理:
可以制取甲醇和水蒸气,其反应原理:
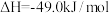 。在体积为1L的恒容密闭容器中,充入
。在体积为1L的恒容密闭容器中,充入 和
和 ,一定条件下发生反应测得
,一定条件下发生反应测得 和
和 的浓度随时间变化如图所示,反应10min达到平衡。
的浓度随时间变化如图所示,反应10min达到平衡。
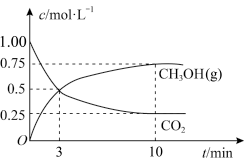
①从反应开始到平衡,氢气的平均反应速率
___________ 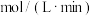 ;该反应的平衡常数为
;该反应的平衡常数为___________ (保留两位有效数字)。
②反应进行到3min时,v(正)___________ v(逆)(填“>”“<”或“=”)。
③下列措施可提高 转化率的是
转化率的是___________ 。
A.升高温度 B.将 从体系中分离出去
从体系中分离出去
C.恒容条件下充入He D.再充入适量的
(3)中国科学家首次用 高效合成乙酸,其反应路径如图所示:
高效合成乙酸,其反应路径如图所示:
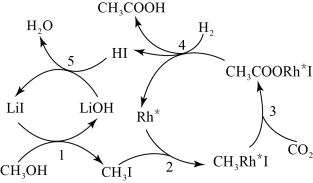
①原料中的 可通过电解法由
可通过电解法由 制取,用稀硫酸作电解质溶液,写出生成
制取,用稀硫酸作电解质溶液,写出生成 的电极反应式:
的电极反应式:___________ 。
②根据图示,写出总反应的化学方程式:___________ 。
 排放量增速趋缓。人们还需要更有力的政策来逐步淘汰化石燃料的使用。
排放量增速趋缓。人们还需要更有力的政策来逐步淘汰化石燃料的使用。 的综合利用是解决温室问题的有效途径。
的综合利用是解决温室问题的有效途径。(1)以
 与
与 为原料可以合成尿素[CO(NH2)2],涉及的化学反应如下:
为原料可以合成尿素[CO(NH2)2],涉及的化学反应如下:反应Ⅰ:
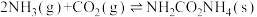
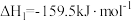 ;
;反应Ⅱ:
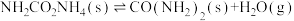
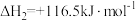 ;
;反应Ⅲ:

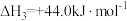 。
。则反应Ⅳ:
 与
与 合成尿素同时生成液态水的热化学方程式为
合成尿素同时生成液态水的热化学方程式为(2)利用工业废气中的
 可以制取甲醇和水蒸气,其反应原理:
可以制取甲醇和水蒸气,其反应原理:
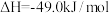 。在体积为1L的恒容密闭容器中,充入
。在体积为1L的恒容密闭容器中,充入 和
和 ,一定条件下发生反应测得
,一定条件下发生反应测得 和
和 的浓度随时间变化如图所示,反应10min达到平衡。
的浓度随时间变化如图所示,反应10min达到平衡。
①从反应开始到平衡,氢气的平均反应速率

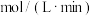 ;该反应的平衡常数为
;该反应的平衡常数为②反应进行到3min时,v(正)
③下列措施可提高
 转化率的是
转化率的是A.升高温度 B.将
 从体系中分离出去
从体系中分离出去C.恒容条件下充入He D.再充入适量的

(3)中国科学家首次用
 高效合成乙酸,其反应路径如图所示:
高效合成乙酸,其反应路径如图所示: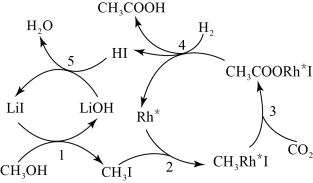
①原料中的
 可通过电解法由
可通过电解法由 制取,用稀硫酸作电解质溶液,写出生成
制取,用稀硫酸作电解质溶液,写出生成 的电极反应式:
的电极反应式:②根据图示,写出总反应的化学方程式:
您最近一年使用:0次



