名校
解题方法
1 . 对下列家务劳动所涉及原理的解释不正确的是
| 选项 | 家务劳动 | 化学知识 |
| A | 餐后将铁锅洗净后擦干 | Fe在潮湿的空气中易生锈 |
| B | 使用白醋除去水壶中的水垢 | 白醋可与CaCO3、Mg(OH)2反应 |
| C | 使用“84”消毒液(主要成分为NaClO、NaCl)进行环境消毒 | NaCl具有强氧化性 |
| D | 用温热的纯碱溶液清洗油污 | 油脂在碱性条件下可发生水解反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-29更新
|
295次组卷
|
3卷引用:2023年江苏省扬州市普通高中学业水平合格性模拟试卷(二)化学试题
解题方法
2 . 下列劳动与所涉及的化学知识不相符的是
| 选项 | 家务劳动 | 化学知识 |
| A | 使用含NaClO的84消毒液拖地 | NaClO具有还原性和漂白性 |
| B | 使用白醋除去水壶中的水垢 | 白醋可溶解碳酸钙等沉淀 |
| C | 餐后将洗净的铁锅擦干 | 铁在潮湿环境中易生锈 |
| D | 用温热的纯碱溶液擦拭有油污的灶台 | 油脂在碱性条件下发生水解反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 下列实验装置或操作能够达到实验目的的是
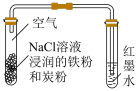 | 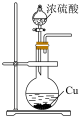 | 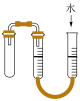 | 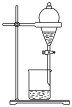 |
| A.验证铁粉发生析氢腐蚀 | B.验证浓硫酸的强氧化性 | C.检查装置气密性 | D.乙醇萃取碘水中的碘 |
A. | B. | C. | D. |
您最近一年使用:0次
解题方法
4 . 钢铁的电化学腐蚀
(1)实验探究——钢铁的电化学腐蚀原理
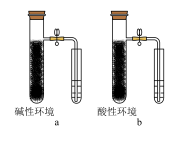
①向铁粉中加入碳粉的目的是___________ ;
②实验现象:a装置右边的小试管中液面________ ;b装置中右边小试管中液面_________ 。
(2)钢铁的电化学腐蚀
根据钢铁表面水溶液薄膜的酸碱性不同,钢铁的电化学腐蚀分为析氢腐蚀和吸氧腐蚀,如下图所示:
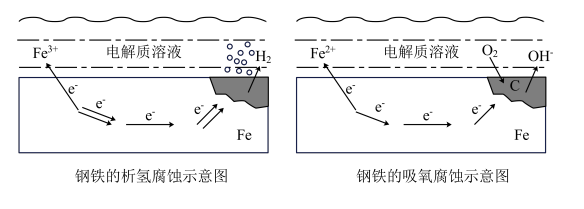
①钢铁的吸氧腐蚀:
通常情况下,在潮湿的空气中,钢铁表面凝结了一层溶有氧气的水膜,将会发生___________ 腐蚀。
负极反应式:_________ ;正极反应式:________ 。
总反应式:___________ 。
Fe(OH)2被进一步氧化成Fe(OH)3:___________ ,Fe(OH)3部分脱水生成Fe2O3·nH2O,是铁锈的主要成分。
②钢铁的析氢腐蚀:
当钢铁表面的电解质溶液_______ 较强时,腐蚀过程中有________ 放出。其中,Fe是_________ 极,C是__________ 极。
负极反应式:___________ ;正极反应式:__________ 。
总反应式:___________ 。
随着了氢气的析出,溶液的pH上升,最终形成铁锈。
(1)实验探究——钢铁的电化学腐蚀原理

①向铁粉中加入碳粉的目的是
②实验现象:a装置右边的小试管中液面
(2)钢铁的电化学腐蚀
根据钢铁表面水溶液薄膜的酸碱性不同,钢铁的电化学腐蚀分为析氢腐蚀和吸氧腐蚀,如下图所示:

①钢铁的吸氧腐蚀:
通常情况下,在潮湿的空气中,钢铁表面凝结了一层溶有氧气的水膜,将会发生
负极反应式:
总反应式:
Fe(OH)2被进一步氧化成Fe(OH)3:
②钢铁的析氢腐蚀:
当钢铁表面的电解质溶液
负极反应式:
总反应式:
随着了氢气的析出,溶液的pH上升,最终形成铁锈。
您最近一年使用:0次
名校
5 . 下列有关化学与生产、生活、科技的叙述错误的是
| A.Ge的单晶可以用于太阳能电池 |
| B.镀锌铁镀层破损后,更容易被腐蚀的金属是铁 |
| C.冷敷袋俗称冰袋,袋内物质是硝酸铵和水 |
| D.用“84”消毒液消毒时,主要是利用了次氯酸钠的强氧化性 |
您最近一年使用:0次
名校
6 . 埋在地下的铸铁输油管道,在下列各种情况下,被腐蚀速率最慢的是
| A.在含铁元素较多的酸性土壤中 |
| B.在潮湿疏松的碱性土壤中 |
| C.在干燥致密不透气的土壤中 |
| D.在含碳粒较多,潮湿透气的中性土壤中 |
您最近一年使用:0次
2023-08-26更新
|
167次组卷
|
3卷引用:第4节 金属的腐蚀与防护
名校
解题方法
7 . 劳动有利于“知行合一”。下列劳动项目与所述的化学知识没有关联的是
| 选项 | 劳动项目 | 化学知识 |
| A | 帮厨活动:热的纯碱液洗涤油污 | 升温碳酸钠溶液水解程度增大,溶液碱性增强 |
| B | 学农活动:氯化铵不能和草木灰混合施肥 | 氯化铵分解产生的HCl易与草木灰中 反应 反应 |
| C | 家务劳动:擦干已洗净的铁锅,以防生锈 | 潮湿会加快铁腐蚀速率 |
| D | 社区服务:使用醋酸清洗锅炉水垢 | 醋酸酸性强于碳酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 由下列实验操作和现象可得出结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向Co2O3中滴入浓盐酸 | 产生黄绿色气体 | 氧化性:Cl2>Co2O3 |
| B | 白铁皮(镀锌铁)出现刮痕后浸泡在饱和食盐水中,一段时间后入几滴K3[Fe(CN)6]溶液 | 无明显现象 | 该过程未发生氧化还原反应 |
| C | 用坩埚钳夹住一小块用砂纸打磨过的铝箔,在酒精灯上加热 | 铝箔熔化并滴落 | 金属铝的熔点较低 |
| D | 将10mL2mol·L-1的KI溶液与1mL1mol·L-1FeCl3溶液混合充分反应后滴加KSCN溶液 | 溶液颜色变红 | KI与FeCl3反应有可逆性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-10-28更新
|
362次组卷
|
2卷引用:河南省南阳市第一中学校2021届高三第三次月考化学试题
解题方法
9 . 埋在下列土壤中的铸铁输油管道,腐蚀速率最慢的是( )
| A.氧化铁较多的酸性土壤 | B.潮湿疏松的中性土壤 |
| C.碳颗粒较多的碱性土壤 | D.干燥致密的中性土壤 |
您最近一年使用:0次



