解题方法
1 . 设NA是阿伏加德罗常数的值。下列说法正确的是
| A.10 g质量分数为46%的乙醇溶液中氧原子数为0.6NA |
| B.0. 5 mol BF3中的共用电子对数为1. 5NA |
| C.标准状况下,22.4 L CH4与44.8 L Cl2在光照条件下充分反应后的分子总数为2NA |
| D.铅蓄电池放电时,若负极增重48g,则此时转移电子数为0.5NA |
您最近一年使用:0次
2023-04-03更新
|
419次组卷
|
2卷引用:陕西省西安市新城区2023届高三二模考试理综化学试题
名校
2 . “84消毒液”和医用酒精混合使用可能发生反应:
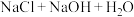 (未配平)。设
(未配平)。设 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是

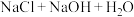 (未配平)。设
(未配平)。设 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是A. 溶液中含有 溶液中含有 个 个 |
B.标准状况下,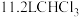 中含有 中含有 个C原子 个C原子 |
C.该反应中每消耗 ,转移 ,转移 个电子 个电子 |
D.100g质量分数为46%的乙醇溶液中含有 个 个 键 键 |
您最近一年使用:0次
3 . 设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.0.1molCH4与足量Cl2光照下反应生成CCl4的分子数为0.1NA |
| B.100g质量分数为17%的H2O2溶液中极性键数目为NA |
| C.25℃时,pH=1的硫酸溶液中含有的H+数目为0.1NA |
| D.1molNa与O2完全反应,转移的电子数一定为NA |
您最近一年使用:0次
解题方法
4 . 综合利用CH4和CO2对构建低碳社会、促进工业可持续发展有重要意义。
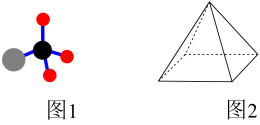
(1)CH4与Cl2光照下反应有多种产物。其中有机产物(图1)的电子式是_______ 。有人认为CH4是四棱锥型,碳原子位于四棱锥的顶点(图2),判断CH4不是四棱锥型分子的依据是_______ 。(选填编号)
a.CH4是非极性分子
b.一氯甲烷只有一种结构
c.二氯甲烷只有一种沸点
d.CH4中碳的质量分数75%
实验室对(CH4-CO2)催化重整,反应原理为:CH4(g)+CO2(g) 2CO(g)+2H2(g)。在1L固定容积的密闭容器中,充入0.1mol CO2、0.1mol CH4,分别在p1、p2、p3三种压强和不同温度下进行(CH4-CO2)催化重整,测得平衡时甲烷的转化率、温度和压强的关系如图。
2CO(g)+2H2(g)。在1L固定容积的密闭容器中,充入0.1mol CO2、0.1mol CH4,分别在p1、p2、p3三种压强和不同温度下进行(CH4-CO2)催化重整,测得平衡时甲烷的转化率、温度和压强的关系如图。
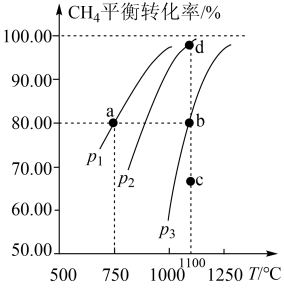
(2)750℃、p1时,反应经20min达到平衡。则平衡后CO的物质的量为_______ 。图中c点时,v正_______ v逆(选填:<、>、=)。
(3)该反应正反应为_______ 热反应(选填:吸、放);在p1、p2、p3中,压强最大的是_______ 。
(4)已知a点时的平衡常数Ka=1.64,则d点时的平衡常数Kd_______ 1.64(选填:<、>、=),理由是_______ 。
(1)CH4与Cl2光照下反应有多种产物。其中有机产物(图1)的电子式是

a.CH4是非极性分子
b.一氯甲烷只有一种结构
c.二氯甲烷只有一种沸点
d.CH4中碳的质量分数75%
实验室对(CH4-CO2)催化重整,反应原理为:CH4(g)+CO2(g)
 2CO(g)+2H2(g)。在1L固定容积的密闭容器中,充入0.1mol CO2、0.1mol CH4,分别在p1、p2、p3三种压强和不同温度下进行(CH4-CO2)催化重整,测得平衡时甲烷的转化率、温度和压强的关系如图。
2CO(g)+2H2(g)。在1L固定容积的密闭容器中,充入0.1mol CO2、0.1mol CH4,分别在p1、p2、p3三种压强和不同温度下进行(CH4-CO2)催化重整,测得平衡时甲烷的转化率、温度和压强的关系如图。
(2)750℃、p1时,反应经20min达到平衡。则平衡后CO的物质的量为
(3)该反应正反应为
(4)已知a点时的平衡常数Ka=1.64,则d点时的平衡常数Kd
您最近一年使用:0次
名校
5 . 设 NA为阿伏加德罗常数的值。下列叙述正确的是
| A.0.1 mol CH4与足量Cl2光照下反应生成CCl4的分子数为 0.1NA |
| B.l mol Na与O2完全反应,转移的电子数一定为NA |
| C.25℃时,pH=1的硫酸溶液中含有的 H+数目为0.1NA |
| D.100 g质量分数为 17%的H2O2溶液中极性键数目为NA |
您最近一年使用:0次
6 . 前四周期元素X、Y、Z、W的原子序数依次增大,X原子中有6个运动状态不同的电子,Y是地壳中含量最多的元素,基态Z原子K、L层上的电子总数是3p原子轨道上电子数的两倍,基态W原子中有6个未成对电子。下列说法不正确 的是
A.电负性: ,原子半径: ,原子半径: |
| B.同周期中,元素Z的第一电离能最大 |
| C.在一定条件下,X与氢元素形成的某些化合物与Z的单质及氢化物均能反应 |
D.在一定条件下,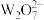 和 和 可以相互转化,且二者均具有强氧化性 可以相互转化,且二者均具有强氧化性 |
您最近一年使用:0次
2021高三·全国·专题练习
7 . 设NA为阿伏加德罗常数的值,下列说法不正确 的是
| A.1mol-CH3中含有的质子数为10NA |
| B.H2O2+Cl2=2HCl+O2反应中,每生成32gO2,转移2NA个电子 |
| C.3.6gCO和N2的混合气体含中子数为1.8NA |
| D.常温常压下,100g质量分数为46%的乙醇水溶液中含有的氧原子数为4NA |
您最近一年使用:0次
8 . 下列关于甲烷的说法正确的是
| A.甲烷是含碳元素质量分数最高的有机物 |
B.1 甲烷与1 甲烷与1  反应恰好生成1 反应恰好生成1 一氯甲烷 一氯甲烷 |
C. 有 有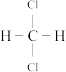 和 和 两种同分异构体 两种同分异构体 |
| D.有机物中的碳原子之间能以共价键结合,形成多种链状和环状 |
您最近一年使用:0次
名校
9 . A、B、C、D、E、F、G均为短周期元素,原子序数依次递增。A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E的化合物焰色反应是黄色,F与G位置相邻,G是同周期元素中原子半径最小的元素。
请用化学用语回答:
(1)D的简单阴离子的结构示意图是__________________ 。
(2)用电子式表示E2F的形成过程___________ 。
(3)E、F、G三种元素所形成的简单离子,半径由大到小的顺序是________ 。
(4)下列实验操作对应的实验现象中,不正确的是________ (填字母)。
(5)写出A与B形成的10电子分子的化学式___________ ,该物质与G的单质在光照下反应,一段时间后,下列装置示意图中能正确反映实验现象的是_________ (填字母)。
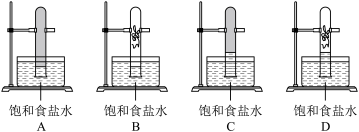
请用化学用语回答:
(1)D的简单阴离子的结构示意图是
(2)用电子式表示E2F的形成过程
(3)E、F、G三种元素所形成的简单离子,半径由大到小的顺序是
(4)下列实验操作对应的实验现象中,不正确的是
| 选项 | 实验操作 | 实验现象 |
| a | 将E单质投入到CuSO4溶液中 | 生成大量红色固体 |
| b | 向AlCl3溶液中通入过量C的气态氢化物 | 先生成白色沉淀,然后沉淀溶解 |
| c | 将G的单质通入到NaBr溶液中充分反应后,加入四氯化碳,振荡,静置 | 下层溶液变为橙色 |
| d | 将B的最高价氧化物通入到Na2SiO3溶液中 | 生成白色沉淀 |

您最近一年使用:0次
解题方法
10 . 下列说法不正确 的是( )
| A.制备铜氨纤维时,取出稀盐酸中的生成物,用水洗涤,得到蓝色的铜氨纤维 |
| B.天然气的主要成分是甲烷,不同地区天然气中甲烷含量不同 |
| C.长久存放的氯水逐渐转变为很稀的盐酸 |
| D.在燃烧木柴时,将木材架空,木材会燃烧的更旺 |
您最近一年使用:0次



