名校
解题方法
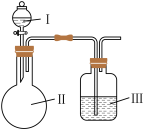
1 . 利用下列试剂和如图所示装置制备气体并除去其中的非水杂质,能达到目的的是(必要时可加热,加热及夹持装置已略去)
| 选项 | 气体 | 试剂I | 试剂II | 试剂Ⅲ |
|
| A | Cl2 | 浓盐酸 | MnO2 | NaOH溶液 | |
| B | CO2 | 稀盐酸 | CaCO3 | 饱和NaHCO3溶液 | |
| C | SO2 | 浓硝酸 | Na2SO3(s) | 饱和NaHSO3溶液 | |
| D | C2H4 | 浓硫酸 | C2H5OH(1) | KMnO4酸性溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-09-14更新
|
1309次组卷
|
9卷引用:山东省金科大联考2023-2024学年高三9月联考化学试题
山东省金科大联考2023-2024学年高三9月联考化学试题北京市海淀区2022-2023学年高三第二次模拟(下学期期末)考试化学试题安徽师范大学附属中学2023届高三下学期5月最后一卷理科综合化学试题北京师范大学附属实验中学2023-2024学年暑期高三第一次督导化学试题北京师范大学附属中学2023-2024学年高三上学期10月月考化学试题(已下线)考点3 物质的制备与性质实验 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)题型07 化学实验基础(选择题)-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)江西省宜春市丰城市第九中学2023-2024学年高一上学期1月期末化学试题(已下线)化学(北京卷02)-2024年高考押题预测卷
10-11高二下·安徽合肥·期末
2 . 下图是实验室用来验证乙烯与氢气反应产物的装置,请回答下列问题:
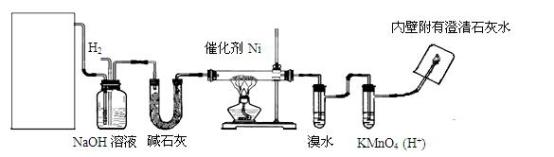
(1)方框内装置用来制取乙烯,其中包括的仪器是:①碎瓷片②石棉网和铁架台③圆底烧瓶④温度计(量程100℃)⑤温度计(量程200℃)⑥酒精灯⑦单孔塞⑧双孔塞⑨导管。不选用的仪器有_______ (填编号)。
(2)写出制乙烯化学方程式:_______ 。
(3)碱石灰的作用是:_______ 。
(4)实验过程中,发现溴水会褪色,可能的原因是:_______ 。
(5)出现什么现象可说明生成了乙烷?_______ 。

(1)方框内装置用来制取乙烯,其中包括的仪器是:①碎瓷片②石棉网和铁架台③圆底烧瓶④温度计(量程100℃)⑤温度计(量程200℃)⑥酒精灯⑦单孔塞⑧双孔塞⑨导管。不选用的仪器有
(2)写出制乙烯化学方程式:
(3)碱石灰的作用是:
(4)实验过程中,发现溴水会褪色,可能的原因是:
(5)出现什么现象可说明生成了乙烷?
您最近一年使用:0次
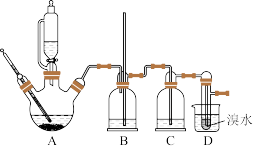
3 . 用少量的溴水和足量的乙醇制备1,2-二溴乙烷的装置如图所示(部分装置未画出):
有关数据列表如下:
请回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170 ℃左右,其最主要目的是_______(填字母代号)。
(2)装置B的作用是_______ 。
(3)在装置C中应加入_______(填字母代号),其目的是吸收反应中可能生成的SO2、CO2气体。
(4)若产物中有少量未反应的Br2,最好用_______(填字母代号)洗涤除去。
(5)若产物中有少量副产物乙醚,可用_______ 的方法除去。
(6)为了检验1,2-二溴乙烷中的溴元素,取出少量产品,下列几项实验步骤正确的操作顺序是_______(填代号)。
①加热;②加入AgNO3溶液;③加入稀HNO3酸化;④加入NaOH水溶液;⑤冷却

有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/(g·cm-3) | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 131 | 34.6 |
| 熔点/℃ | -114 | 10 | -116 |
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170 ℃左右,其最主要目的是_______(填字母代号)。
| A.引发反应 | B.加快反应速率 | C.防止乙醇挥发 | D.减少副产物乙醚生成 |
(3)在装置C中应加入_______(填字母代号),其目的是吸收反应中可能生成的SO2、CO2气体。
| A.水 | B.浓硫酸 | C.氢氧化钠溶液 | D.饱和碳酸氢钠溶液 |
| A.水 | B.氢氧化钠溶液 | C.碘化钠溶液 | D.乙醇 |
(6)为了检验1,2-二溴乙烷中的溴元素,取出少量产品,下列几项实验步骤正确的操作顺序是_______(填代号)。
①加热;②加入AgNO3溶液;③加入稀HNO3酸化;④加入NaOH水溶液;⑤冷却
| A.④①⑤③② | B.④③①⑤② | C.④③②①⑤ | D.④②①③⑤ |
您最近一年使用:0次
4 . 科学实验中要尽可能避免干扰因素对实验的影响。下列对下图的分析错误的是
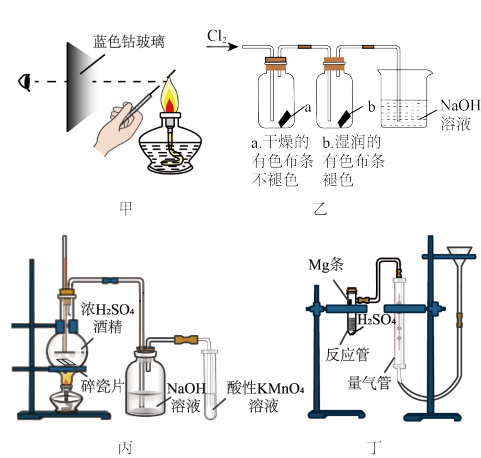

A.用甲操作检验 ,应通过蓝色钴玻璃观察火焰颜色,来排除 ,应通过蓝色钴玻璃观察火焰颜色,来排除 干扰 干扰 |
B.用乙装置验证氯水有漂白作用,设计 、 、 对照实验排除氯气的干扰 对照实验排除氯气的干扰 |
C.用丙装置制备并检验乙烯,氢氧化钠溶液是用来排除 对乙烯检验的干扰 对乙烯检验的干扰 |
D.丁装置中,读取 的体积时,应待装置冷却至室温,将漏斗缓缓下移至两端的液面处于相平,是为了防止温度和压强对气体体积的影响 的体积时,应待装置冷却至室温,将漏斗缓缓下移至两端的液面处于相平,是为了防止温度和压强对气体体积的影响 |
您最近一年使用:0次
2021-09-28更新
|
438次组卷
|
2卷引用:山东省威海乳山市银滩高级中学2022-2023学年高三上学期10月月考化学试题
5 . 下列有关图中所示实验的叙述正确的是
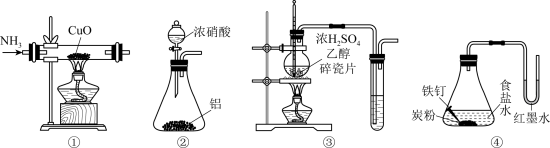
| A.装置①可验证NH3具有还原性 |
| B.装置②可用于制备NO2 |
| C.装置③试管中盛有酸性高锰酸钾溶液,可验证乙烯具有还原性 |
| D.装置④可验证铁的析氢腐蚀 |
您最近一年使用:0次
2022-03-07更新
|
142次组卷
|
3卷引用:单项选择题6-10
解题方法
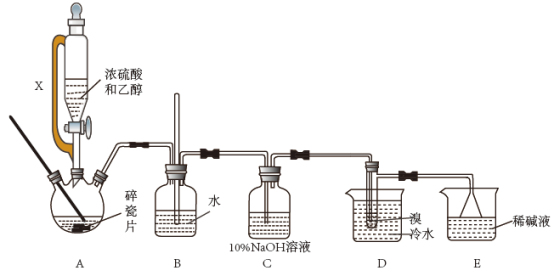
6 . 实验室用乙醇和浓硫酸反应制备乙烯,乙烯再与溴反应制备1,2—二溴乙烷。装置如图所示(加热及夹持装置省略):
已知:①乙醇在浓硫酸、140℃的条件下脱水生成乙醚。
②制备乙烯时部分乙醇可能与浓硫酸反应产生CO2、SO2。
有关数据列表如下:
回答下列问题:
(1)该装置中盛放浓硫酸和乙醇的仪器名称___ ;装置B的作用__ 。
(2)装置C中10%NaOH溶液的作用___ 。
(3)在A中发生的化学反应方程式为___ 。
(4)在制备乙烯时,要尽快地把反应温度提高到170℃左右,其最主要的目的是___ 。
a.引发反应 b.加快反应速率 c.防止乙醇挥发 d.减少副产物乙醚生成
(5)将1,2—二溴乙烷粗产品置于分液漏斗中,加水,振荡后静置,产物应在__ (填“上”或“下”)层。
(6)下列操作除掉1,2—二溴乙烷中的溴单质可行的是__ 。
a.加入碳酸钠溶液振荡、静置后分液
b.加入氢氧化钠溶液振荡、静置后分液
c.蒸馏
已知:①乙醇在浓硫酸、140℃的条件下脱水生成乙醚。
②制备乙烯时部分乙醇可能与浓硫酸反应产生CO2、SO2。

有关数据列表如下:
| 物质 | 乙醇 | 1,2—二溴乙烷 | 溴 |
| 密度g·cm-3 | 0.79 | 2.2 | 3.12 |
| 沸点/℃ | 78.5 | 132 | 59 |
(1)该装置中盛放浓硫酸和乙醇的仪器名称
(2)装置C中10%NaOH溶液的作用
(3)在A中发生的化学反应方程式为
(4)在制备乙烯时,要尽快地把反应温度提高到170℃左右,其最主要的目的是
a.引发反应 b.加快反应速率 c.防止乙醇挥发 d.减少副产物乙醚生成
(5)将1,2—二溴乙烷粗产品置于分液漏斗中,加水,振荡后静置,产物应在
(6)下列操作除掉1,2—二溴乙烷中的溴单质可行的是
a.加入碳酸钠溶液振荡、静置后分液
b.加入氢氧化钠溶液振荡、静置后分液
c.蒸馏
您最近一年使用:0次
2021-05-07更新
|
273次组卷
|
2卷引用:山东省日照五莲县2020-2021学年高二下学期期中考试化学试题
名校
解题方法
7 . 已知C2H5OH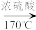 CH2=CH2↑+H2O,实验室制备的乙烯中常含有副产物CO2、SO2等。某实验小组利用如下装置制备少量1,2-二溴乙烷:
CH2=CH2↑+H2O,实验室制备的乙烯中常含有副产物CO2、SO2等。某实验小组利用如下装置制备少量1,2-二溴乙烷:

下列说法正确的是
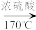 CH2=CH2↑+H2O,实验室制备的乙烯中常含有副产物CO2、SO2等。某实验小组利用如下装置制备少量1,2-二溴乙烷:
CH2=CH2↑+H2O,实验室制备的乙烯中常含有副产物CO2、SO2等。某实验小组利用如下装置制备少量1,2-二溴乙烷:
下列说法正确的是
| A.装置连接顺序为 acbdef |
| B.实验结束时,应首先熄灭酒精灯,再取出IV中的导管 |
| C.可用酸性高锰酸钾溶液代替品红溶液 |
| D.可采用分液操作分离产品 |
您最近一年使用:0次
2021-04-17更新
|
490次组卷
|
6卷引用:山东省菏泽市单县第一中学2021-2022学年高二下学期四月月考化学试题
解题方法
8 . 已知乙醇和浓硫酸混合加热到170℃可制得乙烯,同时乙烯中会混有少量的CO2和SO2杂质。某化学小组利用如图1装置来制备1,2—二溴乙烷,利用图2装置来进一步精制。1,2—二溴乙烷是无色液体,密度为2.18g•cm-3,沸点为131.4℃,熔点为9.79℃,微溶于水,易溶于乙醇、乙醚、丙酮等有机溶剂。实验前将无水乙醇和浓硫酸按体积比1:3混合好制得乙烯制备液。
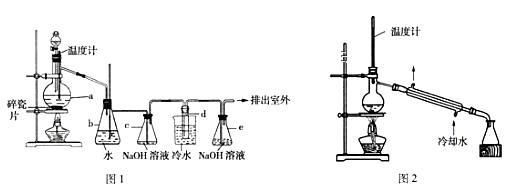
I.制备粗品
实验步骤:连接好装置,检查装置的气密性。分液漏斗中装乙烯制备液,d中装适量的液溴(表面覆盖少量水),其他药品按图1加入,打开分液漏斗旋塞滴入适量的液体后,关闭旋塞,点燃酒精灯加热使温度迅速升高到170℃直至反应完全,停止加热。回答下列问题:
(1)仪器a的名称为___ ,b装置的作用为___ 。
(2)若要配制60mL的乙烯制备液,请简述实验操作__ 。
(3)d装置中发生反应的化学方程式为__ 。
(4)如果缺少c装置会导致1,2—二溴乙烷的产率降低,原因是___ (用离子方程式表示),锥形瓶e中NaOH溶液的作用是____ 。
(5)判断d中液溴反应完全的标准是___ 。
II.制备精品
(6)d中制得的1,2—二溴乙烷中含有水,可先用____ 方法进行分离,再将1,2—二溴乙烷用如图2装置进行蒸馏,蒸馏时加入无水Na2SO4的目的是___ ,收集产品时,温度应控制在__ 左右。

I.制备粗品
实验步骤:连接好装置,检查装置的气密性。分液漏斗中装乙烯制备液,d中装适量的液溴(表面覆盖少量水),其他药品按图1加入,打开分液漏斗旋塞滴入适量的液体后,关闭旋塞,点燃酒精灯加热使温度迅速升高到170℃直至反应完全,停止加热。回答下列问题:
(1)仪器a的名称为
(2)若要配制60mL的乙烯制备液,请简述实验操作
(3)d装置中发生反应的化学方程式为
(4)如果缺少c装置会导致1,2—二溴乙烷的产率降低,原因是
(5)判断d中液溴反应完全的标准是
II.制备精品
(6)d中制得的1,2—二溴乙烷中含有水,可先用
您最近一年使用:0次
9 . 工业中很多重要的原料都是来源于石油化工,如图所示:
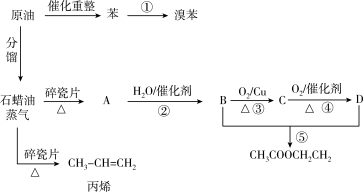
请回答下列问题:
(1) C的结构简式为_______ ,D中官能团的名称是______ 。
(2)②、⑤反应的反应类型分别是_____ 、______ 。
(3)反应①的化学方程式为_____ ;反应③的化学方程式为_____ 。
(4)丙烯分子中最多有____ 个原子共面,丙烯在一定条件下可以发生加聚反应,写出其反应的化学方程式:_____ 。
(5)某实验小组用以下装置制备乙酸乙酯。
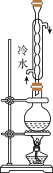
球形冷凝管的作用是_____ 。将圆底烧瓶中的液体倒入饱和碳酸钠溶液中,经过多步操作,可分离得到粗产品。此过程中定需要的操作是______ (填序号)。
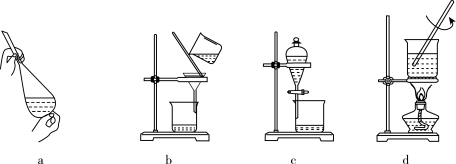

请回答下列问题:
(1) C的结构简式为
(2)②、⑤反应的反应类型分别是
(3)反应①的化学方程式为
(4)丙烯分子中最多有
(5)某实验小组用以下装置制备乙酸乙酯。

球形冷凝管的作用是

您最近一年使用:0次
解题方法
10 . 在实验室里制取的乙烯中常混有少量的二氧化硫,某化学兴趣小组设计了如图所示的实验装置确认该混合气体中是否含有SO2和C2H4。请回答下列问题:
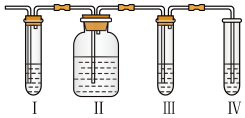
⑴上述Ⅰ、Ⅳ装置可盛放的试剂是:Ⅰ____ ;Ⅳ___ ;(请将下列有关试剂的序号填入对应装置内,可重复选用)。
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
⑵能说明SO2气体存在的现象是________
⑶使用装置Ⅱ的目的是_______ ;有关反应的离子方程式是_____ 。
⑷确定含有乙烯的现象是_______ 。
⑸为了制备重要的有机原料氯乙烷(CH3CH2Cl),下面是两位同学设计的方案。
甲同学:选乙烷和适量氯气在光照条件下制备;
乙同学:选乙烯和适量HCl在一定条件下制备。
你认为上述两位同学的方案中,合理的是______ 的方案。

⑴上述Ⅰ、Ⅳ装置可盛放的试剂是:Ⅰ
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
⑵能说明SO2气体存在的现象是
⑶使用装置Ⅱ的目的是
⑷确定含有乙烯的现象是
⑸为了制备重要的有机原料氯乙烷(CH3CH2Cl),下面是两位同学设计的方案。
甲同学:选乙烷和适量氯气在光照条件下制备;
乙同学:选乙烯和适量HCl在一定条件下制备。
你认为上述两位同学的方案中,合理的是
您最近一年使用:0次
2020-05-31更新
|
179次组卷
|
2卷引用:山东省临沂市沂水四中2019-2020学年下学期高一阶段性教学质量检测化学试题