2024高三·全国·专题练习
解题方法
1 . 下列实验方案、现象、结论的对应关系正确的是
| 选项 | 实验方案 | 现象 | 结论 |
| A | 向淀粉溶液中加入几滴稀硫酸,水浴加热,冷却后加入新制Cu(OH)2,加热 | 无砖红色沉淀生成 | 淀粉未水解 |
| B | 向卤代烃CH3CH2CH2X中加入NaOH溶液并加热,冷却后取上层液体,滴加过量稀硝酸,再加入几滴AgNO3溶液 | 有淡黄色沉淀生成 | 该卤代烃中含有溴元素 |
| C | 向2丁烯醛(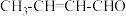 )中滴加酸性KMnO4溶液 )中滴加酸性KMnO4溶液 | 紫色褪去 | 该有机物中存在醛基 |
| D | 向鸡蛋清溶液中加入饱和(NH4)2SO4溶液,振荡 | 有固体析出 | (NH4)2SO4溶液能使蛋白质变性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
2 . 下列化学反应表示错误的是
A.用FeS固体除去污水中的Hg2+: |
B.AgCl沉淀溶于氨水: |
C.苯酚钠(C6H5ONa)溶液中通入少量CO2气体: 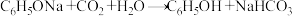 |
D.乙醛和新制Cu(OH)2共热出现砖红色浑浊:  |
您最近半年使用:0次
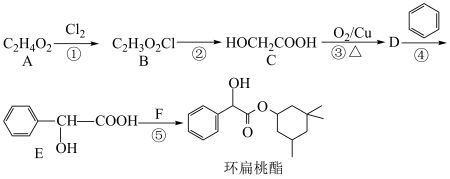
3 . 环扁桃酯临床上主要用于治疗脑动脉硬化。环扁桃酯的一种合成路线如下所示:
(1)写出A的官能团___________ ;①的反应类型___________ ;反应②所需试剂和条件___________ 。
(2)写出反应③的化学方程式___________ 。
(3)反应⑤中另一反应物F的结构简式为___________ 。
(4)写出E自身成环的反应方程式___________ 。
(5)检验D是否已经完全转化为E的操作是___________ 。
(6)满足下列条件,写出一种E的同分异构体的结构简式___________ 。
ⅰ.能发生水解反应 ⅱ.苯环上的一溴代物只有两种
(7)写出由乙苯(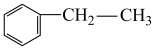 )合成聚苯乙烯()
)合成聚苯乙烯() 的合成路线
的合成路线_______ 。(合成路线常用的表示方式为:A ……B
……B 目标产物)
目标产物)
(1)写出A的官能团
(2)写出反应③的化学方程式
(3)反应⑤中另一反应物F的结构简式为
(4)写出E自身成环的反应方程式
(5)检验D是否已经完全转化为E的操作是
(6)满足下列条件,写出一种E的同分异构体的结构简式
ⅰ.能发生水解反应 ⅱ.苯环上的一溴代物只有两种
(7)写出由乙苯(
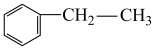 )合成聚苯乙烯()
)合成聚苯乙烯() 的合成路线
的合成路线 ……B
……B 目标产物)
目标产物)
您最近半年使用:0次
4 . 下列方程式与所给事实不相符 的是
A.Al溶于NaOH溶液产生无色气体:2Al+2OH-+2H2O=2AlO +3H2↑ +3H2↑ |
| B.用CuSO4溶液除去乙炔中的H2S产生黑色沉淀:Cu2++S2-=CuS↓ |
| C.Fe(OH)2在空气中放置最终变为红褐色:4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
D.乙醛与新制的Cu(OH)2在加热条件下产生砖红色沉淀:CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O CH3COONa+Cu2O↓+3H2O |
您最近半年使用:0次
5 . 下列说法不正确的是
| A.可用新制氢氧化铜悬浊液鉴别乙醇、乙醛和乙酸溶液 |
| B.可用溴的四氯化碳溶液除去乙烷中混有的乙烯 |
C.可用 射线衍射技术测定青蒿素的分子结构 射线衍射技术测定青蒿素的分子结构 |
| D.将有机溶剂与粉碎后的玫瑰花瓣混合,进行搅拌和浸泡,该提取方法为萃取 |
您最近半年使用:0次
名校
6 . 某有机物A的化学式为CxHyOz,15 g A完全燃烧可生成22 g CO2和9 g H2O。试求:
(1)该有机物的最简式:__________ 。
(2)若A的相对分子质量为60,且和Na2CO3混合时有气体放出,A和醇能发生酯化反应,则其结构简式为__________ 。
(3)若A的相对分子质量为60,且是易挥发有水果香味的液体,能发生水解反应,则其结构简式为__________ 。
(4)若1 mol A与足量的钠反应产生2.5 mol H2,同时A还可以与新制Cu(OH)2悬浊液反应生成砖红色沉淀,则其结构简式为__________ 。
(1)该有机物的最简式:
(2)若A的相对分子质量为60,且和Na2CO3混合时有气体放出,A和醇能发生酯化反应,则其结构简式为
(3)若A的相对分子质量为60,且是易挥发有水果香味的液体,能发生水解反应,则其结构简式为
(4)若1 mol A与足量的钠反应产生2.5 mol H2,同时A还可以与新制Cu(OH)2悬浊液反应生成砖红色沉淀,则其结构简式为
您最近半年使用:0次
7 . 某小组同学探究Cu(OH)2和醛的反应产物。
已知:Cu2O + 2H+ =Cu2+ + Cu + H2O;[CuCl2]−(无色)易被氧化为[CuCl4]2−(黄色)。
(1)将25%的NaOH溶液、8%的CuSO4溶液和37%~40%的甲醛溶液按一定比例依次混合后加热(始终保持NaOH过量)。实验记录如下:
①实验I中的紫红色固体过滤、洗涤后,加入稀硫酸,振荡,溶液无明显变化,证明Cu(OH)2被还原为___________ ;甲醛的氧化产物可能是HCOONa或Na2CO3,通过实验排除了Na2CO3的可能,简述实验操作和现象___________ 。
②X射线衍射等技术确认实验II中砖红色固体主要是Cu2O,写出实验II中生成Cu2O的化学方程式___________ 。
③实验I和II中产生的气体是H2.查阅资料发现:在碱性条件下,Cu2O可以被甲醛还原为Cu并伴有H2产生,写出反应的离子方程式___________ 。
(2)在试管里加入 10 %的NaOH溶液2 mL,然后加入2% 的CuSO4溶液 0.4 mL,振荡后,加入0.5 mL乙醛溶液,加热后得到橙红色浊液,过滤、洗涤之后检验生成的橙红色固体。实验记录如下:
①实验III的目的___________ 。
②用离子方程式解释实验IV溶液中发生的变化:___________ 。
③结合以上实验,小组同学认为橙红色固体只有Cu2O,你认为是否合理并说明原因___________ 。
已知:Cu2O + 2H+ =Cu2+ + Cu + H2O;[CuCl2]−(无色)易被氧化为[CuCl4]2−(黄色)。
(1)将25%的NaOH溶液、8%的CuSO4溶液和37%~40%的甲醛溶液按一定比例依次混合后加热(始终保持NaOH过量)。实验记录如下:
| 实验 | 试剂用量 | 实验现象 |
| I | n(HCHO):n(CuSO4) > 20 | 生成紫红色固体,有大量气体产生 |
| II | n(HCHO):n(CuSO4) = 1 | 生成砖红色固体,有少量气体产生 |
②X射线衍射等技术确认实验II中砖红色固体主要是Cu2O,写出实验II中生成Cu2O的化学方程式
③实验I和II中产生的气体是H2.查阅资料发现:在碱性条件下,Cu2O可以被甲醛还原为Cu并伴有H2产生,写出反应的离子方程式
(2)在试管里加入 10 %的NaOH溶液2 mL,然后加入2% 的CuSO4溶液 0.4 mL,振荡后,加入0.5 mL乙醛溶液,加热后得到橙红色浊液,过滤、洗涤之后检验生成的橙红色固体。实验记录如下:
| 实验 | 实验操作 | 实验现象 |
| III | 铜粉中加入7 mol/L盐酸,振荡 | 铜粉未溶解,溶液呈无色 |
| IV | 氧化亚铜中加入7 mol/L盐酸,振荡; 再加入过量铜粉 | 固体全部溶解,溶液变为黄色; 黄色溶液变为无色 |
| V | 橙红色固体中加入7 mol/L盐酸,振荡 | 固体全部溶解,溶液变为黄色 |
②用离子方程式解释实验IV溶液中发生的变化:
③结合以上实验,小组同学认为橙红色固体只有Cu2O,你认为是否合理并说明原因
您最近半年使用:0次
23-24高二下·全国·课前预习
解题方法
8 . 乙醛的化学性质
(1)加成反应
①催化加氢又称为___________ 反应,化学方程式为___________ 。
②与HCN加成
a.化学方程式为___________ 。
b.反应原理:
(2)氧化反应
①与银氨溶液的反应方程式为___________ 。
②与新制的Cu(OH)2反应方程式为___________ 。
③与O2的催化氧化反应方程式为___________ 。
(1)加成反应
①催化加氢又称为
②与HCN加成
a.化学方程式为
b.反应原理:

(2)氧化反应
①与银氨溶液的反应方程式为
②与新制的Cu(OH)2反应方程式为
③与O2的催化氧化反应方程式为
您最近半年使用:0次
解题方法
9 . 下列化学方程式或离子方程式或热化学方程式书写错误的是
A.钢铁发生吸氧腐蚀的总反应: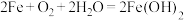 |
B.方铅矿(PbS)遇 溶液生成铜蓝(CuS): 溶液生成铜蓝(CuS): |
C.乙醛与新制的氢氧化铜悬浊液混合后加热: |
D.密闭容器中,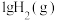 与足量的 与足量的 混合反应后生成HI(g),放出akJ热量(a>0): 混合反应后生成HI(g),放出akJ热量(a>0):  |
您最近半年使用:0次
10 . 下列说法正确的是
| A.工业酒精直接蒸馏可制得无水乙醇 |
| B.教材中苯甲酸重结晶实验操作步骤:热溶解→趁热过滤→冷却结晶再过滤 |
| C.溴乙烷与NaOH水溶液加热充分反应后,取上层清液,先加稀硝酸酸化再加入AgNO3溶液有淡黄色沉淀生成 |
| D.向硫酸铜溶液中滴加少量NaOH溶液,再加入葡萄糖溶液并加热,一定生成砖红色沉淀 |
您最近半年使用:0次



