解题方法
1 . “题图”是部分元素的离子结构示意图和元素周期表的一部分。 请回答:
(1)图①、②中属于阴离子的是______ (填序号),该元素的质子数为______ ;13号元素原子的最外层电子数为_________ 。
① ②
②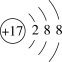
(2)由表中原子序数为1、8、13的元素组成物质的化学式为_____________ 。
(1)图①、②中属于阴离子的是
①
 ②
②
 | ||||||
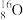 | ||||||
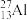 |  | |||||
您最近一年使用:0次
2 . 下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
(1)⑧的原子结构示意图为_________ ;
(2)②的气态氢化物分子的结构式为___________ ,②和⑦的气态氢化物的稳定性相比,其中较弱的是____ (用该氢化物的化学式表示);
(3)②、③的最高价含氧酸的酸性由强到弱的顺序是____ (填化学式);
(4)⑤、⑥元素的金属性强弱依次为___________ (填“增大”、“减小”或“不变”);
(5)④、⑤、⑥的形成的简单离子半径依次_________ (填“增大”、“减小”或“不变”);
(6)①、④、⑤元素可形成既含离子键又含共价键的化合物,写出它的电子式:_____ 。
族 周期 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)⑧的原子结构示意图为
(2)②的气态氢化物分子的结构式为
(3)②、③的最高价含氧酸的酸性由强到弱的顺序是
(4)⑤、⑥元素的金属性强弱依次为
(5)④、⑤、⑥的形成的简单离子半径依次
(6)①、④、⑤元素可形成既含离子键又含共价键的化合物,写出它的电子式:
您最近一年使用:0次
2020-05-18更新
|
517次组卷
|
2卷引用:江西省上饶市横峰中学2019-2020学年高一(自招班)下学期入学考试化学试题
名校
解题方法
3 . 下表是现行中学化学教科书中元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答问题;
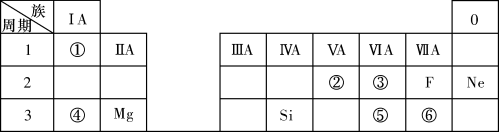
(1)④表示的元素是___ (填元素符号);
(2)②、③两种元素相比较,原子半径较大的是___ (填元素符号);
(3)写出①与⑥两种元素所形成化合物的化学式___ ;
(4)③和⑤两种元素的非金属性强弱顺序是③____ ⑤(填“<”或“>”)。

(1)④表示的元素是
(2)②、③两种元素相比较,原子半径较大的是
(3)写出①与⑥两种元素所形成化合物的化学式
(4)③和⑤两种元素的非金属性强弱顺序是③
您最近一年使用:0次
2020-05-13更新
|
648次组卷
|
3卷引用:湖南省2019-2020学年高二学业水平考试信息模拟(五) 化学
4 . 下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题。
(1)元素②的原子结构示意图为_____ 。
(2)元素③、④、⑤、⑥原子半径由大到小为_____ 。
(3)上述 8 种元素中,非金属性最强的是_____ 。
(4)元素②、③形成的气态氢化物稳定性:_____ >_____ ;元素①、③、⑤可形成既含离子键又含极性共价键的化合物,写出其电子式:_____ 。
(5)元素⑦的最高价氧化物对应的水化物与元素⑤最高价氧化物对应的水化物溶液反应的离子方程式为_____ 。
(6)写出金属铜与②最高价氧化物对应的水化物稀溶液反应的离子方程式_____ 。
(7)从原子结构的角度解释元素③和⑦的非金属性强弱:_____
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)元素③、④、⑤、⑥原子半径由大到小为
(3)上述 8 种元素中,非金属性最强的是
(4)元素②、③形成的气态氢化物稳定性:
(5)元素⑦的最高价氧化物对应的水化物与元素⑤最高价氧化物对应的水化物溶液反应的离子方程式为
(6)写出金属铜与②最高价氧化物对应的水化物稀溶液反应的离子方程式
(7)从原子结构的角度解释元素③和⑦的非金属性强弱:
您最近一年使用:0次
名校
解题方法
5 . 下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:__ (填元素符号),
(2)在最高价氧化物对应的水化物中,酸性最强的化合物的分子__ ,碱性最强的化合物的电子式是:__ 。
(3)用电子式表示元素④与⑥的化合物的形成过程:__ 。
(4)表示①与⑦的化合物的电子式__ ,该化合物是由__ (填“极性”或“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是_ (用化学式表示)。
(6)元素③的简单氢化物的结构式__ ,在常温下和元素⑦的单质反应的离子方程式__ 。
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 |
| 第二周期 | ① | ② | ③ | |||||
| 第三周期 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 第四周期 | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的是:
(2)在最高价氧化物对应的水化物中,酸性最强的化合物的分子
(3)用电子式表示元素④与⑥的化合物的形成过程:
(4)表示①与⑦的化合物的电子式
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是
(6)元素③的简单氢化物的结构式
您最近一年使用:0次
2020-04-22更新
|
297次组卷
|
2卷引用:湖南省双峰县第一中学2019-2020学年高一下学期入学考试化学试题
6 . (1)表中的实线是元素周期表部分边界,请在表中用实线补全元素周期表边界________ 。
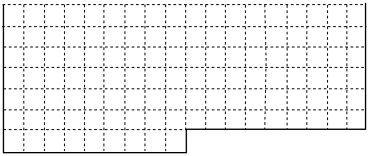
(2)元素甲是第三周期ⅥA族元素,请在方框中按氦元素的式样(如图)
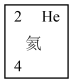
写出元素甲的原子序数、元素符号、元素名称、相对原子质量。
(3)元素乙的M层上有3个电子,则乙原子半径与甲原子半径比较:________ >________ (用元素符号表示),甲、乙的最高价氧化物水化物相互反应的离子方程式为:________
(4)元素周期表体现了元素周期律,即元素的性质随着_________ 的递增呈现____ 的变化。

(2)元素甲是第三周期ⅥA族元素,请在方框中按氦元素的式样(如图)

写出元素甲的原子序数、元素符号、元素名称、相对原子质量。
(3)元素乙的M层上有3个电子,则乙原子半径与甲原子半径比较:
(4)元素周期表体现了元素周期律,即元素的性质随着
您最近一年使用:0次
7 . 表为元素周期表的一部分,表中a~f代表六种短周期主族元素。完成下列填空:
(1)六种元素中,原子半径最大的是_________ (填元素编号) 。d、e、f三种元素的原子结构上的相同点是________________________________ 。
(2)若a的气态氢化物的水溶液呈碱性,则a的气态氢化物的电子式是___________ ;六种元素中,最高价氧化物对应水化物的酸性最强的是_________ (填元素符号)。
(3)若f元素的原子L层电子数比M层电子数多1个,则e元素的非金属性比f元素的非金属性_________ (选填“强”、“弱’’),能说明这一事实的化学方程式是____________________ (任写一个)。
(4)若b为非金属元素,则以下推断正确的是_________ (选填编号)。
①a一定是金属元素 ②d一定是金属元素 ③f一定是非金属元素
| a | b | c |
| d | e | f |
(1)六种元素中,原子半径最大的是
(2)若a的气态氢化物的水溶液呈碱性,则a的气态氢化物的电子式是
(3)若f元素的原子L层电子数比M层电子数多1个,则e元素的非金属性比f元素的非金属性
(4)若b为非金属元素,则以下推断正确的是
①a一定是金属元素 ②d一定是金属元素 ③f一定是非金属元素
您最近一年使用:0次
2013高二·湖南·学业考试
名校
8 . 下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素,请根据要求回答问题。
(1)①元素符号是_______ ;
(2)②的原子序数是______ ;
(3)①和⑤两种元素的非金属性强弱关系:①___ ⑤(填“>”或“<”);
(4)下列化学用语正确的是______ (填字母代号):
A. ④和⑥形成化合物的化学式:NaCl
| 族 周期 | IA | 0 | |||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | ① | ② | Ne | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | |||||
(2)②的原子序数是
(3)①和⑤两种元素的非金属性强弱关系:①
(4)下列化学用语正确的是
A. ④和⑥形成化合物的化学式:NaCl
B. ⑤的原子结构示意图:
C.③和⑥形成化合物的电子式:
您最近一年使用:0次
解题方法
9 . 下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。请根据要求回答问题:

(1)④的原子序数是________ ;
(2)⑤的原子结构示意图是____________ ;
(3)②和③两种元素的非金属性强弱关系是:②______ ③(填“>”、“<”或“=”);
(4)①和⑥两种元素组成的化合物中含有的化学键是_____ (填“共价”或“离子”)键。

(1)④的原子序数是
(2)⑤的原子结构示意图是
(3)②和③两种元素的非金属性强弱关系是:②
(4)①和⑥两种元素组成的化合物中含有的化学键是
您最近一年使用:0次
2020-03-09更新
|
413次组卷
|
2卷引用:2016年湖南省普通高中学业水平考试化学试题
名校
解题方法
10 . 2019年是元素周期表诞生150周年,元素周期表在学习、研究和生产实践中有很重要的作用。①~⑥六种元素在元素周期表中的位置如下:
请回答下列问题:
(1)⑥的元素符号为___________ 。
(2)由①③④形成的化合物是一种强碱,其化学式____________ 。
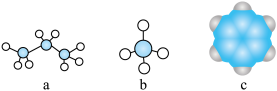
(3)由①②形成的最简单化合物的分子模型为_____________ (填序号)
(4)⑤和⑥两种元素的最高价氧化物对应的水化物之间反应的离子方程式为________________________________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | ① | ||||||
| 2 | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ |
请回答下列问题:
(1)⑥的元素符号为
(2)由①③④形成的化合物是一种强碱,其化学式
(3)由①②形成的最简单化合物的分子模型为

(4)⑤和⑥两种元素的最高价氧化物对应的水化物之间反应的离子方程式为
您最近一年使用:0次
2020-03-09更新
|
373次组卷
|
2卷引用:2019年12月河北省高中学业水平合格性考试(2018级)化学试题



