1 . 用周期表中特殊位置的短周期元素符号填空
(1)族序数等于周期数3倍的元素:_______ ;
(2)周期数是族序数3倍的元素是:_______ ;
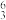 Li、
Li、 Li、
Li、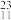 Na、
Na、 Mg、
Mg、 C、
C、 N中,
N中,
(3)_______ 和_______ 互为同位素;
(4)_______ 和_______ 的质量数相等,但不能互称同位素;
(1)族序数等于周期数3倍的元素:
(2)周期数是族序数3倍的元素是:
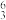 Li、
Li、 Li、
Li、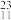 Na、
Na、 Mg、
Mg、 C、
C、 N中,
N中,(3)
(4)
您最近一年使用:0次
2 . 下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
请根据要求用元素符号或化学式回答下列问题:
(1)画出d元素原子的结构示意图___________ ,其气态氢化物溶于水显___________ 性。(填“酸”或“碱”)
(2)比较元素g和元素h形成的最高价氧化物的水化物的碱性强弱___________>___________。___________
(3)表中j元素在元素周期表中的位置是___________ 。
(4)表中所列元素中,最高价氧化物对应水化物碱性最强的是___________ (填写化合物的化学式,下同),具有两性的是___________ 。
| a | b | ||||||||||||||||
| c | d | e | f | ||||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | o |
请根据要求用元素符号或化学式回答下列问题:
(1)画出d元素原子的结构示意图
(2)比较元素g和元素h形成的最高价氧化物的水化物的碱性强弱___________>___________。
(3)表中j元素在元素周期表中的位置是
(4)表中所列元素中,最高价氧化物对应水化物碱性最强的是
您最近一年使用:0次
名校
3 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图元素周期表的回答下列问题。

(1)元素 Ga 在元素周期表中的位置为________ 。
(2) Sn 的最高正价为________ ;As 的气态氢化物为_____ ;CCl4的电子式________
(3)根据元素周期律推断:
①阴影部分元素氢化物热稳定性最高的是______ (填化学式)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4___ H2SeO4(填“>”、“<”或“=”)。
③简单氢化物的熔沸点:H2O__ H2S(填“>”“<”或“=”)。
(4)硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是____ 。
a.原子半径:In>Se
b.In 的金属性比 Se 强
c.In 的金属性比 Al 弱
d.硒化铟的化学式为 InSe2

(1)元素 Ga 在元素周期表中的位置为
(2) Sn 的最高正价为
(3)根据元素周期律推断:
①阴影部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③简单氢化物的熔沸点:H2O
(4)硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是
a.原子半径:In>Se
b.In 的金属性比 Se 强
c.In 的金属性比 Al 弱
d.硒化铟的化学式为 InSe2
您最近一年使用:0次
名校
解题方法
4 . 表是元素周期表的一部分。
请回答:
(1)世界上第一张元素周期表的作者是_______ (填序号);
a.阿伏加德罗 b.门捷列夫 c.居里夫人
(2)从表中查出第2周期第ⅠA族的元素是_______ ;
(3)上表列出的元素中,非金属性最强的是_______ ;
(4)某同学探究元素性质递变规律与原子结构的关系,进行了如下实验:
【实验操作】取已除去氧化膜且面积相等的镁条和铝条,分别投入2ml 1mol/L的盐酸中;
【实验现象】镁比铝与酸反应更剧烈;
【实验结论】①金属性:Mg_______ Al(选填“>”或“<”)
【查阅资料】原子半径(nm)Mg-0.160 Al-0.143;
【思考】②利用元素周期律对上述实验结论进行解释_______ 。
周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | H | He | ||||||
| 2 | Li | Be | B | C | N | O | F | Ne |
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar |
请回答:
(1)世界上第一张元素周期表的作者是
a.阿伏加德罗 b.门捷列夫 c.居里夫人
(2)从表中查出第2周期第ⅠA族的元素是
(3)上表列出的元素中,非金属性最强的是
(4)某同学探究元素性质递变规律与原子结构的关系,进行了如下实验:
【实验操作】取已除去氧化膜且面积相等的镁条和铝条,分别投入2ml 1mol/L的盐酸中;
【实验现象】镁比铝与酸反应更剧烈;
【实验结论】①金属性:Mg
【查阅资料】原子半径(nm)Mg-0.160 Al-0.143;
【思考】②利用元素周期律对上述实验结论进行解释
您最近一年使用:0次
解题方法
5 . 按顺序写出11-18号元素的名称和符号:_______
您最近一年使用:0次
20-21高二·全国·课时练习
解题方法
6 . 指出下列元素在周期表中的位置:
(1)基态原子的电子排布式为[Ar]4s1的元素:第___ 周期、__ 族。
(2)基态原子的电子排布式为[Ar]3d34s2的元素:第__ 周期、__ 族。
(3)基态原子的电子排布式为[Ar]3d104s1的元素:第__ 周期、__ 族。
(4)基态原子的电子排布式为[Ne]3s23p5的元素:第__ 周期、__ 族。
(1)基态原子的电子排布式为[Ar]4s1的元素:第
(2)基态原子的电子排布式为[Ar]3d34s2的元素:第
(3)基态原子的电子排布式为[Ar]3d104s1的元素:第
(4)基态原子的电子排布式为[Ne]3s23p5的元素:第
您最近一年使用:0次
7 . 根据元素周期表1~18号元素的性质和递变规律,回答下列问题。
(1)非金属性最强的元素为___________ (填元素符号)。
(2)正化合价最高的元素,在周期表中位于___________ 族。
(3)其单质既能与盐酸反应,又能与NaOH溶液反应的元素,其最高价氧化物对应的水化物具有___________ (填“酸性”“碱性”或“两性”)。
(4)第三周期中,原子半径最大的是(稀有气体元素除外)___________ (填元素名称)。
(5)推测稳定性H2O___________ NH3(填“大于”或“小于”)
(1)非金属性最强的元素为
(2)正化合价最高的元素,在周期表中位于
(3)其单质既能与盐酸反应,又能与NaOH溶液反应的元素,其最高价氧化物对应的水化物具有
(4)第三周期中,原子半径最大的是(稀有气体元素除外)
(5)推测稳定性H2O
您最近一年使用:0次
8 . 下表是元素周期表的一部分根据A~G元素在周期表中的位置,用化学式填写空白。
(1)氧化性最强的单质是______ ,还原性最强的单质是______ ,化学性质最不活泼的单质是______ 。(填相应的化学式)
(2)最稳定的氢化物是______ 。(填相应的化学式)
(3)按碱性逐渐减弱、酸性逐渐增强的顺序,将B、C、E、G四种元素的最高价氧化物对应水化物的化学式排列成序是__________________ 。(填相应的化学式)
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | A | |||||||
| 2 | D | F | H | |||||
| 3 | B | C | E | G |
(1)氧化性最强的单质是
(2)最稳定的氢化物是
(3)按碱性逐渐减弱、酸性逐渐增强的顺序,将B、C、E、G四种元素的最高价氧化物对应水化物的化学式排列成序是
您最近一年使用:0次
名校
解题方法
9 . 填空下列空白。
(1)原子种类由___ 决定;
(2)元素种类由___ 决定;
(3)原子的质量主要决定于___ ;
(4)原子的质量数主要由___ 决定;
(5)原子半径由___ 决定;
(6)1~18号元素的化合价主要由__ 决定。
(1)原子种类由
(2)元素种类由
(3)原子的质量主要决定于
(4)原子的质量数主要由
(5)原子半径由
(6)1~18号元素的化合价主要由
您最近一年使用:0次
名校
10 . 填空
(1)写出表示含有8个质子、10个中子的原子的化学符号_______ 。
(2)元素周期表中,所含元素超过18种的周期是_______ 。
(1)写出表示含有8个质子、10个中子的原子的化学符号
(2)元素周期表中,所含元素超过18种的周期是
您最近一年使用:0次



