名校
解题方法
1 . 元素周期表的第三周期共有______ 种元素;在第三周期元素中,最高价氧化物对应的水化物碱性最强的是__________ (填化学式,下同);最高价氧化物对应的水化物酸性最强的是________ 。
您最近一年使用:0次
2017-05-04更新
|
609次组卷
|
2卷引用:湖南省长沙市长郡中学2016-2017学年高一下学期期中考试化学试题
2 . 甲、乙、丙、丁、戊代表五种元素.请填空:
(1)甲元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素名称为_______ ,其基态原子的电子排布式为_______ .
(2)乙元素的负一价离子和丙元素的正一价离子的电子层结构都与氩相同,乙的元素符号为_______ ,丙元素的基态原子的电子排布式为_______ .
(3)丁元素的正三价离子的3d能级为半充满,丁的元素符号为_______ ,其基态原子的电子排布式为_______ .
(4)戊元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,该元素在周期表中的位置是_______ (指明周期与族),其基态原子价层电子排布式为_______ .
(1)甲元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素名称为
(2)乙元素的负一价离子和丙元素的正一价离子的电子层结构都与氩相同,乙的元素符号为
(3)丁元素的正三价离子的3d能级为半充满,丁的元素符号为
(4)戊元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,该元素在周期表中的位置是
您最近一年使用:0次
2017-04-24更新
|
144次组卷
|
3卷引用:江苏省江阴市四校2016-2017学年高二下学期期中考试化学试题
名校
3 . 填空题
(1)H、D、T三种原子,它们之间的关系是_________ ;在标准状况下,它们的单质的密度之比为_____ ;1 mol各单质中,它们的质子数之比为________ ;在标准状况下,1L各种单质中,它们的电子数之比为________ 。
(2)第116号元素(元素符号Lv)被中国科学技术名词审定委员会命名为垃,该元素在元素周期表中的位置是_____ ,属于______ 元素(填“金属”或“非金属”),若该元素存在最高价氧化物对应的水化物,则其化学式为_______ 。
(3)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。请把与下面元素有关性质相符的曲线标号(A~G)填入相应的空格中:
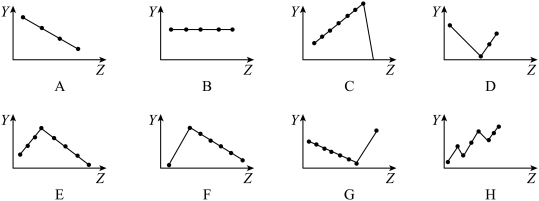
①IIA族元素的价电子数________ ;
②第三周期元素的最高正化合价________ ;
③VIIA族元素氢化物的沸点____________ 。
(4)核内中子数为N的R2+,质量数为A,则ng它的相同价态氧化物中所含的电子的物质的量约为_____ mol。
①若R为钙元素,且N=19,则采用原子符号的表达方式,可将R2+表示为_______ ;
②若R为第五周期IIA元素,则其硫酸盐______ 于水(填“溶”或“不溶”)。
(1)H、D、T三种原子,它们之间的关系是
(2)第116号元素(元素符号Lv)被中国科学技术名词审定委员会命名为垃,该元素在元素周期表中的位置是
(3)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。请把与下面元素有关性质相符的曲线标号(A~G)填入相应的空格中:

①IIA族元素的价电子数
②第三周期元素的最高正化合价
③VIIA族元素氢化物的沸点
(4)核内中子数为N的R2+,质量数为A,则ng它的相同价态氧化物中所含的电子的物质的量约为
①若R为钙元素,且N=19,则采用原子符号的表达方式,可将R2+表示为
②若R为第五周期IIA元素,则其硫酸盐
您最近一年使用:0次
4 . VIA 元素的各种性质可归纳整理如下:
回答下列问题:
(1)碲(Te)的氧化物分子式是____________________ 。
(2)硒酸与碲酸酸性较强的是____________________ (填化学式)。
(3)比较键能:H—S_____ H—Se(填“>”或“<”)。
(4)氢硒酸放在空气中,可能发生反应的化学方程式为______________________________ 。
(5)下图所示为 VIA 族元素单质与 H2反应过程中体系温度变化示意图,其中 a、b、c 分别表示VIA 族中某一元素的单质,下图为相同物质的量的单质与 H2反应过程中的体系温度变化。
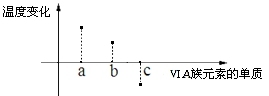
则:c 代表__________ 。(均写单质名称)
| 性质 | 8O | 16S | 34Se | 52Te |
| 单质熔点/°C | -218.4 | 113 | 271 | 450 |
| 单质沸点/°C | -183 | 444.6 | 685 | 1390 |
| 单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
回答下列问题:
(1)碲(Te)的氧化物分子式是
(2)硒酸与碲酸酸性较强的是
(3)比较键能:H—S
(4)氢硒酸放在空气中,可能发生反应的化学方程式为
(5)下图所示为 VIA 族元素单质与 H2反应过程中体系温度变化示意图,其中 a、b、c 分别表示VIA 族中某一元素的单质,下图为相同物质的量的单质与 H2反应过程中的体系温度变化。

则:c 代表
您最近一年使用:0次
名校
5 . 下表列出了①~⑨九种元素在周期表中的位置。
请按要求回答下列问题:
(1)①~⑨九种元素中非金属性最强的是________ (填元素符号)。
(2)元素⑧的原子结构示意图是_________ ;由①、④、⑥三种元素组成的化合物,其电子式是_________ 。
(3)元素②、⑧的气态氢化物的稳定性较强的是________________ (填化学式);元素③、⑨的最高价氧化物对应的水化物的酸性较强的是________________ (填化学式)。
(4)③、④、⑧三种元素的原子半径由大到小的顺序是________________ (填元素符号)。
(5)元素⑤、⑥组成的化合物的化学键类型是________________________ 。
(6)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式是________________
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
请按要求回答下列问题:
(1)①~⑨九种元素中非金属性最强的是
(2)元素⑧的原子结构示意图是
(3)元素②、⑧的气态氢化物的稳定性较强的是
(4)③、④、⑧三种元素的原子半径由大到小的顺序是
(5)元素⑤、⑥组成的化合物的化学键类型是
(6)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式是
您最近一年使用:0次
2016-12-09更新
|
655次组卷
|
6卷引用:2015-2016学年广西桂林十八中高一下开学测化学试卷
解题方法
6 . 钠、铝、碳、硅是四种常见的化学元素。请回答下列问题:
(1)五种元素中,原子半径最大的是____________________ (填元素符号),单质广泛用作半导体材料的是____________________ (填化学式)。
(2)铝在周期表中位于第____________________ 周期第____________________ 族,氧化铝在另三种元素之一的最高价氧化物对应的水化物溶液中可溶解,写出反应的离子方程式:____________________ 。
(3)工业上由下列物质冶炼相应金属时与冶炼铝采用相同方法的是____________________ (填选项代号)。
(4)生产上常利用金属铝与Fe2O3在高温下的反应来进行焊接钢轨,请写出该反应的化学方程式:____________________ 。
(1)五种元素中,原子半径最大的是
(2)铝在周期表中位于第
(3)工业上由下列物质冶炼相应金属时与冶炼铝采用相同方法的是
| A.Fe2O3 | B.MgCl2 | C.NaCl | D.HgO |
(4)生产上常利用金属铝与Fe2O3在高温下的反应来进行焊接钢轨,请写出该反应的化学方程式:
您最近一年使用:0次
7 . 假定元素周期表是有限的,根据已知的元素周期表的某些事实和理论可归纳出一些假说。
(1)已知元素周期表中的各周期可排元素种类如下:
人们预测元素周期表第八周期将来也会排满,那么该周期排满后的元素种数是________________ 。
A.18 B.32 C.50 D.无法判断
(2)根据周期表中每个周期非金属元素的种数(把稀有气体元素看做非金属元素),预测周期表中应该有___________ 种非金属元素,还有__________ 种未发现。未发现的非金属元素处于__________ 周期_________ 族。
(3)小明同学所在的化学探究小组,在查阅相关资料后归纳出元素周期表的另一种画法——三角形元素周期表的一部分,图上标有第ⅦA族和碳、钾两种元素的位置。

回答下列问题:
①请在图中将过渡元素所在的位置涂黑______________ 。
②画出B元素价电子排布图____________________ 。
(1)已知元素周期表中的各周期可排元素种类如下:
| 周期 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 元素种类 | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
A.18 B.32 C.50 D.无法判断
(2)根据周期表中每个周期非金属元素的种数(把稀有气体元素看做非金属元素),预测周期表中应该有
(3)小明同学所在的化学探究小组,在查阅相关资料后归纳出元素周期表的另一种画法——三角形元素周期表的一部分,图上标有第ⅦA族和碳、钾两种元素的位置。

回答下列问题:
①请在图中将过渡元素所在的位置涂黑
②画出B元素价电子排布图
您最近一年使用:0次
2016-12-09更新
|
241次组卷
|
3卷引用:2015-2016学年四川省雅安市天全中学高二9月月考化学试卷
2015-2016学年四川省雅安市天全中学高二9月月考化学试卷2017届湖北省老河口市江山中学高三10月月考化学卷(已下线)模块同步卷02 原子结构与元素的性质-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)
8 . 下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白(涉及表中元素一律用对应化学符号表示):
(1)在这些元素中,化学性质最不活泼的是:________ (填具体元素符号,下同),原子结构示意图为________ 。元素⑩名称为________ 在周期表中的位置________ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是________ ,碱性最强的化合物的电子式是:________ 。
(3)用电子式表示元素④与⑥的化合物的形成过程:________________ ,该化合物属于________ (填“共价”或“离子”)化合物。
(4)表示①与⑦的化合物的电子式________ ,该化合物是由________ (填”极性”、“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是______________ 。
(6)元素③的氢化物的结构式为________ ;该氢化物常温下和元素⑦的单质反应的化学方程式为_________________________________ 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的是:
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)用电子式表示元素④与⑥的化合物的形成过程:
(4)表示①与⑦的化合物的电子式
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是
(6)元素③的氢化物的结构式为
您最近一年使用:0次
2016-12-09更新
|
644次组卷
|
6卷引用:2014-2015辽宁师大附中高一下学期第一次月考化学试卷
9-10高一下·福建龙岩·期中
9 . 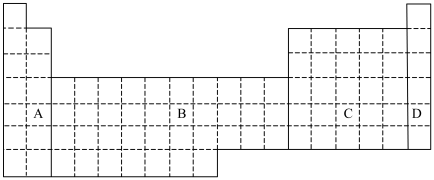
(1)在上面元素周期表中的A、B、、C、D四个区域中,全部是金属元素的区域为___________ 。
(2)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等_____ 。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
②甲、乙两元素,金属性较强的是_____ (填名称),能验证该结论的实验是___ (填编号)
a.将在空气中放置已久的这两种元素的块状单质分别放入热水中
b.将这两种元素单质的粉末分别和同浓度的盐酸反应
c.将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
d.比较这两种元素的气态氢化物的稳定性

(1)在上面元素周期表中的A、B、、C、D四个区域中,全部是金属元素的区域为
(2)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
②甲、乙两元素,金属性较强的是
a.将在空气中放置已久的这两种元素的块状单质分别放入热水中
b.将这两种元素单质的粉末分别和同浓度的盐酸反应
c.将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
d.比较这两种元素的气态氢化物的稳定性
您最近一年使用:0次
10 . 针对下面10种元素,完成以下各小题
(1)地壳中含量最多的元素是___________ (填名称)。
(2)化学性质最不活泼的元素是___________ (填元素符号)。
(3)Al的原子结构示意图为___________________ 。
(4)C与N相比,原子半径较小的是___________ 。
(5)最高价氧化物对应的水化物碱性最强的是___________ (填化学式)。
(6)MgO和Al2O3中,属于两性氧化物的是___________ 。
(7)S和Cl相比,元素非金属性较强的是___________ 。
(1)地壳中含量最多的元素是
| 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Al | Si | S | Cl | Ne |
(2)化学性质最不活泼的元素是
(3)Al的原子结构示意图为
(4)C与N相比,原子半径较小的是
(5)最高价氧化物对应的水化物碱性最强的是
(6)MgO和Al2O3中,属于两性氧化物的是
(7)S和Cl相比,元素非金属性较强的是
您最近一年使用:0次



