1 . 根据下列有机物,回答问题:
①CH3CH3 ②CH2=CH2 ③CH3CH2OH_______ (填数字序号)的产量。
(2)水壶结有水垢时,可用适量_______ (填数字序号)浸泡。
(3)①和⑤互为_______ (填“同系物"或“同分异构体”,下同),⑤和⑥互为_______ 。
(4)③的官能团是_______ 。
(5)(5)CH2=CH2 + H2O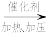 CH3CH2OH,该反应的反应类型为
CH3CH2OH,该反应的反应类型为_______ 。
(6)在一定条件下,③和④反应的化学方程式为_______ 。
①CH3CH3 ②CH2=CH2 ③CH3CH2OH
④CH3COOH ⑤CH3CH2CH2CH3 ⑥
(2)水壶结有水垢时,可用适量
(3)①和⑤互为
(4)③的官能团是
(5)(5)CH2=CH2 + H2O
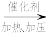 CH3CH2OH,该反应的反应类型为
CH3CH2OH,该反应的反应类型为(6)在一定条件下,③和④反应的化学方程式为
您最近一年使用:0次
2 . 氮及其化合物与生产生活及环境息息相关。请回答下列问题:
(1)N2在常温下性质很稳定,任意写出一种与此性质有关的用途:_____ 。
(2)硝酸与金属反应会产生氮氧化物。
①下列环境问题与氮的氧化物排放无关的是_____ 。
A.酸雨 B.光化学烟雾 C. 白色污染 D.温室效应
②在含有a g HNO3的稀硝酸中,加入b g铁粉充分反应,铁全部溶解并生成NO,有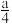 g HNO3被还原,则a∶b可能为
g HNO3被还原,则a∶b可能为_____ 。
A.2∶1 B.3∶1 C.4∶1 D.9∶2
(3)汽车尾气中存在NO和CO,通过在排气管处加装催化剂,可以使其转化为对环境友好的物质,请写出发生反应的化学方程式_____ ,氧化产物与还原产物的物质的量之比为_____ 。
(1)N2在常温下性质很稳定,任意写出一种与此性质有关的用途:
(2)硝酸与金属反应会产生氮氧化物。
①下列环境问题与氮的氧化物排放无关的是
A.酸雨 B.光化学烟雾 C. 白色污染 D.温室效应
②在含有a g HNO3的稀硝酸中,加入b g铁粉充分反应,铁全部溶解并生成NO,有
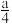 g HNO3被还原,则a∶b可能为
g HNO3被还原,则a∶b可能为A.2∶1 B.3∶1 C.4∶1 D.9∶2
(3)汽车尾气中存在NO和CO,通过在排气管处加装催化剂,可以使其转化为对环境友好的物质,请写出发生反应的化学方程式
您最近一年使用:0次
名校
解题方法
3 . 按要求回答下列问题:
(1)烷烃A在同温、同压下蒸汽的密度是H2的36倍,其分子式为______ 。
(2)某化合物B的分子式为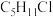 ,分析数据表明:分子中有两个
,分析数据表明:分子中有两个 、两个
、两个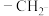 、一个
、一个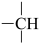 和一个
和一个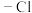 ,它的可能的结构有
,它的可能的结构有______ 种。
(3)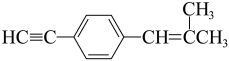 最多有
最多有______ 个原子在同一面上,最多有______ 个原子在同一条直线上。
(4)有机物C的结构简式为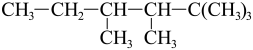 ,若C的一种同分异构体只能由一种烯烃加氢得到,且该烯烃是一个高度对称的结构,存在顺反异构体,写出这种烯烃的顺式异构体的结构简式
,若C的一种同分异构体只能由一种烯烃加氢得到,且该烯烃是一个高度对称的结构,存在顺反异构体,写出这种烯烃的顺式异构体的结构简式______ 。
(5)有机物D(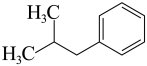 )的同分异构体中,苯环上的一氯代物只有一种的有
)的同分异构体中,苯环上的一氯代物只有一种的有______ 种,写出其中任意一种的结构简式______ 。
(1)烷烃A在同温、同压下蒸汽的密度是H2的36倍,其分子式为
(2)某化合物B的分子式为
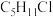 ,分析数据表明:分子中有两个
,分析数据表明:分子中有两个 、两个
、两个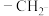 、一个
、一个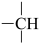 和一个
和一个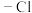 ,它的可能的结构有
,它的可能的结构有(3)
 最多有
最多有(4)有机物C的结构简式为
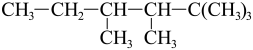 ,若C的一种同分异构体只能由一种烯烃加氢得到,且该烯烃是一个高度对称的结构,存在顺反异构体,写出这种烯烃的顺式异构体的结构简式
,若C的一种同分异构体只能由一种烯烃加氢得到,且该烯烃是一个高度对称的结构,存在顺反异构体,写出这种烯烃的顺式异构体的结构简式(5)有机物D(
 )的同分异构体中,苯环上的一氯代物只有一种的有
)的同分异构体中,苯环上的一氯代物只有一种的有
您最近一年使用:0次
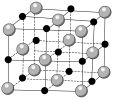
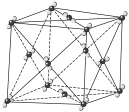
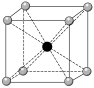
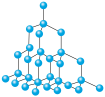
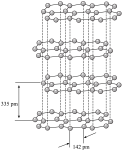
4 . 下图表示一些晶体中的某些结构,它们分别是NaCl、干冰、CsCl、金刚石、石墨晶体结构中的某一种的某一部分。
(1)代表金刚石的是___________ (填字母,下同),金刚石属于___________ 晶体,其中每个碳原子采取___________ 杂化轨道形成共价键三维骨架结构。
(2)代表石墨的是___________ ,石墨属于混合型晶体。石墨晶体是层状结构,其中每个正六边形占有碳原子数平均为___________ 个。层间没有化学键相连,是靠___________ 维系的。
(3)代表NaCl晶体的是___________ ,每个Cl―紧邻着___________ 个Na+。每个晶胞中有___________ 个Na+。
(4)代表CsCl晶体的是___________ ,它属于___________ 晶体。每个Cs+紧邻着___________ 个Cl―。
(5)代表干冰的是___________ ,它属于___________ 晶体,每个CO2分子与___________ 个CO2分子紧邻。
|
|
|
| A | B | C |
|
| |
| D | E |
(1)代表金刚石的是
(2)代表石墨的是
(3)代表NaCl晶体的是
(4)代表CsCl晶体的是
(5)代表干冰的是
您最近一年使用:0次
5 . 按要求回答下列问题:
(1)写出下列有机物的系统命名或结构简式______ 。
④2,5—二甲基—4—乙基庚烷______ 。
(2)写出下列有关反应的化学方程式
①丙烯一定条件下可制得2—丙醇:____________ 。
②由甲苯制TNT炸药:______ 。
③异戊二烯一定条件下可制得聚异戊二烯橡胶:______ 。
④甲苯光照条件下与氯气生成一氯代物:______ 。
(1)写出下列有机物的系统命名或结构简式
①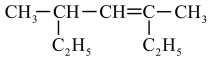
②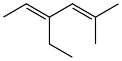
④2,5—二甲基—4—乙基庚烷
(2)写出下列有关反应的化学方程式
①丙烯一定条件下可制得2—丙醇:
②由甲苯制TNT炸药:
③异戊二烯一定条件下可制得聚异戊二烯橡胶:
④甲苯光照条件下与氯气生成一氯代物:
您最近一年使用:0次
名校
解题方法
6 . 铁是人类使用最早的金属之一。运用所学知识,回答下列问题:
(1)电子工业用FeCl3,溶液腐蚀覆在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的化学方程式为______ 。
(2)某研究性学习小组为测定FeCl3溶液腐蚀铜后所得溶液的组成,进行了如下实验:
①取少量待测溶液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子有______ 。
②验证该溶液中是否含有Fe2+,正确的实验方法是______ (填序号)。
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.取适量溶液先滴入双氧水再滴入KSCN溶液,若溶液显红色,证明原溶液中含有Fe2+
D.取适量溶液,滴入K3[Fe(CN)6]溶液,若产生蓝色沉淀,证明含有Fe2+
(3)工程师欲从制造印刷电路板的废液中回收铜,并获得FeCl3,溶液,设计如下方案:______ 。
②向滤液B和滤液E中通入F的目的是______ ,该反应的离子方程式为______ 。
③向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是______ (填序号)。
A.有铜单质剩余但无铁单质剩余 B.有铁单质剩余但无铜单质剩余
C.铁、铜单质都有剩余 D.铁、铜单质都无剩余
(1)电子工业用FeCl3,溶液腐蚀覆在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的化学方程式为
(2)某研究性学习小组为测定FeCl3溶液腐蚀铜后所得溶液的组成,进行了如下实验:
①取少量待测溶液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子有
②验证该溶液中是否含有Fe2+,正确的实验方法是
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.取适量溶液先滴入双氧水再滴入KSCN溶液,若溶液显红色,证明原溶液中含有Fe2+
D.取适量溶液,滴入K3[Fe(CN)6]溶液,若产生蓝色沉淀,证明含有Fe2+
(3)工程师欲从制造印刷电路板的废液中回收铜,并获得FeCl3,溶液,设计如下方案:
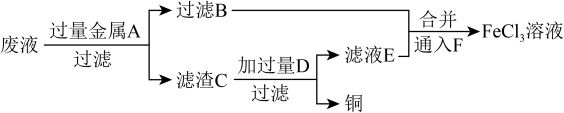
②向滤液B和滤液E中通入F的目的是
③向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
A.有铜单质剩余但无铁单质剩余 B.有铁单质剩余但无铜单质剩余
C.铁、铜单质都有剩余 D.铁、铜单质都无剩余
您最近一年使用:0次
解题方法
7 . 电负性与电离能是两种定量描述元素原子得失电子能力的参数,请根据下列数据回答问题。
(1)非金属性:S___________ (填“>”、“=”或“<”)F。
(2)依据电负性数值,上述元素中最容易形成离子键的是___________ 和___________ 。
(3)已知某主族元素Y,其基态原子核外有2个电子层,3个未成对电子,Y元素基态原子的轨道表示式为___________ ,通过分析电负性的变化规律,确定Y元素电负性的取值范围是___________ 。
(4)由电负性数据推断:化合物PBr3中P的化合价为___________ 。已知PBr3与水反应是非氧化还原反应,写出PBr3与水反应的化学方程式___________ 。
| 元素符号 | Li | Be | C | O | F | Na | Al | P | S | Br |
| 电负性 | 1.0 | 1.5 | 2.5 | 3.5 | 4.0 | 0.9 | 1.5 | 2.2 | 2.5 | 2.8 |
(2)依据电负性数值,上述元素中最容易形成离子键的是
(3)已知某主族元素Y,其基态原子核外有2个电子层,3个未成对电子,Y元素基态原子的轨道表示式为
(4)由电负性数据推断:化合物PBr3中P的化合价为
您最近一年使用:0次
解题方法
8 . 氢氧燃料电池是一种常见化学电源,其工作示意图如图。___________ (用a或b填写),其电极反应为___________ 。
(2)关于该电池,下列说法正确的是___________。
(3)若用 作燃料,以KOH溶液为电解质溶液,则
作燃料,以KOH溶液为电解质溶液,则 通入电池的
通入电池的___________ (填“正极”或“负极”),该电极反应方程式为___________ 。
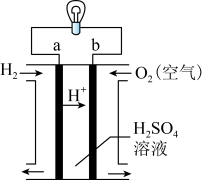
(2)关于该电池,下列说法正确的是___________。
A. 由正极流向负极 由正极流向负极 |
B. 溶液的作用是传导电子 溶液的作用是传导电子 |
| C.该电池工作一段时间后,电解质溶液的酸性减弱 |
D.标准状况下a电极若每消耗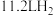 ,外电路转移电子数为 ,外电路转移电子数为 |
(3)若用
 作燃料,以KOH溶液为电解质溶液,则
作燃料,以KOH溶液为电解质溶液,则 通入电池的
通入电池的
您最近一年使用:0次
解题方法
9 . 请回答:
(1)①氧化铝的化学式_______ ,②氯气的电子式是_______ 。
(2)向FeCl3溶液中滴加NaOH,产生_______ 色沉淀。
(3)浓硝酸见光分解的化学方程式是_______ 。
(1)①氧化铝的化学式
(2)向FeCl3溶液中滴加NaOH,产生
(3)浓硝酸见光分解的化学方程式是
您最近一年使用:0次
名校
10 . 回答下列问题
(1)写出 的价电子排布式
的价电子排布式______ 。
(2)实验室用软锰矿和浓盐酸制氯气,写出该反应的化学方程式______ 。
(3)在常温下, 溶液的pH=9,则溶液中由水电离出来的
溶液的pH=9,则溶液中由水电离出来的
______ 。
(4)火箭发射可以用肼( ,液态)作燃料,
,液态)作燃料, 作氧化剂,两者反应生成
作氧化剂,两者反应生成 和水蒸气。
和水蒸气。
已知:
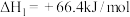 ;
;
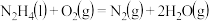
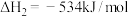
请写出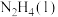 与
与 反应的热化学方程式
反应的热化学方程式______ 。
(5)下表列出了某短周期元素R的各级电离能数据(用 、
、 ……表示)。
……表示)。
关于元素R的下列推断中,正确的是______ (用相应的编号填写)
①R元素位于元素周期表中第ⅡA族
②R元素基态原子的电子排布式为
③R元素的最高价氧化物可表示为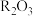
④R元素的第一电离能高于同周期相邻元素的第一电离能
(1)写出
 的价电子排布式
的价电子排布式(2)实验室用软锰矿和浓盐酸制氯气,写出该反应的化学方程式
(3)在常温下,
 溶液的pH=9,则溶液中由水电离出来的
溶液的pH=9,则溶液中由水电离出来的
(4)火箭发射可以用肼(
 ,液态)作燃料,
,液态)作燃料, 作氧化剂,两者反应生成
作氧化剂,两者反应生成 和水蒸气。
和水蒸气。已知:

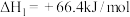 ;
;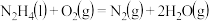
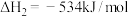
请写出
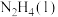 与
与 反应的热化学方程式
反应的热化学方程式(5)下表列出了某短周期元素R的各级电离能数据(用
 、
、 ……表示)。
……表示)。元素 | 电离能 | |||||
|
|
|
|
| … | |
| 740 | 1500 | 7700 | 10500 | 13630 | … |
①R元素位于元素周期表中第ⅡA族
②R元素基态原子的电子排布式为

③R元素的最高价氧化物可表示为
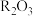
④R元素的第一电离能高于同周期相邻元素的第一电离能
您最近一年使用:0次