解题方法
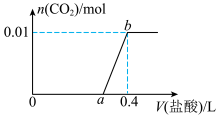
1 . 向NaOH和Na2CO3混合溶液中滴加0.1 mol·L-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示回答下列问题_______ 。_______
(2)ab段发生的化学反应方程式为_______ 。
(3)a的值是_______ 、NaOH的物质的量为_______ 、NaOH和Na2CO3的物质的量浓度之比为_______ 。
(2)ab段发生的化学反应方程式为
(3)a的值是
您最近一年使用:0次
2 . 按要求回答下列问题:
(1)用标准碘溶液滴定溶有 的水溶液,以测定水中
的水溶液,以测定水中 的含量,应选用
的含量,应选用___________ 作指示剂,达到滴定终点的现象是___________ 。
(2)①已知常温下 的电离平衡常数
的电离平衡常数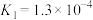 ,
,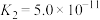 ,则NaHSe溶液呈
,则NaHSe溶液呈___________ (填“酸性”或“碱性”),该溶液中的元素守恒关系式为___________ 。
② 在一定条件下可以制备出CuSe,已知常温时CuSe的
在一定条件下可以制备出CuSe,已知常温时CuSe的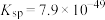 ,CuS的
,CuS的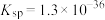 ,则反应
,则反应 的化学平衡常数
的化学平衡常数
___________ (保留两位有效数字)。
(3)在化学分析中采用 为指示剂,以
为指示剂,以 标准溶液滴定溶液中的
标准溶液滴定溶液中的 ,利用
,利用 与
与 生成砖红色沉淀,指示到达滴定终点。当溶液中
生成砖红色沉淀,指示到达滴定终点。当溶液中 恰好完全沉淀(浓度等于
恰好完全沉淀(浓度等于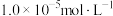 )时,溶液中
)时,溶液中 为
为___________  ,此时溶液中
,此时溶液中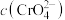 等于
等于___________  (已知
(已知 、AgCl的
、AgCl的 分别为
分别为 和
和 )。
)。
(1)用标准碘溶液滴定溶有
 的水溶液,以测定水中
的水溶液,以测定水中 的含量,应选用
的含量,应选用(2)①已知常温下
 的电离平衡常数
的电离平衡常数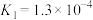 ,
,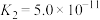 ,则NaHSe溶液呈
,则NaHSe溶液呈②
 在一定条件下可以制备出CuSe,已知常温时CuSe的
在一定条件下可以制备出CuSe,已知常温时CuSe的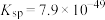 ,CuS的
,CuS的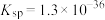 ,则反应
,则反应 的化学平衡常数
的化学平衡常数
(3)在化学分析中采用
 为指示剂,以
为指示剂,以 标准溶液滴定溶液中的
标准溶液滴定溶液中的 ,利用
,利用 与
与 生成砖红色沉淀,指示到达滴定终点。当溶液中
生成砖红色沉淀,指示到达滴定终点。当溶液中 恰好完全沉淀(浓度等于
恰好完全沉淀(浓度等于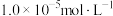 )时,溶液中
)时,溶液中 为
为 ,此时溶液中
,此时溶液中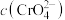 等于
等于 (已知
(已知 、AgCl的
、AgCl的 分别为
分别为 和
和 )。
)。
您最近一年使用:0次
解题方法
3 . 前四周期元素及其化合物在生产、生活中应用广泛。回答下列问题:
(1)下列状态的N原子或离子在跃迁时,用光谱仪可捕捉到发射光谱的是___________ (填序号)。
a. b.
b. c.
c.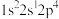 d.
d.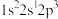
(2)某云母片岩石的主要成分为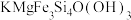 ,含有少量Cr(杂质)。
,含有少量Cr(杂质)。
①Mg的基态原子的电子排布式为___________ ,其原子核外电子填充的能级数目为___________ 。
②Cr元素在元素周期表中的位置为___________ 。
(3)基态Na原子中,核外电子的空间运动状态有___________ 种,其占据的最高能级电子云轮廓图形状为___________ 。
(4)在元素周期表中,As是___________ 区元素;与磷同周期且第一电离能大于磷元素的有___________ (写元素符号)。
(1)下列状态的N原子或离子在跃迁时,用光谱仪可捕捉到发射光谱的是
a.
 b.
b. c.
c.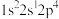 d.
d.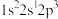
(2)某云母片岩石的主要成分为
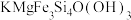 ,含有少量Cr(杂质)。
,含有少量Cr(杂质)。①Mg的基态原子的电子排布式为
②Cr元素在元素周期表中的位置为
(3)基态Na原子中,核外电子的空间运动状态有
(4)在元素周期表中,As是
您最近一年使用:0次
解题方法
4 . 下表为元素周期表的一部分,请参照元素在表中①~⑩的位置,用相应的化学用语回答下列问题:
(1)形成化合物种类最多的元素在周期表中的位置是_______ 。
(2)元素③的最简单氢化物与元素⑩的最简单氢化物可发生化学反应,请写出该反应的化学方程式:_______ ,其中生成物的电子式为_______ 。
(3)②、③、④、⑤元素形成的最简单氢化物中,热稳定性最强的是_______ (填化学式),原因是_______ (从原子结构角度分析),④、⑨简单氢化物中,沸点较高的是_______ (填化学式),原因是_______ 。
(4)下列事实能说明⑩元素原子得电子能力比⑨元素原子强的是_______ (填序号)。
①氢化物的溶解度:⑩>⑨ ②氢化物的酸性:⑩>⑨
③氢化物的稳定性:⑩>⑨ ④氢化物的还原性:⑩<⑨
⑤最高价氧化物对应的水化物的酸性:⑩>⑨
族 周期 | IA | 0 | ||||||
| 1 | IIA | IIIA | IVA | VA | VIA | VIIA | ||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
(2)元素③的最简单氢化物与元素⑩的最简单氢化物可发生化学反应,请写出该反应的化学方程式:
(3)②、③、④、⑤元素形成的最简单氢化物中,热稳定性最强的是
(4)下列事实能说明⑩元素原子得电子能力比⑨元素原子强的是
①氢化物的溶解度:⑩>⑨ ②氢化物的酸性:⑩>⑨
③氢化物的稳定性:⑩>⑨ ④氢化物的还原性:⑩<⑨
⑤最高价氧化物对应的水化物的酸性:⑩>⑨
您最近一年使用:0次
5 . H、C、N、O与Mn、Fe、Cu等形成的多种化合物在生产和生活中有广泛应用。回答下列问题:
(1)H、C、N、O四种元素的电负性由大到小的顺序为_______ 。
(2)Mn位于元素周期表中的位置是_______ ;Mn和O基态原子的核外未成对电子数较多的是_______ 。
(3)在元素周期表中,Cu位于_______ 区,基态Cu原子价层电子排布式为_______ ,Cu元素有两种常见离子,化合价为+1和+2,从结构上分析其基态离子更稳定的是_______ 。
(4)含有Cu元素的盐的焰色试验为绿色,许多金属盐都可以发生焰色试验,其原因是______ 。
(5)基态Fe等多原子核外电子排布中,能级会发生交错现象。以下表示的各能级能量大小关系,不符合客观事实的是_______ 。
a.4s>3s>2s>1s b.4s>4p>4d>4f c.6s>5p>4d>3d
(1)H、C、N、O四种元素的电负性由大到小的顺序为
(2)Mn位于元素周期表中的位置是
(3)在元素周期表中,Cu位于
(4)含有Cu元素的盐的焰色试验为绿色,许多金属盐都可以发生焰色试验,其原因是
(5)基态Fe等多原子核外电子排布中,能级会发生交错现象。以下表示的各能级能量大小关系,不符合客观事实的是
a.4s>3s>2s>1s b.4s>4p>4d>4f c.6s>5p>4d>3d
您最近一年使用:0次
6 . 1861年比利时人索尔维(E.Solvay)提出氨碱法用以生产纯碱。该法以① 、②
、② 、③
、③ 为原料制取④
为原料制取④ ,再将
,再将 煅烧生成⑤
煅烧生成⑤ 。该法具有技术成熟,原料来源丰富且价廉等优点,但食盐的利用率低,氨损失大,⑥
。该法具有技术成熟,原料来源丰富且价廉等优点,但食盐的利用率低,氨损失大,⑥ 用处不大。我国杰出化工专家侯德榜针对氨碱法的不足,将制碱和合成氨创造性地结合起来,于1942年成功发明了联合制碱法,该法革除了用⑦
用处不大。我国杰出化工专家侯德榜针对氨碱法的不足,将制碱和合成氨创造性地结合起来,于1942年成功发明了联合制碱法,该法革除了用⑦ 生产
生产 这一工段,使食盐的利用率提高到
这一工段,使食盐的利用率提高到 ,同时可生产化肥⑧
,同时可生产化肥⑧ ,其部分工艺流程如下:
,其部分工艺流程如下:
(1)上文标有序号的物质中,属于碳酸盐的是_______ (填序号);不是电解质的是_______ (填序号)。
(2)写出⑧的电离方程式_______ 。
(3)④可用于治疗胃酸(主要成分为盐酸)过多,其原理是_______ (用离子方程式表示)。
(4)写出 和饱和食盐水发生反应的化学方程式
和饱和食盐水发生反应的化学方程式_______ 。
(5)工业纯碱中常含有少量 ,现取
,现取 该样品,向其中加入足量稀硫酸,充分反应后,产生标准状况下的
该样品,向其中加入足量稀硫酸,充分反应后,产生标准状况下的 气体
气体 ,则该样品中
,则该样品中 的质量分数为
的质量分数为_______ (保留一位小数)。
 、②
、② 、③
、③ 为原料制取④
为原料制取④ ,再将
,再将 煅烧生成⑤
煅烧生成⑤ 。该法具有技术成熟,原料来源丰富且价廉等优点,但食盐的利用率低,氨损失大,⑥
。该法具有技术成熟,原料来源丰富且价廉等优点,但食盐的利用率低,氨损失大,⑥ 用处不大。我国杰出化工专家侯德榜针对氨碱法的不足,将制碱和合成氨创造性地结合起来,于1942年成功发明了联合制碱法,该法革除了用⑦
用处不大。我国杰出化工专家侯德榜针对氨碱法的不足,将制碱和合成氨创造性地结合起来,于1942年成功发明了联合制碱法,该法革除了用⑦ 生产
生产 这一工段,使食盐的利用率提高到
这一工段,使食盐的利用率提高到 ,同时可生产化肥⑧
,同时可生产化肥⑧ ,其部分工艺流程如下:
,其部分工艺流程如下: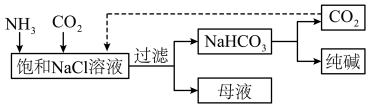
(1)上文标有序号的物质中,属于碳酸盐的是
(2)写出⑧的电离方程式
(3)④可用于治疗胃酸(主要成分为盐酸)过多,其原理是
(4)写出
 和饱和食盐水发生反应的化学方程式
和饱和食盐水发生反应的化学方程式(5)工业纯碱中常含有少量
 ,现取
,现取 该样品,向其中加入足量稀硫酸,充分反应后,产生标准状况下的
该样品,向其中加入足量稀硫酸,充分反应后,产生标准状况下的 气体
气体 ,则该样品中
,则该样品中 的质量分数为
的质量分数为
您最近一年使用:0次
7 . 生产、生活中处处有化学,利用所学化学知识回答下列问题。
(1) 气体是一种高效、环保的消毒剂,可代替氯气用于饮用水的消毒。对水进行消毒时,还可将水中的
气体是一种高效、环保的消毒剂,可代替氯气用于饮用水的消毒。对水进行消毒时,还可将水中的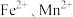 等转化为
等转化为 和
和 等难溶物除去,由此说明
等难溶物除去,由此说明 具有
具有_______ 性。
(2)工业上可以通过 与
与 反应的方法制取
反应的方法制取 ,请完成该化学反应方程式:
,请完成该化学反应方程式: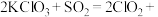
_______ 。
(3)查阅资料显示: 处理污水后的还原产物为
处理污水后的还原产物为 ,检验处理后的溶液中是否存在
,检验处理后的溶液中是否存在 的方法是
的方法是_______ 。
(4)为验证次氯酸光照分解的产物,分别利用氯离子传感器、 传感器、氧气传感器采集数据并绘制变化图像如下,其中能表示氯水的
传感器、氧气传感器采集数据并绘制变化图像如下,其中能表示氯水的 随时间变化的图像是
随时间变化的图像是_______ (填字母),用化学方程式说明这一变化的原因_______ 。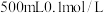 的稀盐酸,
的稀盐酸,
①需要用量筒量取 的稀盐酸
的稀盐酸_______  。
。
②需要用到的玻璃仪器除烧杯、量筒、胶头滴管、玻璃棒外,还需要_______ 。
③下列操作会使配制的溶液物质的量浓度偏低的是_______ 。
A.定容时俯视容量瓶刻度线 B.容量瓶用蒸馏水洗涤后未干燥
C.未将洗涤液转移进容量瓶 D.定容时水加多了用胶头滴管吸出
E.摇匀静置,液面下降
(1)
 气体是一种高效、环保的消毒剂,可代替氯气用于饮用水的消毒。对水进行消毒时,还可将水中的
气体是一种高效、环保的消毒剂,可代替氯气用于饮用水的消毒。对水进行消毒时,还可将水中的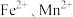 等转化为
等转化为 和
和 等难溶物除去,由此说明
等难溶物除去,由此说明 具有
具有(2)工业上可以通过
 与
与 反应的方法制取
反应的方法制取 ,请完成该化学反应方程式:
,请完成该化学反应方程式: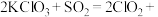
(3)查阅资料显示:
 处理污水后的还原产物为
处理污水后的还原产物为 ,检验处理后的溶液中是否存在
,检验处理后的溶液中是否存在 的方法是
的方法是(4)为验证次氯酸光照分解的产物,分别利用氯离子传感器、
 传感器、氧气传感器采集数据并绘制变化图像如下,其中能表示氯水的
传感器、氧气传感器采集数据并绘制变化图像如下,其中能表示氯水的 随时间变化的图像是
随时间变化的图像是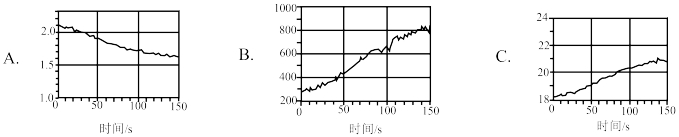
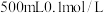 的稀盐酸,
的稀盐酸,①需要用量筒量取
 的稀盐酸
的稀盐酸 。
。②需要用到的玻璃仪器除烧杯、量筒、胶头滴管、玻璃棒外,还需要
③下列操作会使配制的溶液物质的量浓度偏低的是
A.定容时俯视容量瓶刻度线 B.容量瓶用蒸馏水洗涤后未干燥
C.未将洗涤液转移进容量瓶 D.定容时水加多了用胶头滴管吸出
E.摇匀静置,液面下降
您最近一年使用:0次
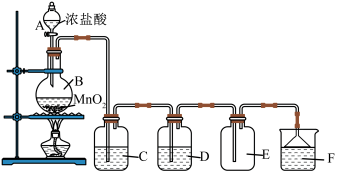
8 . 实验室中常用二氧化锰与浓盐酸共热制取氯气。某化学兴趣小组为制取较为纯净、干燥的氯气,设计如图实验装置。
(1)该实验制取 的化学方程式为
的化学方程式为_______ 。
(2)图中盛放浓盐酸的仪器名称为_______ 。
(3)C、D中盛放的试剂依次为_______ 、_______ 。
(4)F中盛放的试剂为 溶液,其作用是
溶液,其作用是_______ 。
(1)该实验制取
 的化学方程式为
的化学方程式为(2)图中盛放浓盐酸的仪器名称为
(3)C、D中盛放的试剂依次为
(4)F中盛放的试剂为
 溶液,其作用是
溶液,其作用是
您最近一年使用:0次
9 . 肼( )是长征系列运载火箭的推进剂之一、回答下列问题:
)是长征系列运载火箭的推进剂之一、回答下列问题:
(1)肼的相对分子质量是_______ 。
(2)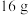 肼中含有氮原子的数目为
肼中含有氮原子的数目为_______ 。
(3)在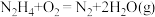 反应中,
反应中,_______ (填化学式)是还原剂, 还原剂在反应中失去
还原剂在反应中失去_______  电子。
电子。
(4)标准状况下,等质量的氧气与氮气的体积之比为_______ 。
 )是长征系列运载火箭的推进剂之一、回答下列问题:
)是长征系列运载火箭的推进剂之一、回答下列问题:(1)肼的相对分子质量是
(2)
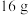 肼中含有氮原子的数目为
肼中含有氮原子的数目为(3)在
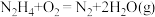 反应中,
反应中, 还原剂在反应中失去
还原剂在反应中失去 电子。
电子。(4)标准状况下,等质量的氧气与氮气的体积之比为
您最近一年使用:0次
解题方法
10 . 现有下列10种物质:①Fe(OH)3胶体②铜③干冰④3%硫酸溶液 ⑤硫酸⑥盐酸⑦烧碱 ⑧纯碱⑨水 ⑩乙醇,用序号填空:
属于混合物的是_______ ;属于氧化物的是_______ ;属于酸的是_______ ;属于碱的是_______ ;属于盐的是_______ ;属于有机物的是_______ ;可以导电的有_______ 。
属于混合物的是
您最近一年使用:0次



