名校
解题方法
1 . 高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。回答下列问题:
(1)SiO2属于___________ (填“酸性”“碱性”或“两性”)氧化物。盛装NaOH溶液的试剂瓶不能用玻璃塞,其原因为___________ (用离子方程式表示)。
(2)用氮化硅(Si3N4)陶瓷制造发动机,能大幅度提高发动机的热效率。工业上制备氮化硅的原理为:3SiCl4+2N2+6H2 Si3N4+12HCl。
Si3N4+12HCl。
①SiCl4是___________ (填“离子化合物”或“共价化合物”)。
②若该反应转移3mol电子,生成Si3N4的质量为___________ g。
(3)芯片制作中的部分流程如图:___________ 。
Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是___________ 。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.铁坩埚
②去除磷硅玻璃即除去扩散制结过程中产生的SiO2,下列试剂合适的为___________ (填标号),写出其化学方程式:___________ 。
a.浓硫酸 b.氢氟酸 c.稀硝酸
(1)SiO2属于
(2)用氮化硅(Si3N4)陶瓷制造发动机,能大幅度提高发动机的热效率。工业上制备氮化硅的原理为:3SiCl4+2N2+6H2
 Si3N4+12HCl。
Si3N4+12HCl。①SiCl4是
②若该反应转移3mol电子,生成Si3N4的质量为
(3)芯片制作中的部分流程如图:

Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是
A.普通玻璃坩埚 B.石英玻璃坩埚 C.铁坩埚
②去除磷硅玻璃即除去扩散制结过程中产生的SiO2,下列试剂合适的为
a.浓硫酸 b.氢氟酸 c.稀硝酸
您最近一年使用:0次
2 . 电解质的水溶液跟日常生活、工农业生产和环境保护息息相关。常温下,叠氮酸 是一元弱酸,高锰酸
是一元弱酸,高锰酸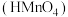 是一元强酸,
是一元强酸, 的高铼酸
的高铼酸 、
、 的高锰酸
的高锰酸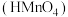 溶液分别与
溶液分别与 的
的 溶液等体积混合,所得溶液均呈中性。请回答下列问题:
溶液等体积混合,所得溶液均呈中性。请回答下列问题:
(1)高铼酸属于___________ (填“强”或“弱”)酸,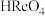 中Re的化合价为
中Re的化合价为___________ 。
(2)常温下,已知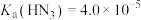 ,则
,则 的
的 溶液中
溶液中
___________  。
。
(3)已知25°C时, 的
的 ;
; 的:
的: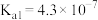
 ;HCN的
;HCN的 ,回答下列问题:
,回答下列问题:
①25°C时,向NaCN溶液中通入少量 ,反应的离子方程式为
,反应的离子方程式为___________ 。
②下列措施中能使醋酸的水溶液中 增大的同时
增大的同时 减小的是
减小的是___________ (填标号)。
A.加入 固体 B.加入固体
固体 B.加入固体 C.加入NaCN固体 D.升高温度
C.加入NaCN固体 D.升高温度
(4)常温时
 溶液,
溶液, 浓度为
浓度为___________ ,由水电离的 为
为___________ 。
 是一元弱酸,高锰酸
是一元弱酸,高锰酸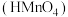 是一元强酸,
是一元强酸, 的高铼酸
的高铼酸 、
、 的高锰酸
的高锰酸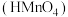 溶液分别与
溶液分别与 的
的 溶液等体积混合,所得溶液均呈中性。请回答下列问题:
溶液等体积混合,所得溶液均呈中性。请回答下列问题:(1)高铼酸属于
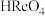 中Re的化合价为
中Re的化合价为(2)常温下,已知
 ,则
,则 的
的 溶液中
溶液中
 。
。(3)已知25°C时,
 的
的 ;
; 的:
的: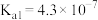
 ;HCN的
;HCN的 ,回答下列问题:
,回答下列问题:①25°C时,向NaCN溶液中通入少量
 ,反应的离子方程式为
,反应的离子方程式为②下列措施中能使醋酸的水溶液中
 增大的同时
增大的同时 减小的是
减小的是A.加入
 固体 B.加入固体
固体 B.加入固体 C.加入NaCN固体 D.升高温度
C.加入NaCN固体 D.升高温度(4)常温时

 溶液,
溶液, 浓度为
浓度为 为
为
您最近一年使用:0次
名校
3 . 请按照官能团的种类不同将下列有机化合物进行分类:___________ ,属于酚的是___________ ,属于卤代烃的是___________ 。(填选项,下同)
(2)C中所含有的官能团的名称为:___________ 。
(3)含有两种官能团的物质是:___________ 。
A. 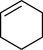 B.
B.  C.
C. 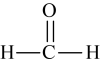 D.
D. 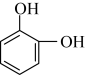 E.
E. 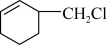 F.
F. 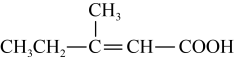 G.
G.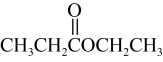
(2)C中所含有的官能团的名称为:
(3)含有两种官能团的物质是:
您最近一年使用:0次
名校
解题方法
4 . 一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:____________ 。
(2)反应开始到10 s间,用Z表示的反应速率v(Z)=____________ 。
(3)反应开始到10 s时,Y的转化率=___________ (转化率是指某反应物转化的物质的量与该反应物的起始物质的量的百分比)。
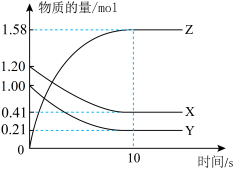
(2)反应开始到10 s间,用Z表示的反应速率v(Z)=
(3)反应开始到10 s时,Y的转化率=
您最近一年使用:0次
名校
解题方法
5 . 影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。他们利用Cu、Fe、Mg和2 mol/L硫酸设计实验方案来研究影响反应速率的因素。请完成下列实验报告:
该小组的实验目的是研究反应物本身的______ 对反应速率的影响。
| 实验内容 | 实验现象 | 结论 |
| ①分别取等体积的2 mol/L硫酸于试管中; ②分别投入大小、形状相同的Cu、Fe、Mg。 | 反应快慢:Mg | 反应物的性质越 |
您最近一年使用:0次
名校
6 . 原子结构与元素周期表存在着内在联系。根据已学知识,请回答下列问题:
(1)基态N原子电子占据___________ 个能层,电子占据的最高能级的符号是___________ ;基态N原子共有___________ 种不同空间运动状态的电子。
(2)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为:___________ ,位于元素周期表的___________ 区。
(3)比较Cu和Zn的第二电离能大小[用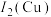 和
和 表示]:
表示]:___________ 。
(4)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填选项)。
(5)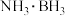 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(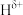 ),与B原子相连的H负电性(
),与B原子相连的H负电性(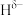 )。在H、B、N三种元素中,电负性由大到小的顺序是
)。在H、B、N三种元素中,电负性由大到小的顺序是___________ 。
(1)基态N原子电子占据
(2)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为:
(3)比较Cu和Zn的第二电离能大小[用
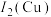 和
和 表示]:
表示]:(4)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填选项)。
A.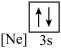 | B.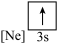 | C. | D.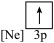 |
(5)
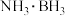 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(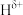 ),与B原子相连的H负电性(
),与B原子相连的H负电性(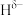 )。在H、B、N三种元素中,电负性由大到小的顺序是
)。在H、B、N三种元素中,电负性由大到小的顺序是
您最近一年使用:0次
名校
7 . 原子核外电子排布与族的关系
(1)将下列各主族元素的价电子排布式填入表中
(2)以第四周期副族元素为例,填写表格
(1)将下列各主族元素的价电子排布式填入表中
| 主族数 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 价电子排布式 |
| 副族元素 | Sc | Ti | V | Cr | Mn | Cu | Zn |
| 价电子排布式 |
您最近一年使用:0次
名校
8 . 回答下列问题。
I.酸雨是指 pH<5.6 的降水。
(1)下列气体中,与形成酸雨无关的是_________ 。
A.CO2 B.SO2 C.NOx
(2)下列变化属于“氮的固定”的是_________ (填字母)。
(3)汽车尾气中的CO、NOx在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出NO被CO还原的化学方程式:_________ 。
(4)从硫元素的化合价看,下列物质不具有氧化性的是___________。
Ⅱ.揭开浓硫酸的“神秘面纱”。
(5)在化工生产的过程中,一些试剂需要特殊的运输方式,比如具有强氧化性、强还原性、强腐蚀性等性质的试剂。通常情况下,下列物质可用铁制槽车装运的是_________。
I.酸雨是指 pH<5.6 的降水。
(1)下列气体中,与形成酸雨无关的是
A.CO2 B.SO2 C.NOx
(2)下列变化属于“氮的固定”的是_________ (填字母)。
| A.植物从土壤中吸收氮肥 | B.将空气中的氮气转变为氮的化合物 |
| C.硝酸和氨气反应生成氮肥 | D.大豆的根瘤菌将含氮的化合物转变为植物蛋白质 |
(4)从硫元素的化合价看,下列物质不具有氧化性的是___________。
| A.Na2S | B.S | C.SO2 | D.H2SO4 |
Ⅱ.揭开浓硫酸的“神秘面纱”。
(5)在化工生产的过程中,一些试剂需要特殊的运输方式,比如具有强氧化性、强还原性、强腐蚀性等性质的试剂。通常情况下,下列物质可用铁制槽车装运的是_________。
| A.浓盐酸 | B.浓硫酸 | C.稀硫酸 | D.浓氢氧化钠溶液 |
您最近一年使用:0次
名校
解题方法
9 . 向盛有下列溶液的试管中分别通入SO2气体:①NaOH溶液(滴有酚酞溶液);②紫色石蕊溶液;③品红溶液;④酸性高锰酸钾溶液;⑤硫化钠溶液。请回答下列问题:
(1)试管①中的现象是_______ ,发生反应的离子方程式为_______
(2)试管③中的现象是_______ 若将吸收SO2的溶液加热,现象是_______ 。
(3)上述实验,SO2表现出还原性的是_______ (填序号,下同),SO2表现出漂白性的是_______ 。
(1)试管①中的现象是
(2)试管③中的现象是
(3)上述实验,SO2表现出还原性的是
您最近一年使用:0次
名校
解题方法
10 . 在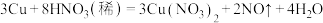 反应中,
反应中,
(1)用双线桥表示电子的转移情况_______
(2)_______ 是氧化剂;_______ 元素被氧化;氧化剂与还原剂的物质的量之比是_______ ;
(3)写出该反应的离子方程式_______ 。
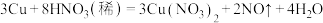 反应中,
反应中,(1)用双线桥表示电子的转移情况
(2)
(3)写出该反应的离子方程式
您最近一年使用:0次



