1 . 下表是元素周期表的一部分。表中所列字母分别代表一种元素。
回答下列问题:
(1)j在元素周期表中的位置是______ 。
(2)e、h、m形成的简单离子其半径由大到小的顺序为________ 。(填写离子符号)
(3)n与g形成的化合物为______ (填写化学式,下同),将该化合物进行焰色反应,火焰呈______ 色。
(4)k、1形成的最高价氧化物的水化物,酸性由强到弱的顺序为______ 。
(5)g的最高价氧化物对应的水化物与i的最高价氧化物对应的水化物反应的离子方程式为______ 。
(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
(实验操作)取已除去氧化膜且面积相等的镁条和铝条,分别投入2mL1mol/L盐酸中;
(实验现象)镁与酸反应比铝更剧烈;
(实验结论)①金属性:Mg_____ Al(选填“>”或“<”);
(查阅资料)原子半径(nm)Mg:0.160 Al:0.143;
(思考)②利用元素周期律对上述实验结论进行解释______ 。
| a | b | |||||||
| c | d | e | f | |||||
| g | h | i | j | k | l | m | ||
| n |
(1)j在元素周期表中的位置是
(2)e、h、m形成的简单离子其半径由大到小的顺序为
(3)n与g形成的化合物为
(4)k、1形成的最高价氧化物的水化物,酸性由强到弱的顺序为
(5)g的最高价氧化物对应的水化物与i的最高价氧化物对应的水化物反应的离子方程式为
(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
(实验操作)取已除去氧化膜且面积相等的镁条和铝条,分别投入2mL1mol/L盐酸中;
(实验现象)镁与酸反应比铝更剧烈;
(实验结论)①金属性:Mg
(查阅资料)原子半径(nm)Mg:0.160 Al:0.143;
(思考)②利用元素周期律对上述实验结论进行解释
您最近一年使用:0次
2022-01-14更新
|
785次组卷
|
4卷引用:湖南省怀化市2021-2022学年高一上学期期末考试化学试题
湖南省怀化市2021-2022学年高一上学期期末考试化学试题(已下线)第四章 物质结构 元素周期律(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)湖北省孝感市新高考联考协作体2022-2023学年高二上学期9月联考化学试题(已下线)【2023】【高一下】【其他】【杭高卷四-期中复习卷】【高中化学】【刘尼尼收集】
21-22高二·全国·单元测试
2 . 下图所示为元素周期表的大致框架:
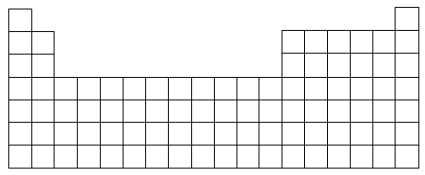
(1)在上图所示元素周期表中画出金属元素与非金属元素的分界线_______ 。
(2)鉴于NaH的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的_______ 族。
(3)现有甲、乙两种元素,甲元素原子核外3p能级上有5个电子,乙元素的焰色实验呈黄色。
①在上图所示的元素周期表中,将甲、乙两元素的元素符号填在元素周期表中的相应位置_______ 。
②甲元素与硫元素相比,非金属性较强的是_______ (填元素名称),写出可以验证该结论的一个化学方程式:_______ 。
(4)近年来“铊中毒”事件屡屡发生,铊再次成为公众关注的焦点。铊元素的相关信息如下图所示。下列叙述不正确的是_______ (填字母)。

A.铊元素在元素周期表中的位置是第六周期第ⅡA族
B.铊原子的中子数为204-81=123
C.6s26p1表示铊原子有6个电子层,最外电子层上有3个电子
D.铊元素的金属性比铝元素的强
E.铊元素是p区元素

(1)在上图所示元素周期表中画出金属元素与非金属元素的分界线
(2)鉴于NaH的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的
(3)现有甲、乙两种元素,甲元素原子核外3p能级上有5个电子,乙元素的焰色实验呈黄色。
①在上图所示的元素周期表中,将甲、乙两元素的元素符号填在元素周期表中的相应位置
②甲元素与硫元素相比,非金属性较强的是
(4)近年来“铊中毒”事件屡屡发生,铊再次成为公众关注的焦点。铊元素的相关信息如下图所示。下列叙述不正确的是

A.铊元素在元素周期表中的位置是第六周期第ⅡA族
B.铊原子的中子数为204-81=123
C.6s26p1表示铊原子有6个电子层,最外电子层上有3个电子
D.铊元素的金属性比铝元素的强
E.铊元素是p区元素
您最近一年使用:0次
21-22高二·全国·课时练习
3 . 原子结构与元素周期表存在内在联系,按要求回答下列问题:
(1)根据元素在周期表中的位置,写出元素基态原子的价电子排布式。
①第四周期第ⅥB族_______ ;
②第五周期第ⅠB族_______ ;
③第五周期第ⅣA族_______ ;
④第六周期第ⅡA族_______ 。
(2)根据元素电子排布可以确定元素在周期表中的位置。
①具有(n-1)d10ns2电子排布的元素位于周期表中的第_______ 族。
②已知某元素+2价离子的核外电子排布式为1s22s22p63s23p63d3。该元素位于元素周期表_______ (填序号)。
A.第二周期第ⅡB族
B.第四周期第ⅡA族
C.第四周期第ⅤB族
D.第五周期第ⅡB族
③某元素原子的核电荷数为33,则其原子的价电子排布式为_______ ,其位于元素周期表中的_______ ,属于_______ 区的元素。
(3)根据元素核外电子排布可以推知元素的性质。
①被誉为“21世纪金属”的钛(Ti)元素,基态原子价电子轨道表示式为_______ ,Ti元素形成的化合物中,Ti呈现的最高价态为_______ 价。
②日常生活中广泛应用的不锈钢,在其生产过程中添加了某种元素,该元素基态原子的价电子排布式为3d54s1,该元素的名称是_______ 。
(1)根据元素在周期表中的位置,写出元素基态原子的价电子排布式。
①第四周期第ⅥB族
②第五周期第ⅠB族
③第五周期第ⅣA族
④第六周期第ⅡA族
(2)根据元素电子排布可以确定元素在周期表中的位置。
①具有(n-1)d10ns2电子排布的元素位于周期表中的第
②已知某元素+2价离子的核外电子排布式为1s22s22p63s23p63d3。该元素位于元素周期表
A.第二周期第ⅡB族
B.第四周期第ⅡA族
C.第四周期第ⅤB族
D.第五周期第ⅡB族
③某元素原子的核电荷数为33,则其原子的价电子排布式为
(3)根据元素核外电子排布可以推知元素的性质。
①被誉为“21世纪金属”的钛(Ti)元素,基态原子价电子轨道表示式为
②日常生活中广泛应用的不锈钢,在其生产过程中添加了某种元素,该元素基态原子的价电子排布式为3d54s1,该元素的名称是
您最近一年使用:0次
21-22高一上·全国·课前预习
解题方法
4 . 门捷列夫在研究元素周期表时,科学地预言了11种尚未发现的元素,为它们在周期表中留下了空位。例如:他认为铝的下方有一个与铝类似的元素“类铝”,并预测了它的性质。1875年,法国化学家布瓦博德朗发现了这种元素,将它命名为“镓”,镓的性质与门捷列夫预测的一样。门捷列夫还预测在硅和锡之间存在一种元素“类硅”,15年后该元素被德国化学家文克勒发现,为了纪念他的祖国,将其命名为“锗”。
2016年国际纯粹与应用化学联合会(IUPAC)正式宣布,元素周期表中将加入4种新元素,原子序数分别为113、115、117和118.这可是件大事,因为这四种元素都是在实验室合成的,放射性强,还特别重。也因此而补齐了元素周期表的第七行。他们的发现也为科学家在未来合成更重要、更有实用价值的元素提供了可能。
问题:元素周期表给科学工作者发现元素提供了哪些依据_____ ?元素周期表中元素的位置和性质之间存在着怎样的内在联系_____ ?
2016年国际纯粹与应用化学联合会(IUPAC)正式宣布,元素周期表中将加入4种新元素,原子序数分别为113、115、117和118.这可是件大事,因为这四种元素都是在实验室合成的,放射性强,还特别重。也因此而补齐了元素周期表的第七行。他们的发现也为科学家在未来合成更重要、更有实用价值的元素提供了可能。
问题:元素周期表给科学工作者发现元素提供了哪些依据
您最近一年使用:0次
21-22高一上·全国·课前预习
5 . 随着化学科学的不断发展,元素周期表中为未知元素留下的空位先后被填满,周期表的形式也变得更加完美。请认真观察教材最后面的元素周期表,并结合初中所学的有关知识,回答下列问题。
(1)问题一:元素周期表中共有_____ 种底色?分别代表_____ ?分布有什么特点_____ ?周期表中有些元素用红框圈了起来,这些元素是哪类元素_____ ?
(2)问题二:元素周期表中共有_____ 行?_____ 列?周期表中一个横行叫做_____ ?每一行各有_____ 种元素?周期表中一个纵列叫做_____ ?用什么符号表示的_____ ?
(1)问题一:元素周期表中共有
(2)问题二:元素周期表中共有
您最近一年使用:0次
21-22高一上·全国·课前预习
解题方法
6 . 某年,瑞典的化学家阿尔费德森在分析一种矿物时发现,得出的已知成分只有96%,那么其余的4%到哪儿去了呢?他经过反复试验,确信一定是矿物中含有一种至今还不知道的元素。因这种元素是在名叫透锂长石的矿物中发现的,他就取名为“锂”(希腊文“岩石”之意)。不久,阿尔费德森又在其它矿物中发现了这种元素。另一名瑞典化学家贝采尼乌斯也在卡尔斯温泉和捷克的马里安温泉的矿泉水中发生了锂。
(1)问题一:在元素周期表中,锂处于什么位置________ ?
(2)问题二:由Na的性质预测Li可能的化学性质_________ ?
(1)问题一:在元素周期表中,锂处于什么位置
(2)问题二:由Na的性质预测Li可能的化学性质
您最近一年使用:0次
7 . 1907年1月27日,俄国首都圣彼得堡寒风凛冽,太阳黯淡无光,寒暑表上的水银柱降到零下20多度,街上到处点着蒙有黑纱的灯笼,显出一派悲哀的气氛。几万人的送葬队伍在街上缓缓移动着,在队伍最前头,既不是花圈,也不是遗像,而是由十几个青年学生扛着的一块大木牌,上面画着好多方格,方格里写着“C”“O”“Fe”“Zn”等元素符号。原来,逝者是著名的俄国化学家门捷列夫,木牌上画着好多方格的表是化学元素周期表——门捷列夫对化学的主要贡献。1869年门捷列夫根据当时已发现的60多种元素制出了第一张元素周期表,下图是门捷列夫最初绘制的元素周期表。

(1)问题一:你能看出门捷列夫的元素周期表是按照什么顺序排列的吗_______ ?
(2)问题二:现行元素周期表是按什么原则编排的_________ ?

(1)问题一:你能看出门捷列夫的元素周期表是按照什么顺序排列的吗
(2)问题二:现行元素周期表是按什么原则编排的
您最近一年使用:0次
8 . 在研究原子核外电子排布与元素周期表的关系时,人们发现价电子排布相似的元素集中在一起,据此,人们将元素周期表分为五个区,并以最后填入电子的轨道能级符号作为该区的符号,如图所示。
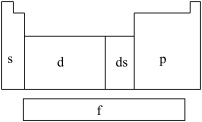
(1)在s区中,族序数最大、原子序数最小的元素原子的价电子的电子云形状为___________ 。
(2)在d区中,族序数最大、原子序数最小的元素,常见离子的电子排布式为___________ ,其中较稳定的是___________ 。
(3)在ds区中,族序数最大、原子序数最小的元素,原子的价电子排布式为___________ 。
(4)在p区中,第二周期ⅤA族元素原子的价电子排布图为___________ 。
(5)当今常用于核能开发的元素是铀和钚,它们在___________ 区中。

(1)在s区中,族序数最大、原子序数最小的元素原子的价电子的电子云形状为
(2)在d区中,族序数最大、原子序数最小的元素,常见离子的电子排布式为
(3)在ds区中,族序数最大、原子序数最小的元素,原子的价电子排布式为
(4)在p区中,第二周期ⅤA族元素原子的价电子排布图为
(5)当今常用于核能开发的元素是铀和钚,它们在
您最近一年使用:0次
2021-12-04更新
|
555次组卷
|
9卷引用:同步君 选修3 第一章 第二节 原子结构与元素周期表
(已下线)同步君 选修3 第一章 第二节 原子结构与元素周期表高中化学人教版 选修三 第1章 原子结构与性质 原子结构与元素周期表山东省济宁市实验中学2018-2019学年高二上学期第二次月考化学试题(人教版2019)选择性必修2 第一章 原子结构与性质 第二节 原子结构与元素的性质(已下线)第30讲 原子结构与性质(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)1.2.1 原子结构与元素周期表(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)1.2.1 原子结构与元素周期表-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)专题2 原子结构与元素性质 第二单元 元素性质的递变规律 第1课时 原子核外电子排布的周期性2.2.1原子核外电子排布的周期性 课后
9 . 下列各元素是主族元素还是副族元素____ ?位于周期表中的第几周期和哪个族____ ?属于哪个区____ ?
(1)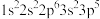 (2)
(2)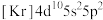 (3)
(3)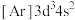 (4)
(4)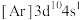 (5)
(5)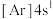
(1)
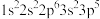 (2)
(2)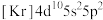 (3)
(3)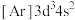 (4)
(4)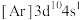 (5)
(5)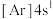
您最近一年使用:0次
解题方法
10 . 请完成下列空白:
铁元素位于元素周期表的第___________ 周期第___________ 族,属于___________ 区。
| 表示方法 |  |  |
| 原子(或离子)结构示意图 | ||
| 电子排布式 | ||
| 价电子轨道表示式 |
您最近一年使用:0次



