1 . 分析如下操作对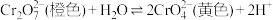 平衡影响的实验,说法不正确的是
平衡影响的实验,说法不正确的是

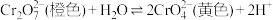 平衡影响的实验,说法不正确的是
平衡影响的实验,说法不正确的是
| A.试管a中溶液橙色变浅至黄色,说明平衡向正向移动 |
B.试管b中溶液橙色变深,说明增大 平衡向逆向移动 平衡向逆向移动 |
| C.该实验反应属于非氧化还原反应 |
| D.元素Cr属于主族元素 |
您最近一年使用:0次
名校
2 . 碲(Te)是52号元素,位于周期表中VIA族,处于金属区与非金属区的交界线上。下列叙述错误的是
| A.碲的单质具有半导体的性能 |
| B.碲化氢(H2Te)比H2S更稳定 |
| C.碲可在空气中燃烧生成二氧化碲(TeO2) |
| D.H2TeO4的酸性比H2SO4弱 |
您最近一年使用:0次
2022-11-04更新
|
508次组卷
|
4卷引用:河南省南召现代中学2021-2022学年高一下学期开学检测化学试题
河南省南召现代中学2021-2022学年高一下学期开学检测化学试题(已下线)物质结构 元素周期表——进阶学习广东省梅州市2022-2023学年高一上学期1月期末化学试题(已下线)【定心卷】4.2.2 元素周期表和元素周期律的应用随堂练习-人教版2023-2024学年必修第一册
22-23高一上·全国·课时练习
解题方法
3 . 已知短周期主族元素X、Y、Z、W的原子序数依次增大,Y在周期表中的周期数等于其族的序数,其在周期表的相对位置如下图所示。
下列说法正确的是
| X | ||||
| Y | Z | W |
| A.W元素的原子半径,在同周期主族元素中是最小的 |
| B.X元素原子的最高价为+6价 |
| C.Z的原子序数是X的3倍 |
| D.Y的氢氧化物化学式为Y(OH)2 |
您最近一年使用:0次
名校
解题方法
4 . 已知元素周期表中共有18纵行。如图所示实线表示元周期表的边界,按电子排布,可把元素周期表划分为s区、p区、d区、ds等,除ds区外,其他区的名称均按构造原理最后填入电子的能级符号来命名。
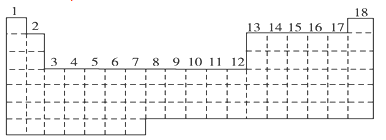
(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并标记分区_____ 。
(2)有的同学受这种划分的启示,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在___________ 区。
(3)请在元素周期表中标出4s轨道半充满的元素(用元素符号表示)_____ 。
(4)请利用电子排布的相关知识解释Fe3+比Fe2+稳定的原因:___________ 。
(5)随着科学技术的发展,不断有新的元素被发现。现在第七周期已经排满,则元素周期表共可以排布___________ 种元素。

(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并标记分区
(2)有的同学受这种划分的启示,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在
(3)请在元素周期表中标出4s轨道半充满的元素(用元素符号表示)
(4)请利用电子排布的相关知识解释Fe3+比Fe2+稳定的原因:
(5)随着科学技术的发展,不断有新的元素被发现。现在第七周期已经排满,则元素周期表共可以排布
您最近一年使用:0次
2022-10-20更新
|
158次组卷
|
2卷引用:河北省石家庄市第23中学2022-2023学年高二上学期第一次月考化学试题
名校
5 . X、Y、Z、W是原子序数依次增大的短周期不同主族元素,X的2p轨道有两个未成对电子,Y元素原子半径在同周期中最大,X与Y最外层电子数之和与Z的最外层电子数相等,W元素单质常温下是淡黄色固体。下列说法正确的是
| A.第一电离能:Z>W>Y | B.Y在元素周期表中位于p区 |
| C.X、Z、W形成的单质均属于分子晶体 | D.最高价含氧酸的酸性:Z>W |
您最近一年使用:0次
2022-10-20更新
|
586次组卷
|
5卷引用:广东省华南师范大学附属中学2023届高三上学期第一次月考化学试题
解题方法
6 . 如图是元素周期表的一部分,回答下列问题:
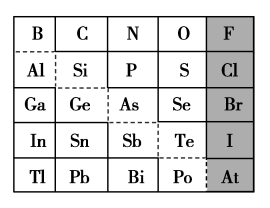
(1)元素Ga在元素周期表中的位置为:第_______ 周期第_______ 族。
(2)Sn的最高正价为_______ ,Cl的最高价氧化物对应的水化物的化学式为_______ ,Bi的最高价氧化物的化学式为_______ 。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是_______ (填元素符号)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4_______ H2SeO4(填“>”或“<”下同)。
③氢化物的还原性:H2O_______ H2S。

(1)元素Ga在元素周期表中的位置为:第
(2)Sn的最高正价为
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③氢化物的还原性:H2O
您最近一年使用:0次
名校
7 . 科学家成功合成了一种拥有117个质子的新元素。科学家用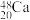 轰击
轰击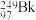 ,生成了6个拥有117个质子的新原子,其中的5个原子有176个中子,1个原子有177个中子。下列有关说法正确的是
,生成了6个拥有117个质子的新原子,其中的5个原子有176个中子,1个原子有177个中子。下列有关说法正确的是
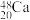 轰击
轰击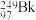 ,生成了6个拥有117个质子的新原子,其中的5个原子有176个中子,1个原子有177个中子。下列有关说法正确的是
,生成了6个拥有117个质子的新原子,其中的5个原子有176个中子,1个原子有177个中子。下列有关说法正确的是| A.第117号元素是副族元素 | B.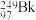 的质量数为97 的质量数为97 |
C.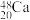 的中子数为48 的中子数为48 | D.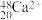 的中子数比核外电子数多10 的中子数比核外电子数多10 |
您最近一年使用:0次
8 . 下列说法正确的是
| A.s电子的形状为球形 | B.单质气体分子均为非极性分子 |
| C.Fe 和Zn位于元素周期表不同区 | D.3p2 表示3p能级有两个轨道 |
您最近一年使用:0次
9 . 在1-18号元素中,最外层电子数是其电子层数3倍的元素共有
| A.1种 | B.2种 | C.3种 | D.4种 |
您最近一年使用:0次
解题方法
10 . 下表是元素周期表的一部分,请回答:
(1)钠元素在元素周期表中的位置是___________ ;
(2)N、O、F三种元素中,非金属性最强的是___________ (填元素符号);
(3)由上表中两种元素组成的化合物是光导纤维的主要原料,该化合物的化学式为___________ ;
(4)碘与氯是同主族元素。下面关于碘的推断错误的是___________ (选填字母);
a.常温下,碘单质为气态 b.最高正化合价为+7 c.Cl2通入淀粉KI溶液中出现蓝色
(5)氮的氢化物和氯的氢化物反应生成一种铵盐,常用作氮肥,该反应的化学方程式为___________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ||||||||
| 2 | N | O | F | |||||
| 3 | Na | Si | Cl |
(1)钠元素在元素周期表中的位置是
(2)N、O、F三种元素中,非金属性最强的是
(3)由上表中两种元素组成的化合物是光导纤维的主要原料,该化合物的化学式为
(4)碘与氯是同主族元素。下面关于碘的推断错误的是
a.常温下,碘单质为气态 b.最高正化合价为+7 c.Cl2通入淀粉KI溶液中出现蓝色
(5)氮的氢化物和氯的氢化物反应生成一种铵盐,常用作氮肥,该反应的化学方程式为
您最近一年使用:0次



