名校
解题方法
1 . 硫和硒(34Se)在元素周期表中位于同一主族,均是生产生活中重要的非金属元素。
I.生成SO2并检验性质:点燃酒精灯,试管ⅰ中有白雾生成,铜丝表面产生气泡;试管ⅱ中溶液红色褪去,一段时间后,将铜丝抽离硫酸并停止加热。
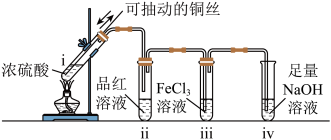
(1)i中发生反应的化学反应方程式为___________ 。
(2)ii中现象说明SO2具有___________ 作用。
(3)SO2能使溴水褪色,说明SO2具有的化学性质是___________ ,写出发生反应的离子方程式___________ 。
(4)将SO2通入FeCl3溶液中,下列实验事实能够证实FeCl3和SO2一定发生了反应的是___________ (填字母)。
a.加入酸性高锰酸钾,高锰酸钾褪色
b.取反应后的溶液少许,加入BaCl2溶液,产生白色沉淀
c.取反应后的溶液,加入Ba(OH)2溶液,产生沉淀,加入足量盐酸后,沉淀部分溶解。
II.以工业硒为原料制备高纯硒时的主要物质转化如图。
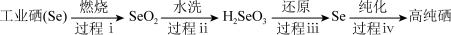
(5)下列说法不正确的是___________ (填字母序号)。
a.稳定性:H2Se>H2S b.过程ⅰ中硒被氧化
c.SeO2属于酸性氧化物 d.酸性:H2SeO4>H2SO4
(6)过程ⅲ中使用的还原剂为N2H4·nH2O,对应产物是N2。理论上,过程ⅰ消耗的O2与过程iii消耗的N2H4·nH2O的物质的量之比为___________ (工业硒中杂质与O2的反应可忽略)。
(7)SeO2易溶于水得到H2SeO3溶液,向溶液中通入HI气体后,再加入淀粉溶液,溶液变蓝色,同时生成Se沉淀,写出反应的化学方程式___________ 。
I.生成SO2并检验性质:点燃酒精灯,试管ⅰ中有白雾生成,铜丝表面产生气泡;试管ⅱ中溶液红色褪去,一段时间后,将铜丝抽离硫酸并停止加热。

(1)i中发生反应的化学反应方程式为
(2)ii中现象说明SO2具有
(3)SO2能使溴水褪色,说明SO2具有的化学性质是
(4)将SO2通入FeCl3溶液中,下列实验事实能够证实FeCl3和SO2一定发生了反应的是
a.加入酸性高锰酸钾,高锰酸钾褪色
b.取反应后的溶液少许,加入BaCl2溶液,产生白色沉淀
c.取反应后的溶液,加入Ba(OH)2溶液,产生沉淀,加入足量盐酸后,沉淀部分溶解。
II.以工业硒为原料制备高纯硒时的主要物质转化如图。
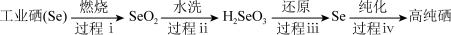
(5)下列说法不正确的是
a.稳定性:H2Se>H2S b.过程ⅰ中硒被氧化
c.SeO2属于酸性氧化物 d.酸性:H2SeO4>H2SO4
(6)过程ⅲ中使用的还原剂为N2H4·nH2O,对应产物是N2。理论上,过程ⅰ消耗的O2与过程iii消耗的N2H4·nH2O的物质的量之比为
(7)SeO2易溶于水得到H2SeO3溶液,向溶液中通入HI气体后,再加入淀粉溶液,溶液变蓝色,同时生成Se沉淀,写出反应的化学方程式
您最近一年使用:0次
名校
2 . 为研究同主族元素性质的递变规律,某小组以第VIIA元素为例用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。

已知: 的氧化性大于
的氧化性大于
(1)仪器X的名称为___________ ,A中反应的离子方程式___________ 。
(2)探究卤素单质氧化性的相对强弱,将实验现象填写在下表对应的空格里:
(3)操作步骤III的实验目的是___________ 。
(4)结合元素周期律解释氯、溴、碘单质的氧化性逐渐减小的原因:___________ 。
(5)实验中若氯气的通入量过多,淀粉碘化钾试纸会逐渐褪色,可能的原因____ 。

已知:
 的氧化性大于
的氧化性大于
(1)仪器X的名称为
(2)探究卤素单质氧化性的相对强弱,将实验现象填写在下表对应的空格里:
| 操作步骤 | 实验现象 |
| I.打开弹簧夹、活塞a,滴加浓盐酸。 II.当B和C中分液漏斗中的溶液都变为黄色时,夹紧弹簀夹。 | 湿润的淀粉碘化钾试纸 |
| III.当B中溶液由黄色变为棕色时,关闭活塞a。 IV.打开活塞b,将少量溶液滴入C中,关闭活塞b,取下C振荡。 | 试管C中的现象为 |
(4)结合元素周期律解释氯、溴、碘单质的氧化性逐渐减小的原因:
(5)实验中若氯气的通入量过多,淀粉碘化钾试纸会逐渐褪色,可能的原因
您最近一年使用:0次
2022-05-10更新
|
380次组卷
|
4卷引用:安徽省亳州市第二完全中学2022-2023学年高一下学期期中考试化学试题



