1 . 下表中"方法导引”与“示例"对应关系不正确的是
| 选项 | 方法导引 | 示例 |
| A | 分类 | 实验室中制取气体装置的连接顺序一般为:发生装置 除杂装置 除杂装置 收集装置 收集装置 尾气处理装置 尾气处理装置 |
| B | 预测 | 钠、钾能与水反应,铷与钠、钾都属于IA族元素,则可预测铷也能与水反应 |
| C | 变量控制 | 探究催化剂对化学反应速率的影响时,需要控制温度、浓度和他影响因素保持不变 |
| D | 认识有机化合物的一般思路 | 先分析有机物的碳骨架和官能团,再认识它的类别、性质和用途 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 周期表中VIA族元素及其化合物应用广泛。 、
、 、
、 是氧元素的3种核素,可以形成多种重要的化合物。亚硫酰氯
是氧元素的3种核素,可以形成多种重要的化合物。亚硫酰氯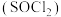 为黄色液体,其结构式为(
为黄色液体,其结构式为(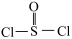 ),遇水发生水解。工业上可电解H2SO4与
),遇水发生水解。工业上可电解H2SO4与 混合溶液制备过二硫酸铵
混合溶液制备过二硫酸铵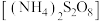 ,过二硫酸铵与双氧水中都含有过氧键(-O-O-)。硝化法制硫酸的主要反应为:
,过二硫酸铵与双氧水中都含有过氧键(-O-O-)。硝化法制硫酸的主要反应为:
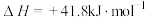 。SO2和SO3都是酸性氧化物,是制备硫酸的中间产物。下列物质结构与性质或物质性质与用途具有对应关系的是
。SO2和SO3都是酸性氧化物,是制备硫酸的中间产物。下列物质结构与性质或物质性质与用途具有对应关系的是
 、
、 、
、 是氧元素的3种核素,可以形成多种重要的化合物。亚硫酰氯
是氧元素的3种核素,可以形成多种重要的化合物。亚硫酰氯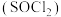 为黄色液体,其结构式为(
为黄色液体,其结构式为(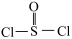 ),遇水发生水解。工业上可电解H2SO4与
),遇水发生水解。工业上可电解H2SO4与 混合溶液制备过二硫酸铵
混合溶液制备过二硫酸铵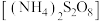 ,过二硫酸铵与双氧水中都含有过氧键(-O-O-)。硝化法制硫酸的主要反应为:
,过二硫酸铵与双氧水中都含有过氧键(-O-O-)。硝化法制硫酸的主要反应为:
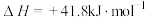 。SO2和SO3都是酸性氧化物,是制备硫酸的中间产物。下列物质结构与性质或物质性质与用途具有对应关系的是
。SO2和SO3都是酸性氧化物,是制备硫酸的中间产物。下列物质结构与性质或物质性质与用途具有对应关系的是| A.SO2具有还原性,可用于漂白纸浆 |
B. 中S为+6价, 中S为+6价, 具有较强的氧化性 具有较强的氧化性 |
| C.浓硫酸具有脱水性,可用于干燥氯气 |
D.H-O的键能强于H-S, 的热稳定性比的 的热稳定性比的 高 高 |
您最近一年使用:0次
名校
3 . 下列各图表示物质的某种性质与核电荷数的关系(Z为核电荷数,从第二周期开始,γ为元素的有关性质),下列选项中的对应关系不正确的是
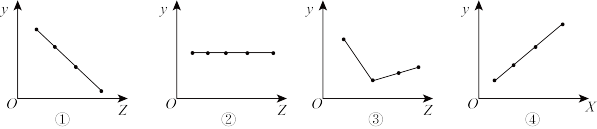

| A.图①可表示碱金属单质的熔点大小关系 |
| B.图②可表示ⅥA族元素的价电子数关系 |
| C.图③可表示ⅣA族元素的简单氢化物的沸点高低关系 |
| D.图④可表示ⅦA族元素的简单氢化物酸性大小关系 |
您最近一年使用:0次
4 . 元素周期表被认为是“科学共同的语言”,它的发现使化学学习和研究变得有规律可循。其简洁有序的背后,是众多科学家艰苦奋斗的结果。下图是元素周期表的一部分,请按要求回答下列问题:

(1)317年左右,东晋炼丹家葛洪在炼丹时分离出了砷。砷的原子结构示意图为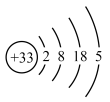 ,砷在周期表中的位置是
,砷在周期表中的位置是___________ 。我国“天宫”空间站的核心舱“天和”选择了高效柔性砷化镓(GaAs)薄膜太阳能电池来供电。原子半径:Ga___________ As(填“>”或“<”)。
(2)1787年,法国化学家拉瓦锡首次发现硅存在于岩石中。硅元素位于元素周期表金属与非金属的分界处,请写出硅单质的一种用途___________ 。
(3)1817年瑞典化学家贝采利乌斯发现硒元素。硫化硒(SeS)可用于治疗脂溢性皮炎。硫元素和硒元素简单气态氢化物热稳定性较强的为___________ (填化学式)。
(4)1825年,丹麦化学家奥斯特首次分离出了铝的单质。铝是地壳中含量最高的金属元素,但铝的利用却比铜和铁晚得多,可能的原因是___________ 。
(5)目前,世界上还有许多科学家为发现新元素孜孜不倦地努力着。可能存在的第119号元素,有人称“类钫”,位于元素周期表第八周期ⅠA族,有关“类钫”的预测说法正确的是
(6)小赵同学在研究元素周期表时发现,碳元素有“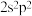 ”这一信息,观察元素周期表后,寻找规律,推测某元素“
”这一信息,观察元素周期表后,寻找规律,推测某元素“ ”中
”中 可能的含义是
可能的含义是___________ 。

(1)317年左右,东晋炼丹家葛洪在炼丹时分离出了砷。砷的原子结构示意图为
 ,砷在周期表中的位置是
,砷在周期表中的位置是(2)1787年,法国化学家拉瓦锡首次发现硅存在于岩石中。硅元素位于元素周期表金属与非金属的分界处,请写出硅单质的一种用途
(3)1817年瑞典化学家贝采利乌斯发现硒元素。硫化硒(SeS)可用于治疗脂溢性皮炎。硫元素和硒元素简单气态氢化物热稳定性较强的为
(4)1825年,丹麦化学家奥斯特首次分离出了铝的单质。铝是地壳中含量最高的金属元素,但铝的利用却比铜和铁晚得多,可能的原因是
(5)目前,世界上还有许多科学家为发现新元素孜孜不倦地努力着。可能存在的第119号元素,有人称“类钫”,位于元素周期表第八周期ⅠA族,有关“类钫”的预测说法正确的是
| A.“类钫”在化合物中显+1价 |
| B.“类钫”单质具有强氧化性 |
| C.“类钫”最高价氧化物对应的水化物为弱碱 |
| D.“类钫”单质能与冷水剧烈反应 |
(6)小赵同学在研究元素周期表时发现,碳元素有“
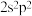 ”这一信息,观察元素周期表后,寻找规律,推测某元素“
”这一信息,观察元素周期表后,寻找规律,推测某元素“ ”中
”中 可能的含义是
可能的含义是
您最近一年使用:0次
5 . 随着原子序数的递增,A~M八种短周期元素的最高正价或最低负价与原子序数的关系如图所示。

(1)A、B、C三种元素的原子半径最大的是___________ (填元素名称),该元素的最高价氧化物的用途___________ 。(写一种即可)
(2)C、G两种元素对应的简单气态氢化物为___________ (填“离子”或“共价”)化合物,其中沸点较低的氢化物的结构式为___________ 。
(3)E、F、G、M三种元素的最高价氧化物对应水化物的酸性最强的是___________ (填化学式)。
(4)D元素的最高价氧化物对应的水化物含有的化学键为___________ ,工业上可用电解饱和DM的水溶液制备该物质,同时得到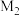 和另一种单质气体,该反应的化学方程式为
和另一种单质气体,该反应的化学方程式为___________ ;已知铷(Rb)的原子序数为37,关于铷的下列说法中不正确的是___________ (填字母序号)。
A.单质Rb与水反应比钠更剧烈
B.单质Rb的熔沸点比钠更高
C.RbOH的碱性比同浓度的NaOH更强
D.Rb是第五周期第ⅠA族元素

(1)A、B、C三种元素的原子半径最大的是
(2)C、G两种元素对应的简单气态氢化物为
(3)E、F、G、M三种元素的最高价氧化物对应水化物的酸性最强的是
(4)D元素的最高价氧化物对应的水化物含有的化学键为
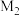 和另一种单质气体,该反应的化学方程式为
和另一种单质气体,该反应的化学方程式为A.单质Rb与水反应比钠更剧烈
B.单质Rb的熔沸点比钠更高
C.RbOH的碱性比同浓度的NaOH更强
D.Rb是第五周期第ⅠA族元素
您最近一年使用:0次
解题方法
6 . 门捷列夫在研究周期表时预言了包括“类铝”、“类硅”在内的11种元素。
(1)“类铝”在门捷列夫顶言4年后,被布瓦博德朗在一种矿石中发现,命名为镓( )。
)。
①镓与铝同主族,且位于铝的下一周期,则镓的原子结构示意图为_______ 。
②已知 难溶于水,为判断
难溶于水,为判断 是否为两性氢氧化物,设计实验时,需要选用的试剂有
是否为两性氢氧化物,设计实验时,需要选用的试剂有 溶液、
溶液、_______ 和_______ 。
③工业上冶炼金属镓通常采用的方法是_______ 。
④设计实验证明碱性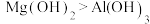 :
:_______ 。
(2)门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现,命名为锗( )。
)。
①硅和锗单质分别与 反应时,反应较难进行的是
反应时,反应较难进行的是_______ (填“硅”或“锗”)。
②根据锗在周期表中处于金属和非金属分界线附近,预测锗单质的一种用途是_______ 。
(3)某同学查找 、
、 、
、 三种元素在周期表的位置如图所示:
三种元素在周期表的位置如图所示:
 、
、 、
、 的
的 价氢氧化物碱性强弱顺序为
价氢氧化物碱性强弱顺序为_______ (用化学式表示)。
(1)“类铝”在门捷列夫顶言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(
 )。
)。①镓与铝同主族,且位于铝的下一周期,则镓的原子结构示意图为
②已知
 难溶于水,为判断
难溶于水,为判断 是否为两性氢氧化物,设计实验时,需要选用的试剂有
是否为两性氢氧化物,设计实验时,需要选用的试剂有 溶液、
溶液、③工业上冶炼金属镓通常采用的方法是
④设计实验证明碱性
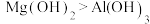 :
:(2)门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现,命名为锗(
 )。
)。①硅和锗单质分别与
 反应时,反应较难进行的是
反应时,反应较难进行的是②根据锗在周期表中处于金属和非金属分界线附近,预测锗单质的一种用途是
(3)某同学查找
 、
、 、
、 三种元素在周期表的位置如图所示:
三种元素在周期表的位置如图所示:| 周期 | ⅣA |
| 4 |  |
| 5 |  |
| 6 |  |
 、
、 、
、 的
的 价氢氧化物碱性强弱顺序为
价氢氧化物碱性强弱顺序为
您最近一年使用:0次
名校
解题方法
7 . 下表是元素周期表的一部分,回答下列问题:

(1) 在元素周期表中的位置为
在元素周期表中的位置为___________ 。 的原子结构示意图为
的原子结构示意图为___________ 。
(2) 三种元素的简单离子半径由大到小的顺序为
三种元素的简单离子半径由大到小的顺序为___________ (用离子符号表示)。将 气体通入
气体通入 溶液中,反应生成单质硒沉淀和
溶液中,反应生成单质硒沉淀和 ,写出反应的化学方程式:
,写出反应的化学方程式:___________ ;消耗标准状况下 时,可制得单质硒的质量为
时,可制得单质硒的质量为___________ 。
(3)写出 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:_______ , 的一种用途为
的一种用途为________ 。
(4)下列有关性质的比较,不能用元素周期律解释的是___________(填标号)。
(5) 是一种新型水处理剂,该化合物溶于水后的溶液具有漂白性,同时产生有刺激性气味的无色气体,写出该化合物与水反应的化学方程式:
是一种新型水处理剂,该化合物溶于水后的溶液具有漂白性,同时产生有刺激性气味的无色气体,写出该化合物与水反应的化学方程式:___________ 。

(1)
 在元素周期表中的位置为
在元素周期表中的位置为 的原子结构示意图为
的原子结构示意图为(2)
 三种元素的简单离子半径由大到小的顺序为
三种元素的简单离子半径由大到小的顺序为 气体通入
气体通入 溶液中,反应生成单质硒沉淀和
溶液中,反应生成单质硒沉淀和 ,写出反应的化学方程式:
,写出反应的化学方程式: 时,可制得单质硒的质量为
时,可制得单质硒的质量为(3)写出
 与
与 溶液反应的离子方程式:
溶液反应的离子方程式: 的一种用途为
的一种用途为(4)下列有关性质的比较,不能用元素周期律解释的是___________(填标号)。
A.酸性: | B.得电子能力: |
C.热稳定性: | D.热稳定性: |
 是一种新型水处理剂,该化合物溶于水后的溶液具有漂白性,同时产生有刺激性气味的无色气体,写出该化合物与水反应的化学方程式:
是一种新型水处理剂,该化合物溶于水后的溶液具有漂白性,同时产生有刺激性气味的无色气体,写出该化合物与水反应的化学方程式:
您最近一年使用:0次
2023-07-01更新
|
102次组卷
|
2卷引用:河南省南阳六校2022-2023学年高一下学期期末考试化学试题
解题方法
8 . 下列物质与其用途相符的是
①Cl2—作消毒剂 ②AgBr—制胶卷、感光纸 ③NaClO—漂白纺织物 ④加碘食盐—预防甲状腺肿大 ⑤淀粉—检验I2的存在
①Cl2—作消毒剂 ②AgBr—制胶卷、感光纸 ③NaClO—漂白纺织物 ④加碘食盐—预防甲状腺肿大 ⑤淀粉—检验I2的存在
| A.②③④⑤ | B.①②④⑤ | C.①③④⑤ | D.全部 |
您最近一年使用:0次
9 . B、Al、Ga等第ⅢA族元素,N、P、As等第VA族元素的单质及其化合物在生产、生活中有重要的用途。
(1)根据元素周期律的知识,下列说法不 正确的是_______ 。
①As与H2在低温时可剧烈化合为AsH3,AsH3电子式为: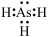
②酸性:HNO3>H3AsO4
③原子半径:N<As
④Al(OH)3为两性氢氧化物,既能溶于硝酸也能溶于氨水
(2)我国的“天宫”空间站的核心舱“天和”选择了高效柔性砷化镓(GaAs)薄膜太阳能电池来供电。镓元素在元素周期表中的位置是第四周期ⅢA族,镓的原子结构示意图为_______ 。
(3)把在空气中久置的铝片5.0g投入盛有50mL0.1mol·L-1盐酸的烧杯中,该铝片与盐酸反应,产生氢气的速率v(H2)与反应时间t的关系可用如图所示的坐标曲线来表示,下列推论错误的是_______ (填字母代号)。
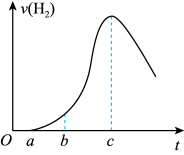
a.O→a不产生氢气是因为表面的氧化物隔离了铝和稀盐酸
b.b→c段产生氢气的速率增加较快的主要原因之一是温度升高
c.t=c时,反应处于平衡状态
d.t>c时,产生氢气的速率降低的主要原因是溶液中H+浓度下降
(4)雌黄(As2S3)和雄黄(As4S4)都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。在雌黄(As2S3)和雄黄(As4S4)中,S元素均为-2价,一定条件下,雌黄和雄黄的转化关系如图所示。
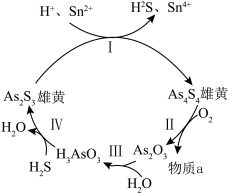
①以上转换关系中发生的Ⅰ、Ⅱ、Ⅲ、Ⅳ反应,属于氧化还原反应的是_______ 。(填字母)
②Ⅱ中若0.1molAs4S4反应转移2.8mole-,则消耗标况下O2的体积是_______ L,a物质是_______ 。
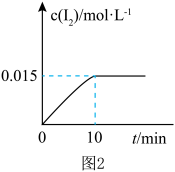
(5)砷酸钠(Na3AsO4)具有氧化性,298K时,在100mL烧杯中加入10mL0.1mol/LNa3AsO4溶液、20mL0.1mol/LKI溶液和20mL0.05mol/L硫酸溶液,发生下列反应:AsO (无色)+2I-+2H+⇌AsO
(无色)+2I-+2H+⇌AsO (无色)+I2(浅黄色)+H2O,测得溶液中c(I2)与时间(t)的关系如图2所示(溶液体积变化忽略不计)。下列情况表明上述可逆反应达到平衡状态的是
(无色)+I2(浅黄色)+H2O,测得溶液中c(I2)与时间(t)的关系如图2所示(溶液体积变化忽略不计)。下列情况表明上述可逆反应达到平衡状态的是_______ (填字母代号)。
a.溶液pH保持不变 b.c(AsO )+c(AsO
)+c(AsO )不再变化
)不再变化
c.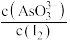 保持变化 d.c(I-)=0.07mol·L-1
保持变化 d.c(I-)=0.07mol·L-1
(1)根据元素周期律的知识,下列说法
①As与H2在低温时可剧烈化合为AsH3,AsH3电子式为:
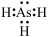
②酸性:HNO3>H3AsO4
③原子半径:N<As
④Al(OH)3为两性氢氧化物,既能溶于硝酸也能溶于氨水
(2)我国的“天宫”空间站的核心舱“天和”选择了高效柔性砷化镓(GaAs)薄膜太阳能电池来供电。镓元素在元素周期表中的位置是第四周期ⅢA族,镓的原子结构示意图为
(3)把在空气中久置的铝片5.0g投入盛有50mL0.1mol·L-1盐酸的烧杯中,该铝片与盐酸反应,产生氢气的速率v(H2)与反应时间t的关系可用如图所示的坐标曲线来表示,下列推论错误的是

a.O→a不产生氢气是因为表面的氧化物隔离了铝和稀盐酸
b.b→c段产生氢气的速率增加较快的主要原因之一是温度升高
c.t=c时,反应处于平衡状态
d.t>c时,产生氢气的速率降低的主要原因是溶液中H+浓度下降
(4)雌黄(As2S3)和雄黄(As4S4)都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。在雌黄(As2S3)和雄黄(As4S4)中,S元素均为-2价,一定条件下,雌黄和雄黄的转化关系如图所示。

①以上转换关系中发生的Ⅰ、Ⅱ、Ⅲ、Ⅳ反应,属于氧化还原反应的是
②Ⅱ中若0.1molAs4S4反应转移2.8mole-,则消耗标况下O2的体积是
(5)砷酸钠(Na3AsO4)具有氧化性,298K时,在100mL烧杯中加入10mL0.1mol/LNa3AsO4溶液、20mL0.1mol/LKI溶液和20mL0.05mol/L硫酸溶液,发生下列反应:AsO
 (无色)+2I-+2H+⇌AsO
(无色)+2I-+2H+⇌AsO (无色)+I2(浅黄色)+H2O,测得溶液中c(I2)与时间(t)的关系如图2所示(溶液体积变化忽略不计)。下列情况表明上述可逆反应达到平衡状态的是
(无色)+I2(浅黄色)+H2O,测得溶液中c(I2)与时间(t)的关系如图2所示(溶液体积变化忽略不计)。下列情况表明上述可逆反应达到平衡状态的是
a.溶液pH保持不变 b.c(AsO
 )+c(AsO
)+c(AsO )不再变化
)不再变化c.
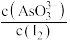 保持变化 d.c(I-)=0.07mol·L-1
保持变化 d.c(I-)=0.07mol·L-1
您最近一年使用:0次
名校
解题方法
10 . (1)二氯化二硫(S2Cl2)是一种琥珀色液体,是合成硫化染料的重要原料。
a.S2Cl2分子中所有原子都满足8电子稳定结构,写出它的电子式____________ ;
b.指出它分子内的键型_________ 。
(2)硒的原子序数为34,硒的单质及其化合物用途非常广泛。
a.硒在元素周期表中的位置是___________ 。
b.硒化铟是一种可应用于未来超算设备的新型半导体材料。已知铟(In)与铝同族且比铝多两个电子层。下列说法正确的是________ (填字母)。
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
a.S2Cl2分子中所有原子都满足8电子稳定结构,写出它的电子式
b.指出它分子内的键型
(2)硒的原子序数为34,硒的单质及其化合物用途非常广泛。
a.硒在元素周期表中的位置是
b.硒化铟是一种可应用于未来超算设备的新型半导体材料。已知铟(In)与铝同族且比铝多两个电子层。下列说法正确的是
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
您最近一年使用:0次
2020-07-13更新
|
133次组卷
|
2卷引用:上海市宜川中学2023-2024学年高三上学期9月月考化学试卷



