解题方法
1 .  为原子序数依次增大的短周期主族非金属元素.常温下,
为原子序数依次增大的短周期主族非金属元素.常温下,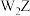 为一种常见的无色液体,X与Z的原子序数之和为¥的两倍,四种元素形成的一种化合物甲的结构如图所示.下列说法错误的是
为一种常见的无色液体,X与Z的原子序数之和为¥的两倍,四种元素形成的一种化合物甲的结构如图所示.下列说法错误的是
 为原子序数依次增大的短周期主族非金属元素.常温下,
为原子序数依次增大的短周期主族非金属元素.常温下,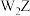 为一种常见的无色液体,X与Z的原子序数之和为¥的两倍,四种元素形成的一种化合物甲的结构如图所示.下列说法错误的是
为一种常见的无色液体,X与Z的原子序数之和为¥的两倍,四种元素形成的一种化合物甲的结构如图所示.下列说法错误的是
A.原子半径: | B.甲与熟石灰混合研磨可以生成有刺激性气味的气体 |
C.最简单氢化物的稳定性: | D.最高价氧化物对应水化物的酸性: |
您最近一年使用:0次
名校
2 . 2019年是元素周期表诞生150周年,元素周期表在学习、研究和生产实践中有很重要的作用。①~⑦七种元素在元素周期表中的位置如表:
请回答下列问题:
(1)⑦的元素符号是______ ,其在元素周期表中的位置是______ 。
(2)元素①④⑤原子半径由大到小的顺序是______ ,由这三种元素组成的化合物是一种强碱,其化学式是______ ,电子式是______ ,该化合物中含有的化学键______ 。
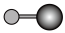
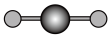
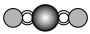
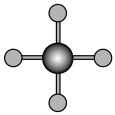
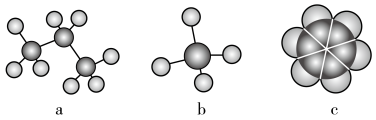
(3)由①②形成的最简单化合物的分子模型是______ (填序号)。______ 。
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
1 | ① | ||||||
2 | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ |
(1)⑦的元素符号是
(2)元素①④⑤原子半径由大到小的顺序是
(3)由①②形成的最简单化合物的分子模型是
您最近一年使用:0次
名校
3 . X、Y、Z、W为四种短周期主族元素,它们在周期表中的位置如图所示。Z元素原子的最外层电子数与电子层数相同。下列说法中不正确 的是
X | Y | ||
Z | W |
| A.X元素位于第二周期第ⅤA族 | B.原子半径由大到小的顺序为: |
C.Z单质既能与盐酸又能与 溶液反应 溶液反应 | D.W单质可作半导体材料 |
您最近一年使用:0次
2024-06-05更新
|
171次组卷
|
2卷引用:北京理工大学附属中学2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
4 . 短周期元素X、Y、Z、W、Q在元素周期表中的位置如下表所示,一种新型人工合成固定X元素的原理如下图所示。
下列说法正确的是

X | Y | ||
Z | W | Q |
| A.原子半径:Z>W>Y>X |
| B.简单氢化物的稳定性:Y>W |
| C.Q元素氧化物的水化物的酸性比W的强 |
| D.上图总反应中X的单质置换出氧气,说明X的非金属性比氧强 |
您最近一年使用:0次
名校
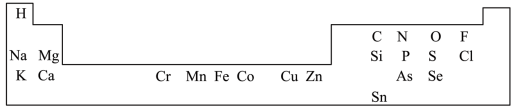
5 . 一些元素在周期表中的分布情况如图:___________ 。
(2)Na、Cl、K元素对应的简单离子半径由小到大的顺序___________ (用离子符号表示)。
(3)Sn的价电子数为___________ 。
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是___________(填字母)。
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________。
(6)用电子式表示 的形成过程
的形成过程___________ 。
(7)在下列物质中:① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦Ar⑧
⑦Ar⑧ (用物质前序号填空)。其中既存在极性键又存在非极性键的是
(用物质前序号填空)。其中既存在极性键又存在非极性键的是___________ ;既存在离子键又存在极性键的是___________ 。
(2)Na、Cl、K元素对应的简单离子半径由小到大的顺序
(3)Sn的价电子数为
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是___________(填字母)。
| A | B | C | D |
 |  |  |  |
|
|
|
|
| 直线形 | 直线形 | 直线形 | 平面正方形 |
| A.A | B.B | C.C | D.D |
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________。
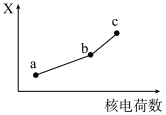
| A.若a、b、c表示ⅠA族金属元素,则X表示对应单质的密度 |
| B.若a、b、c表示ⅦA族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示ⅥA族元素,则X表示对应氢化物的稳定性 |
| D.若a、b、c表示第ⅡA族元素,则X表示最高价氧化物对应水化物的碱性 |
(6)用电子式表示
 的形成过程
的形成过程(7)在下列物质中:①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦Ar⑧
⑦Ar⑧ (用物质前序号填空)。其中既存在极性键又存在非极性键的是
(用物质前序号填空)。其中既存在极性键又存在非极性键的是
您最近一年使用:0次
名校
解题方法
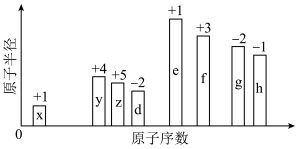
6 . 随着原子序数的递增,8种短周期元素(用英文字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示._____________ 。
(2)元素x分别与y、z、d形成的10电子气态分子中,热稳定性由强到弱的顺序为_____________ (填化学式).元素z、d、e、f形成的简单离子中半径最大的离子是_____________ (填离子符号)。
(3)将化合物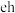 由固态加热至熔融态,吸收的能量主要用于断裂
由固态加热至熔融态,吸收的能量主要用于断裂_____________ 键(填“离子”或“共价”).x与d可形成多种共价分子,其中三原子共价分子的电子式为_____________ ;四原子共价分子的结构式为_____________ 。
(4)不能作为比较g与h的非金属性强弱的依据是____________。
(5)x和g的形成的二元化合物与h的单质发生反应的离子方程式为___________ 。
(2)元素x分别与y、z、d形成的10电子气态分子中,热稳定性由强到弱的顺序为
(3)将化合物
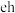 由固态加热至熔融态,吸收的能量主要用于断裂
由固态加热至熔融态,吸收的能量主要用于断裂(4)不能作为比较g与h的非金属性强弱的依据是____________。
| A.氢化物酸性h强于g | B.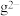 的还原性强于 的还原性强于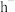 |
| C.与x单质反应,g单质比h单质更困难 | D.常温下g单质呈固态,h单质呈气态 |
(5)x和g的形成的二元化合物与h的单质发生反应的离子方程式为
您最近一年使用:0次
名校
解题方法
7 . 短周期主族元素W、X、Y、Z、Q原子序数依次增大,形成的化合物是一种重要的食品添加剂,结构如下图.Z核外最外层电子数与X核外电子总数相等.W的原子半径在周期表中最小.下列有关叙述正确的是
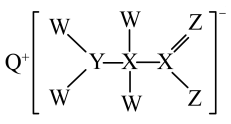
A.原子半径大小: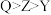 |
| B.该化合物中Y原子不满足8电子稳定结构 |
| C.Y元素对应的气态氢化物能与它的最高价含氧酸发生反应 |
| D.该化合物中,W、X、Y、Z、Q之间均为共价键 |
您最近一年使用:0次
8 . A、B、C、D、E是原子序数依次增大的短周期主族元素,它们在元素周期表中的相对位置如表,已知C的内层电子总数是最外层电子数的2倍。
(1)C在元素周期表中的位置为___________ 。
(2)A、B、C的最简单氢化物的稳定性由弱到强的顺序是___________ (填化学式);用电子式表示出A的最简单氢化物的形成过程:___________ 。
(3)C、D、E的简单离子半径由大到小的顺序是___________ (填离子符号),画出C的简单离子的结构示意图:___________ 。
(4)实验室制取 气体的离子方程式为
气体的离子方程式为___________ 。
(5)工业上,A的最简单气态氢化物可用来检测输送 气体的管道是否泄漏,发生反应的现象为
气体的管道是否泄漏,发生反应的现象为___________ ,写出反应的化学方程式:___________ 。
| A | B | |
| C | D | E |
(2)A、B、C的最简单氢化物的稳定性由弱到强的顺序是
(3)C、D、E的简单离子半径由大到小的顺序是
(4)实验室制取
 气体的离子方程式为
气体的离子方程式为(5)工业上,A的最简单气态氢化物可用来检测输送
 气体的管道是否泄漏,发生反应的现象为
气体的管道是否泄漏,发生反应的现象为
您最近一年使用:0次
名校
解题方法
9 . 短周期主族元素A、B、C、D的原子序数依次增大,A、B、D分别位于不同周期,且B和D是同主族,B的最外层电子数是内层的3倍,C是同周期原子半径最大的,下列说法正确的是
| A.A与B、D均可形成18电子分子 |
| B.B、C两种元素形成的化合物中只含离子键 |
| C.B的非金属性强于D,故简单气态氢化物的沸点水高于硫化氢 |
D.离子半径大小关系: |
您最近一年使用:0次
名校
10 . 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等。下列判断不正确的是
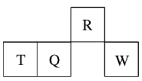
A.简单氢化物的热稳定性: |
B.最高价氧化物对应水化物的酸性: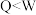 |
C.原子半径: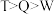 |
| D.含T的盐溶液一定能电离出T的阳离子 |
您最近一年使用:0次