名校
1 . Ⅰ.金属家(Ga)应用广泛,在半导体和光电材料、合金、磁性材料等领域都有重要应用。镓与铝是同主族元素,性质相似。
(1)铝在元素周期表中的位置是__________ 。
Ⅱ.GaAs是共价化合物,一种重要的半导体材料。As与Ga同周期,As与N同主族。
(2)下列事实不能用元素周期律解释的是_________ (填字母)。
a.碱性:Ga(OH)3>Al(OH)3
b.非金属性:As>Ga
c.酸性:H3AsO4>H3AsO3
(3)废弃含GaAs半导体材料可以用浓硝酸溶解GaAs,生成H3AsO4和Ga3+和NO2,写出该反应的化学方程式_____________________ 。
Ⅲ.A+、B2-、C-、D、E、F3+分别表示含10个电子的六种粒子。其中:
a.A+、B2-、F3+核外电子层结构相同
b.C-是由两种元素组成的
c.D是两种元素组成的四原子分子
d.E在常温下是无色液体
e.往含F3+的溶液中滴加含C-的溶液至过量,先有白色沉淀生成,后白色沉淀消失
(4)C-的电子式:_________ 。
(5)简单离子A+、B2-、F3+中,离子半径由大到小的顺序是_________ (填离子符号)。
(6)电子式表示A2B的形成过程__________________ 。
(7)含F3+的溶液中通入过量D,反应的离子方程式是__________________ 。
(8)A单质与E反应的生成的化合物中化学键的类型是_________ 。
(1)铝在元素周期表中的位置是
Ⅱ.GaAs是共价化合物,一种重要的半导体材料。As与Ga同周期,As与N同主族。
(2)下列事实不能用元素周期律解释的是
a.碱性:Ga(OH)3>Al(OH)3
b.非金属性:As>Ga
c.酸性:H3AsO4>H3AsO3
(3)废弃含GaAs半导体材料可以用浓硝酸溶解GaAs,生成H3AsO4和Ga3+和NO2,写出该反应的化学方程式
Ⅲ.A+、B2-、C-、D、E、F3+分别表示含10个电子的六种粒子。其中:
a.A+、B2-、F3+核外电子层结构相同
b.C-是由两种元素组成的
c.D是两种元素组成的四原子分子
d.E在常温下是无色液体
e.往含F3+的溶液中滴加含C-的溶液至过量,先有白色沉淀生成,后白色沉淀消失
(4)C-的电子式:
(5)简单离子A+、B2-、F3+中,离子半径由大到小的顺序是
(6)电子式表示A2B的形成过程
(7)含F3+的溶液中通入过量D,反应的离子方程式是
(8)A单质与E反应的生成的化合物中化学键的类型是
您最近一年使用:0次
名校
2 . X、Y、Z、W是原子序数依次增大的四种短周期主族元素.X、Z的最外层电子数均等于其周期序数,X是宇宙中含量最丰富的元素,Y是海水中含量最多的金属元素,W的最高正化合价与最低负化合价的代数和为6.下列说法错误的是
| A.W的氧化物对应的水化物一定是强电解质 |
B.简单离子半径: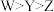 |
C. 是一种清洁能源 是一种清洁能源 |
| D.Y、Z、W的最高价氧化物对应的水化物之间能互相反应 |
您最近一年使用:0次
2024-03-28更新
|
154次组卷
|
2卷引用:河北省保定市部分高中2023-2024学年高一下学期开学化学试题
名校
解题方法
3 . 嫦娥五号带回1731克月壤,月壤中含有的六种元素Q、R、T、X、Y、Z,均为前20号元素,原子序数依次增大,最外层电子数之和为18,R、T、X三种元素的原子序数之和等于Y与Z两元素的原子序数之和。R、T、X同周期且原子序数相邻,Y、Z左右相邻,R与Z上下相邻,下列结论正确的是
| A.R的金属性比Y的金属性大 |
| B.Q与X组成化合物XQ2由固态转化为液态需要克服分子间作用力 |
| C.单质从酸或水中置换氢的能力:Y>Z>R>T |
| D.简单离子半径大小顺序:Y>Z>R>T>Q |
您最近一年使用:0次
名校
4 . 某种咪唑盐具有良好的导电性,其结构如下.X、Y、Z原子序数依次增大,均为短周期主族元素.下列说法正确的是


A.原子半径: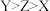 | B.分子的极性: |
C.简单氢化物的还原性: | D.该化合物具有良好的导电性,是因为它含有有机环状结构 |
您最近一年使用:0次
2024-03-18更新
|
238次组卷
|
3卷引用:河北省保定市部分高中2023-2024学年高三下学期开学化学试题
名校
5 .  为原子序数依次增大的前四周期元素,基态原子中,
为原子序数依次增大的前四周期元素,基态原子中, 为元素周期表中半径最小的原子,
为元素周期表中半径最小的原子, 原子最外层电子数为次外层电子数的三倍,
原子最外层电子数为次外层电子数的三倍, 原子的价电子排布为
原子的价电子排布为 形成的阳离子如图所示(狭长八面体结构),下列说法正确的是
形成的阳离子如图所示(狭长八面体结构),下列说法正确的是

 为原子序数依次增大的前四周期元素,基态原子中,
为原子序数依次增大的前四周期元素,基态原子中, 为元素周期表中半径最小的原子,
为元素周期表中半径最小的原子, 原子最外层电子数为次外层电子数的三倍,
原子最外层电子数为次外层电子数的三倍, 原子的价电子排布为
原子的价电子排布为 形成的阳离子如图所示(狭长八面体结构),下列说法正确的是
形成的阳离子如图所示(狭长八面体结构),下列说法正确的是
A.原子半径: |
B.气态氢化物的稳定性: |
C.加热时该离子首先失去的组分是 |
D.两种配体中的键角: |
您最近一年使用:0次
名校
解题方法
6 . 下表列出了①~⑨九种元素在周期表中的位置。

回答下列问题:
(1)①~⑨九种元素中,化学性质最不活泼的是___________ (填元素符号)。
(2)元素②的原子结构示意图是___________ ,元素②与⑨组成的化合物中化学键类型为___________ (填“离子键”或“共价键”)。
(3)元素②和③中原子半径较大的是___________ (填元素符号)。
(4)元素③和④中气态氢化物稳定性较强的是___________ (填化学式)。
(5)元素⑧和⑨的最高价氧化物对应的水化物中,酸性强的是___________ (填化学式)。

回答下列问题:
(1)①~⑨九种元素中,化学性质最不活泼的是
(2)元素②的原子结构示意图是
(3)元素②和③中原子半径较大的是
(4)元素③和④中气态氢化物稳定性较强的是
(5)元素⑧和⑨的最高价氧化物对应的水化物中,酸性强的是
您最近一年使用:0次
名校
解题方法
7 . 短周期主族元素W、X、Y、Z的原子序数依次增大,W的阴离子与锂离子具有相同的电子层结构,X的一种核素常用于考古断代,Y原子的最外层电子数是内层电子数的3倍,W、X、Y原子的最外层电子数总和等于Z的原子序数。下列推断错误的是
A.原子半径:  |
B.化合物  中既含离子键又含共价键 中既含离子键又含共价键 |
C.最简单气态氢化物的稳定性:  |
| D.由上述四种元素组成的化合物的水溶液可能呈碱性 |
您最近一年使用:0次
名校
解题方法
8 . 中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,并被采用为国际新标准。铟与铷(37Rb)同周期,下列说法错误的是
| A.In是第五周期第ⅢA族元素 | B.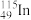 的中子数与电子数的差值为66 的中子数与电子数的差值为66 |
C.原子半径: | D.碱性: |
您最近一年使用:0次
名校
9 . X、Y、Z、M、Q、R皆为前20号元素,其原子半径与化合价的关系如图所示。下列说法正确的是
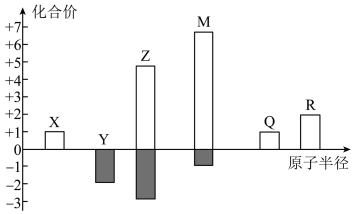

| A.简单离子半径:M>Y>Q |
| B.简单氢化物的稳定性:Z>Y |
| C.X、Y、Z组成的化合物只含有共价键 |
| D.Q、R的最高价氧化物对应的水化物可以发生反应 |
您最近一年使用:0次
名校
10 . 下表是元素周期表的一部分,a~k分别代表10种元素,请回答:
(1)元素a~k中,其简单氢化物最稳定的是_____ (填元素符号)。
(2)b的简单氢化物的结构式_____ 。
(3)c、d、e、f中形成的简单离子半径由大到小的顺序是_____ (填离子符号)。
(4)写出两种由c原子和e原子构成的化合物的电子式_____ 。
(5)元素h、i的最高价氧化物对应水化物中酸性较强的是_____ (填化学式)。
(6)写出84号元素在元素周期表中的位置_____ 。
(7)g的单质与e的最高价氧化物对应的水化物反应的化学方程式是_____ 。
(8)下列说法能证明金属性k强于f的是_____ (填序号)。
A.k的简单阳离子的氧化性更弱
B.k的氢氧化物水溶液的导电性更强
C.k的单质与水反应更剧烈
| a | ||||||||
| b | c | d | ||||||
| e | f | g | h | i | ||||
| k | …… | |||||||
(2)b的简单氢化物的结构式
(3)c、d、e、f中形成的简单离子半径由大到小的顺序是
(4)写出两种由c原子和e原子构成的化合物的电子式
(5)元素h、i的最高价氧化物对应水化物中酸性较强的是
(6)写出84号元素在元素周期表中的位置
(7)g的单质与e的最高价氧化物对应的水化物反应的化学方程式是
(8)下列说法能证明金属性k强于f的是
A.k的简单阳离子的氧化性更弱
B.k的氢氧化物水溶液的导电性更强
C.k的单质与水反应更剧烈
您最近一年使用:0次



