1 . 回答下列问题
(1)为什么副族元素又称为过渡元素?_______
(2)为什么在元素周期表中非金属元素主要集中在右上角三角区内?处于非金属三角区边缘的元素常被称为半金属或准金属。为什么?_______
(3)在周期表里找出Cr和Cu的价层电子,它们的电子排布符合构造原理吗?此外还有哪些元素的基态原子电子排布不符合构造原理?_______
(4)预言119号元素基态原子最外层电子排布;预言第八周期有多少种元素?_______
(5)对角线规则:元素周期表中的某些主族元素其某些性质与_______ 元素相似。
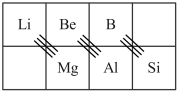
如铍、铝两元素的性质相似性
(1)为什么副族元素又称为过渡元素?
(2)为什么在元素周期表中非金属元素主要集中在右上角三角区内?处于非金属三角区边缘的元素常被称为半金属或准金属。为什么?
(3)在周期表里找出Cr和Cu的价层电子,它们的电子排布符合构造原理吗?此外还有哪些元素的基态原子电子排布不符合构造原理?
(4)预言119号元素基态原子最外层电子排布;预言第八周期有多少种元素?
(5)对角线规则:元素周期表中的某些主族元素其某些性质与

如铍、铝两元素的性质相似性
| 与酸反应 | 与碱反应 | |
| 单质 | ||
| 氧化物 | ||
| 氢氧化物 |
您最近一年使用:0次
2 . 在周期表中,与 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是___________ ,该元素基态原子核外M层电子的自旋状态___________ (填“相同”或“相反”)。 基态核外电子排布式为
基态核外电子排布式为___________ 。
 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是 基态核外电子排布式为
基态核外电子排布式为
您最近一年使用:0次
3 . 在周期表中,与Li的化学性质最相似的邻族元素是__ ,该元素基态原子核外M层电子的自旋状态__ (填“相同”或“相反”)。
您最近一年使用:0次
2021-02-19更新
|
837次组卷
|
5卷引用:(人教版2019)选择性必修2 第一章 原子结构与性质 C高考挑战区
(人教版2019)选择性必修2 第一章 原子结构与性质 C高考挑战区(已下线)考点33 原子结构与性质-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点46 原子结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第29讲 原子结构与性质(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)01 常考题空1 电子排布、电离能与电负性 (解析)-备战2023年高考化学大题逐空突破系列(全国通用)
4 . 在周期表中,同一主族元素化学性质相似。目前也发现某些元素的性质和它在周期表中右下方的另一主族元素性质相似,这称为对角线规则。
据此请回答下列问题:
(1)锂在空气中燃烧,除生成__ 外,也生成微量的__ 。
(2)铍的最高价氧化物对应的水化物的化学式是__ ,属于两性化合物,证明这一结论的有关离子方程式为__ 。
(3)若已知反应Be2C+4H2O=2Be(OH)2+CH4↑,则Al4C3与足量强碱溶液反应的离子方程式为__ 。
(4)科学家证实,BeCl2属于共价化合物,设计一个简单实验证明,其方法是__ 。用电子式表示BeCl2的形成过程:__ 。
据此请回答下列问题:
(1)锂在空气中燃烧,除生成
(2)铍的最高价氧化物对应的水化物的化学式是
(3)若已知反应Be2C+4H2O=2Be(OH)2+CH4↑,则Al4C3与足量强碱溶液反应的离子方程式为
(4)科学家证实,BeCl2属于共价化合物,设计一个简单实验证明,其方法是
您最近一年使用:0次
解题方法
5 . 目前已发现,在元素周期表中某些元素与右下方的主族元素的有些性质相似,这种相似性被称为对角线规则。据此回答下列问题:
(1)铍的最高价氧化物对应水化物的化学式是______ ,属于两性化合物,证明这一结论的有关离子方程式为______ 、______ 。
(2)若已知反应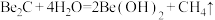 ,则
,则 与足量强碱溶液反应的离子方程式为
与足量强碱溶液反应的离子方程式为______ 。
(3)科学家证实, 属于共价化合物,请设计一个简单实验证明,方法是
属于共价化合物,请设计一个简单实验证明,方法是______ 。用电子式表示 的形成过程:
的形成过程:______ 。
(1)铍的最高价氧化物对应水化物的化学式是
(2)若已知反应
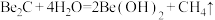 ,则
,则 与足量强碱溶液反应的离子方程式为
与足量强碱溶液反应的离子方程式为(3)科学家证实,
 属于共价化合物,请设计一个简单实验证明,方法是
属于共价化合物,请设计一个简单实验证明,方法是 的形成过程:
的形成过程:
您最近一年使用:0次
6 . 元素周期表中的某些元素之间存在着特殊的“对角线”关系,如Li和Mg、Be和Al、B和Si性质相似。下列说法不正确的是
| A.氢氧化铍是两性氢氧化物 |
| B.B、Si的电负性相近 |
| C.Li、Mg的原子半径相近,且核外电子排布相似 |
D.Li在O2中燃烧生成 |
您最近一年使用:0次
2021-02-16更新
|
198次组卷
|
4卷引用:(人教版2019)选择性必修2 第一章 原子结构与性质 第二节 原子结构与元素的性质
7 . 根据元素周期表中的对角线规则,下列说法或推论错误的是
A.实验室可用 溶液鉴别 溶液鉴别 和 和 |
B. 是共价化合物,则 是共价化合物,则 也是共价化合物 也是共价化合物 |
| C.Si的熔点高、硬度大,则B也具有高熔点和大的硬度 |
D.碱金属元素的单质与 反应均可生成两种及以上的氧化物 反应均可生成两种及以上的氧化物 |
您最近一年使用:0次
8 . (1)观察Li、Be、Mg、Al在元素周期表中的位置回答下列问题:______ (填“酸性”“碱性”或“两性”)化合物,证明这一结论的有关的离子方程式是______ 。
②根据Mg在空气中的燃烧情况可知,Li在空气中燃烧,生成的产物为______ (用化学式表示)。
(2)现有核电荷数小于20的元素A,其电离能数据如表:( 表示原子失去第n个电子的电离能,单位:
表示原子失去第n个电子的电离能,单位: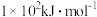 )
)
①外层电子离核越远,能量越高,电离能越______ (填“大”或“小”);阳离子所带电荷数越大,失去电子时,电离能越______ (填“大”或“小”)。
②表中11个电子分属______ 个电子层;失去了11个电子后,该元素原子还有______ 个电子。
③该元素最高价氧化物对应的水化物的化学式是______ 。
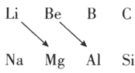
②根据Mg在空气中的燃烧情况可知,Li在空气中燃烧,生成的产物为
(2)现有核电荷数小于20的元素A,其电离能数据如表:(
 表示原子失去第n个电子的电离能,单位:
表示原子失去第n个电子的电离能,单位: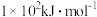 )
)| 序号 |  |  |  |  | 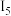 |  | 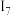 | 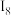 | 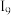 |  |  | … |
| 电离能 | 7.644 | 15.03 | 80.12 | 109.3 | 141.2 | 186.5 | 224.9 | 266.0 | 327.9 | 367.4 | 1761 | … |
②表中11个电子分属
③该元素最高价氧化物对应的水化物的化学式是
您最近一年使用:0次
2021-02-06更新
|
477次组卷
|
2卷引用:高二选择性必修2(人教版2019)第一章 原子结构与性质 第二节 原子结构与元素的性质 课时2 元素周期律
9 . 已知对角线规则为:沿周期表中金属与非金属分界线方向对角的两主族元素性质相似,如Li与Mg,Be与Al,B和Si相似,则下列叙述中正确的是
| A.Li在空气中的燃烧产物为Li2O2 |
B.Be(OH)2溶于NaOH可生成BeO |
| C.BeO是两性氧化物 |
| D.B2O3既能溶于强酸又能溶于强碱 |
您最近一年使用:0次
10 . 回答下列问题:
(1)锂和镁在元素周期表中有特殊“对角线”关系,它们的性质相似。下列有关锂及其化合物的叙述不正确的是___ 。
A.Li2SO4难溶于水
B.Li与N2反应产物是Li3N
C.LiOH难溶于水
D.LiOH与Li2CO3受热都易分解
(2)与铝位于对角线位置的第二周期元素是Be,能区别Be(OH)2和Mg(OH)2的一种试剂是___ ,反应的离子方程式为___ 。
(3)门捷列夫在研究元素周期表时,科学地预言了11种尚未发现的元素,为它们在周期表中留下空位。例如,他预测在铝的下方有一个与铝类似的元素“类铝”,后来被法国化学家于1875年发现,命名为镓。它在周期表中的位置是___ 。
(4)关于与镓同主族的第六周期元素性质的推测中不正确的是___ 。
A.单质是银白色较软的金属
B.其氢氧化物是两性氢氧化物
C.在化合物中显+3价
D.单质与盐酸的反应比铝剧烈
(5)写出短周期主族元素中原子半径最大的原子的单质在空气中加热条件下反应产物的电子式___ 。
(1)锂和镁在元素周期表中有特殊“对角线”关系,它们的性质相似。下列有关锂及其化合物的叙述不正确的是
A.Li2SO4难溶于水
B.Li与N2反应产物是Li3N
C.LiOH难溶于水
D.LiOH与Li2CO3受热都易分解
(2)与铝位于对角线位置的第二周期元素是Be,能区别Be(OH)2和Mg(OH)2的一种试剂是
(3)门捷列夫在研究元素周期表时,科学地预言了11种尚未发现的元素,为它们在周期表中留下空位。例如,他预测在铝的下方有一个与铝类似的元素“类铝”,后来被法国化学家于1875年发现,命名为镓。它在周期表中的位置是
(4)关于与镓同主族的第六周期元素性质的推测中不正确的是
A.单质是银白色较软的金属
B.其氢氧化物是两性氢氧化物
C.在化合物中显+3价
D.单质与盐酸的反应比铝剧烈
(5)写出短周期主族元素中原子半径最大的原子的单质在空气中加热条件下反应产物的电子式
您最近一年使用:0次



